
|
|

|
|
| Names | |
|---|---|
| IUPAC name
Potassium hydroxide |
|
| Other names
Caustic potash, Lye, Potash lye, Potassia, Potassium hydrate, KOH |
|
| Identifiers | |
|
CAS Number |
|
|
3D model (JSmol) |
|
| ChEBI |
|
| ChemSpider |
|
| ECHA InfoCard | 100.013.802 |
| EC Number |
|
| E number | E525 (acidity regulators, …) |
|
PubChem CID |
|
| RTECS number |
|
| UNII |
|
| UN number | 1813 |
|
CompTox Dashboard (EPA) |
|
|
InChI
|
|
|
SMILES
|
|
| Properties | |
|
Chemical formula |
KOH |
| Molar mass | 56.11 g mol−1 |
| Appearance | white solid, deliquescent |
| Odor | odorless |
| Density | 2.044 g/cm3 (20 °C)[1] 2.12 g/cm3 (25 °C)[2] |
| Melting point | 360[3] °C (680 °F; 633 K) |
| Boiling point | 1,327 °C (2,421 °F; 1,600 K) |
|
Solubility in water |
85 g/100 mL (-23.2 °C) 97 g/100 mL (0 °C) 121 g/100 mL (25 °C) 138.3 g/100 mL (50 °C) 162.9 g/100 mL (100 °C)[1][4] |
| Solubility | soluble in alcohol, glycerol insoluble in ether, liquid ammonia |
| Solubility in methanol | 55 g/100 g (28 °C)[2] |
| Solubility in isopropanol | ~14 g / 100 g (28 °C) |
| Acidity (pKa) | 14.7[5] |
|
Magnetic susceptibility (χ) |
−22.0·10−6 cm3/mol |
|
Refractive index (nD) |
1.409 (20 °C) |
| Structure | |
|
Crystal structure |
rhombohedral |
| Thermochemistry | |
|
Heat capacity (C) |
65.87 J/mol·K[2] |
|
Std molar |
79.32 J/mol·K[2][6] |
|
Std enthalpy of |
-425.8 kJ/mol[2][6] |
|
Gibbs free energy (ΔfG⦵) |
-380.2 kJ/mol[2] |
| Hazards | |
| GHS labelling: | |
|
Pictograms |
  [7] [7]
|
|
Signal word |
Danger |
|
Hazard statements |
H302, H314[7] |
|
Precautionary statements |
P280, P305+P351+P338, P310[7] |
| NFPA 704 (fire diamond) |
3 0 0 ALK |
| Flash point | Non-flammable |
| Lethal dose or concentration (LD, LC): | |
|
LD50 (median dose) |
273 mg/kg (oral, rat)[9] |
| NIOSH (US health exposure limits): | |
|
PEL (Permissible) |
none[8] |
|
REL (Recommended) |
C 2 mg/m3[8] |
|
IDLH (Immediate danger) |
N.D.[8] |
| Safety data sheet (SDS) | ICSC 0357 |
| Related compounds | |
|
Other anions |
Potassium hydrosulfide Potassium amide |
|
Other cations |
Lithium hydroxide Sodium hydroxide Rubidium hydroxide Caesium hydroxide |
|
Related compounds |
Potassium oxide |
|
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references |
Potassium hydroxide is an inorganic compound with the formula KOH, and is commonly called caustic potash.
Along with sodium hydroxide (NaOH), KOH is a prototypical strong base. It has many industrial and niche applications, most of which exploit its caustic nature and its reactivity toward acids. An estimated 700,000 to 800,000 tonnes were produced in 2005. KOH is noteworthy as the precursor to most soft and liquid soaps, as well as numerous potassium-containing chemicals. It is a white solid that is dangerously corrosive.[10]
Properties and structure[edit]
KOH exhibits high thermal stability. Because of this high stability and relatively low melting point, it is often melt-cast as pellets or rods, forms that have low surface area and convenient handling properties. These pellets become tacky in air because KOH is hygroscopic. Most commercial samples are ca. 90% pure, the remainder being water and carbonates.[10] Its dissolution in water is strongly exothermic. Concentrated aqueous solutions are sometimes called potassium lyes. Even at high temperatures, solid KOH does not dehydrate readily.[11]
Structure[edit]
At higher temperatures, solid KOH crystallizes in the NaCl crystal structure. The OH group is either rapidly or randomly disordered so that the OH− group is effectively a spherical anion of radius 1.53 Å (between Cl− and F− in size). At room temperature, the OH− groups are ordered and the environment about the K+ centers is distorted, with K+−OH− distances ranging from 2.69 to 3.15 Å, depending on the orientation of the OH group. KOH forms a series of crystalline hydrates, namely the monohydrate KOH · H2O, the dihydrate KOH · 2H2O and the tetrahydrate KOH · 4H2O.[12]
Reactions[edit]
Solubility and desiccating properties[edit]
About 121 g of KOH dissolve in 100 mL water at room temperature, which contrasts with 100 g/100 mL for NaOH. Thus on a molar basis, NaOH is slightly more soluble than KOH. Lower molecular-weight alcohols such as methanol, ethanol, and propanols are also excellent solvents. They participate in an acid-base equilibrium. In the case of methanol the potassium methoxide (methylate) forms:
[13]
- KOH + CH3OH → CH3OK + H2O
Because of its high affinity for water, KOH serves as a desiccant in the laboratory. It is often used to dry basic solvents, especially amines and pyridines.
As a nucleophile in organic chemistry[edit]
KOH, like NaOH, serves as a source of OH−, a highly nucleophilic anion that attacks polar bonds in both inorganic and organic materials. Aqueous KOH saponifies esters:
- KOH + RCOOR’ → RCOOK + R’OH
When R is a long chain, the product is called a potassium soap. This reaction is manifested by the «greasy» feel that KOH gives when touched — fats on the skin are rapidly converted to soap and glycerol.
Molten KOH is used to displace halides and other leaving groups. The reaction is especially useful for aromatic reagents to give the corresponding phenols.[14]
Reactions with inorganic compounds[edit]
Complementary to its reactivity toward acids, KOH attacks oxides. Thus, SiO2 is attacked by KOH to give soluble potassium silicates. KOH reacts with carbon dioxide to give potassium bicarbonate:
- KOH + CO2 → KHCO3
Manufacture[edit]
Historically, KOH was made by adding potassium carbonate to a strong solution of calcium hydroxide (slaked lime). The salt metathesis reaction results in precipitation of solid calcium carbonate, leaving potassium hydroxide in solution:
- Ca(OH)2 + K2CO3 → CaCO3 + 2 KOH
Filtering off the precipitated calcium carbonate and boiling down the solution gives potassium hydroxide («calcinated or caustic potash»). This method of producing potassium hydroxide remained dominant until the late 19th century, when it was largely replaced by the current method of electrolysis of potassium chloride solutions.[10] The method is analogous to the manufacture of sodium hydroxide (see chloralkali process):
- 2 KCl + 2 H2O → 2 KOH + Cl2 + H2
Hydrogen gas forms as a byproduct on the cathode; concurrently, an anodic oxidation of the chloride ion takes place, forming chlorine gas as a byproduct. Separation of the anodic and cathodic spaces in the electrolysis cell is essential for this process.[15]
Uses[edit]
KOH and NaOH can be used interchangeably for a number of applications, although in industry, NaOH is preferred because of its lower cost.
Catalyst for hydrothermal gasification process[edit]
In industry, KOH is a good catalyst for hydrothermal gasification process. In this process, it is used to improve the yield of gas and amount of hydrogen in process. For example, production of coke (fuel) from coal often produces much coking wastewater. In order to degrade it, supercritical water is used to convert it to the syngas containing carbon monoxide, carbon dioxide, hydrogen and methane. Using pressure swing adsorption, we could separate various gases and then use power-to-gas technology to convert them to fuel.[16] On the other hand, the hydrothermal gasification process could degrade other waste such as sewage sludge and waste from food factories.
Precursor to other potassium compounds[edit]
Many potassium salts are prepared by neutralization reactions involving KOH. The potassium salts of carbonate, cyanide, permanganate, phosphate, and various silicates are prepared by treating either the oxides or the acids with KOH.[10] The high solubility of potassium phosphate is desirable in fertilizers.
Manufacture of soft soaps[edit]
The saponification of fats with KOH is used to prepare the corresponding «potassium soaps», which are softer than the more common sodium hydroxide-derived soaps. Because of their softness and greater solubility, potassium soaps require less water to liquefy, and can thus contain more cleaning agent than liquefied sodium soaps.[17]
As an electrolyte[edit]
Potassium carbonate, formed from the hydroxide solution leaking from an alkaline battery
Aqueous potassium hydroxide is employed as the electrolyte in alkaline batteries based on nickel-cadmium, nickel-hydrogen, and manganese dioxide-zinc. Potassium hydroxide is preferred over sodium hydroxide because its solutions are more conductive.[18] The nickel–metal hydride batteries in the Toyota Prius use a mixture of potassium hydroxide and sodium hydroxide.[19] Nickel–iron batteries also use potassium hydroxide electrolyte.
Food industry[edit]
In food products, potassium hydroxide acts as a food thickener, pH control agent and food stabilizer. The FDA considers it generally safe as a direct food ingredient when used in accordance with Good Manufacturing Practices.[20] It is known in the E number system as E525.
Niche applications[edit]
Like sodium hydroxide, potassium hydroxide attracts numerous specialized applications, virtually all of which rely on its properties as a strong chemical base with its consequent ability to degrade many materials. For example, in a process commonly referred to as «chemical cremation» or «resomation», potassium hydroxide hastens the decomposition of soft tissues, both animal and human, to leave behind only the bones and other hard tissues.[21] Entomologists wishing to study the fine structure of insect anatomy may use a 10% aqueous solution of KOH to apply this process.[22]
In chemical synthesis, the choice between the use of KOH and the use of NaOH is guided by the solubility or keeping quality of the resulting salt.
The corrosive properties of potassium hydroxide make it a useful ingredient in agents and preparations that clean and disinfect surfaces and materials that can themselves resist corrosion by KOH.[15]
KOH is also used for semiconductor chip fabrication (for example anisotropic wet etching).
Potassium hydroxide is often the main active ingredient in chemical «cuticle removers» used in manicure treatments.
Because aggressive bases like KOH damage the cuticle of the hair shaft, potassium hydroxide is used to chemically assist the removal of hair from animal hides. The hides are soaked for several hours in a solution of KOH and water to prepare them for the unhairing stage of the tanning process. This same effect is also used to weaken human hair in preparation for shaving. Preshave products and some shave creams contain potassium hydroxide to force open the hair cuticle and to act as a hygroscopic agent to attract and force water into the hair shaft, causing further damage to the hair. In this weakened state, the hair is more easily cut by a razor blade.
Potassium hydroxide is used to identify some species of fungi. A 3–5% aqueous solution of KOH is applied to the flesh of a mushroom and the researcher notes whether or not the color of the flesh changes. Certain species of gilled mushrooms, boletes, polypores, and lichens[23] are identifiable based on this color-change reaction.[24]
Safety[edit]
Potassium hydroxide and its solutions are severe irritants to skin and other tissue.[25]
See also[edit]
- Potash
- Soda lime
- Saltwater soap – sailors’ soap
References[edit]
- ^ a b Lide, D. R., ed. (2005). CRC Handbook of Chemistry and Physics (86th ed.). Boca Raton (FL): CRC Press. p. 4-80. ISBN 0-8493-0486-5.
- ^ a b c d e f «potassium hydroxide». chemister.ru. Archived from the original on 18 May 2014. Retrieved 8 May 2018.
- ^ «A18854 Potassium hydroxide». Alfa Aesar. Thermo Fisher Scientific. Archived from the original on 19 October 2015. Retrieved 26 October 2015.
- ^ Seidell, Atherton; Linke, William F. (1952). Solubilities of Inorganic and Organic Compounds. Van Nostrand. Retrieved 2014-05-29.
- ^ Popov, K.; et al. (2002). «7Li, 23Na, 39K and 133Cs NMR comparative equilibrium study of alkali metal cation hydroxide complexes in aqueous solutions. First numerical value for CsOH formation». Inorganic Chemistry Communications. 3 (5): 223–225. doi:10.1016/S1387-7003(02)00335-0. ISSN 1387-7003. Retrieved October 20, 2018.
- ^ a b Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. p. A22. ISBN 978-0-618-94690-7.
- ^ a b c Sigma-Aldrich Co., Potassium hydroxide. Retrieved on 2014-05-18.
- ^ a b c NIOSH Pocket Guide to Chemical Hazards. «#0523». National Institute for Occupational Safety and Health (NIOSH).
- ^ Chambers, Michael. «ChemIDplus — 1310-58-3 — KWYUFKZDYYNOTN-UHFFFAOYSA-M — Potassium hydroxide [JAN:NF] — Similar structures search, synonyms, formulas, resource links, and other chemical information». chem.sis.nlm.nih.gov. Archived from the original on 12 August 2014. Retrieved 8 May 2018.
- ^ a b c d Schultz, Heinz; Bauer, Günter; Schachl, Erich; Hagedorn, Fritz; Schmittinger, Peter (2005). «Potassium Compounds». Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim, Germany: Wiley-VCH. doi:10.1002/14356007.a22_039. ISBN 978-3-527-30673-2.
- ^ Holleman, A. F; Wiberg, E. (2001). Inorganic Chemistry. San Diego: Academic Press. ISBN 978-0-12-352651-9.
- ^ Wells, A.F. (1984). Structural Inorganic Chemistry. Oxford: Clarendon Press. ISBN 978-0-19-855370-0.
- ^ Platonov, Andrew Y.; Kurzin, Alexander V.; Evdokimov, Andrey N. (2009). «Composition of Vapor and Liquid Phases in the Potassium Hydroxide + Methanol Reaction System at 25 °С». J. Solution Chem. 39 (3): 335–342. doi:10.1007/s10953-010-9505-1. S2CID 97177429.
- ^ W. W. Hartman (1923). «p-Cresol». Organic Syntheses. 3: 37. doi:10.15227/orgsyn.003.0037.; Collective Volume, vol. 1, p. 175
- ^ a b Römpp Chemie-Lexikon, 9th Ed. (in German)
- ^ Chen, Fu; Li, Xiaoxiao; Qu, Junfeng; Ma, Jing; Zhu, Qianlin; Zhang, Shaoliang (2020-01-13). «Gasification of coking wastewater in supercritical water adding alkali catalyst». International Journal of Hydrogen Energy. 45 (3): 1608–1614. doi:10.1016/j.ijhydene.2019.11.033. ISSN 0360-3199. S2CID 213336330.
- ^ K. Schumann; K. Siekmann (2005). «Soaps». Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a24_247. ISBN 978-3527306732.
- ^ D. Berndt; D. Spahrbier (2005). «Batteries». Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a03_343. ISBN 978-3527306732.
- ^ «Toyota Prius Hybrid 2010 Model Emergency Response Guide» (PDF). Toyota Motor Corporation. 2009. Archived from the original (PDF) on 2012-03-20.
- ^ «Compound Summary for CID 14797 — Potassium Hydroxide». PubChem.
- ^ Green, Margaret (January 1952). «A RAPID METHOD FOR CLEARING AND STAINING SPECIMENS FOR THE DEMONSTRATION OF BONE». The Ohio Journal of Science. 52 (1): 31–33. hdl:1811/3896.
- ^ Thomas Eisner (2003). For the Love of Insects. Harvard University Press. p. 71.
- ^ Elix, J.A.; Stocker-Wörgötter, Elfie (2008). «Chapter 7: Biochemistry and secondary metabolites». In Nash III, Thomas H. (ed.). Lichen Biology (2nd ed.). New York: Cambridge University Press. pp. 118–119. ISBN 978-0-521-69216-8.
- ^ Testing Chemical Reactions Archived 2009-10-15 at the Wayback Machine at MushroomExpert.com
- ^ Potassium hydroxide, SIDS Initial Assessment Report For SIAM 13. Bern, Switzerland, 6-9 November 2001. Archived 3 January 2018 at the Wayback Machine By Dr. Thaly LAKHANISKY. Date of last Update: February 2002
External links[edit]
- Newscientist article dn10104
- MSDS from JTBaker
- CDC — NIOSH Pocket Guide to Chemical Hazards

|
|

|
|
| Names | |
|---|---|
| IUPAC name
Potassium hydroxide |
|
| Other names
Caustic potash, Lye, Potash lye, Potassia, Potassium hydrate, KOH |
|
| Identifiers | |
|
CAS Number |
|
|
3D model (JSmol) |
|
| ChEBI |
|
| ChemSpider |
|
| ECHA InfoCard | 100.013.802 |
| EC Number |
|
| E number | E525 (acidity regulators, …) |
|
PubChem CID |
|
| RTECS number |
|
| UNII |
|
| UN number | 1813 |
|
CompTox Dashboard (EPA) |
|
|
InChI
|
|
|
SMILES
|
|
| Properties | |
|
Chemical formula |
KOH |
| Molar mass | 56.11 g mol−1 |
| Appearance | white solid, deliquescent |
| Odor | odorless |
| Density | 2.044 g/cm3 (20 °C)[1] 2.12 g/cm3 (25 °C)[2] |
| Melting point | 360[3] °C (680 °F; 633 K) |
| Boiling point | 1,327 °C (2,421 °F; 1,600 K) |
|
Solubility in water |
85 g/100 mL (-23.2 °C) 97 g/100 mL (0 °C) 121 g/100 mL (25 °C) 138.3 g/100 mL (50 °C) 162.9 g/100 mL (100 °C)[1][4] |
| Solubility | soluble in alcohol, glycerol insoluble in ether, liquid ammonia |
| Solubility in methanol | 55 g/100 g (28 °C)[2] |
| Solubility in isopropanol | ~14 g / 100 g (28 °C) |
| Acidity (pKa) | 14.7[5] |
|
Magnetic susceptibility (χ) |
−22.0·10−6 cm3/mol |
|
Refractive index (nD) |
1.409 (20 °C) |
| Structure | |
|
Crystal structure |
rhombohedral |
| Thermochemistry | |
|
Heat capacity (C) |
65.87 J/mol·K[2] |
|
Std molar |
79.32 J/mol·K[2][6] |
|
Std enthalpy of |
-425.8 kJ/mol[2][6] |
|
Gibbs free energy (ΔfG⦵) |
-380.2 kJ/mol[2] |
| Hazards | |
| GHS labelling: | |
|
Pictograms |
  [7] [7]
|
|
Signal word |
Danger |
|
Hazard statements |
H302, H314[7] |
|
Precautionary statements |
P280, P305+P351+P338, P310[7] |
| NFPA 704 (fire diamond) |
3 0 0 ALK |
| Flash point | Non-flammable |
| Lethal dose or concentration (LD, LC): | |
|
LD50 (median dose) |
273 mg/kg (oral, rat)[9] |
| NIOSH (US health exposure limits): | |
|
PEL (Permissible) |
none[8] |
|
REL (Recommended) |
C 2 mg/m3[8] |
|
IDLH (Immediate danger) |
N.D.[8] |
| Safety data sheet (SDS) | ICSC 0357 |
| Related compounds | |
|
Other anions |
Potassium hydrosulfide Potassium amide |
|
Other cations |
Lithium hydroxide Sodium hydroxide Rubidium hydroxide Caesium hydroxide |
|
Related compounds |
Potassium oxide |
|
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references |
Potassium hydroxide is an inorganic compound with the formula KOH, and is commonly called caustic potash.
Along with sodium hydroxide (NaOH), KOH is a prototypical strong base. It has many industrial and niche applications, most of which exploit its caustic nature and its reactivity toward acids. An estimated 700,000 to 800,000 tonnes were produced in 2005. KOH is noteworthy as the precursor to most soft and liquid soaps, as well as numerous potassium-containing chemicals. It is a white solid that is dangerously corrosive.[10]
Properties and structure[edit]
KOH exhibits high thermal stability. Because of this high stability and relatively low melting point, it is often melt-cast as pellets or rods, forms that have low surface area and convenient handling properties. These pellets become tacky in air because KOH is hygroscopic. Most commercial samples are ca. 90% pure, the remainder being water and carbonates.[10] Its dissolution in water is strongly exothermic. Concentrated aqueous solutions are sometimes called potassium lyes. Even at high temperatures, solid KOH does not dehydrate readily.[11]
Structure[edit]
At higher temperatures, solid KOH crystallizes in the NaCl crystal structure. The OH group is either rapidly or randomly disordered so that the OH− group is effectively a spherical anion of radius 1.53 Å (between Cl− and F− in size). At room temperature, the OH− groups are ordered and the environment about the K+ centers is distorted, with K+−OH− distances ranging from 2.69 to 3.15 Å, depending on the orientation of the OH group. KOH forms a series of crystalline hydrates, namely the monohydrate KOH · H2O, the dihydrate KOH · 2H2O and the tetrahydrate KOH · 4H2O.[12]
Reactions[edit]
Solubility and desiccating properties[edit]
About 121 g of KOH dissolve in 100 mL water at room temperature, which contrasts with 100 g/100 mL for NaOH. Thus on a molar basis, NaOH is slightly more soluble than KOH. Lower molecular-weight alcohols such as methanol, ethanol, and propanols are also excellent solvents. They participate in an acid-base equilibrium. In the case of methanol the potassium methoxide (methylate) forms:
[13]
- KOH + CH3OH → CH3OK + H2O
Because of its high affinity for water, KOH serves as a desiccant in the laboratory. It is often used to dry basic solvents, especially amines and pyridines.
As a nucleophile in organic chemistry[edit]
KOH, like NaOH, serves as a source of OH−, a highly nucleophilic anion that attacks polar bonds in both inorganic and organic materials. Aqueous KOH saponifies esters:
- KOH + RCOOR’ → RCOOK + R’OH
When R is a long chain, the product is called a potassium soap. This reaction is manifested by the «greasy» feel that KOH gives when touched — fats on the skin are rapidly converted to soap and glycerol.
Molten KOH is used to displace halides and other leaving groups. The reaction is especially useful for aromatic reagents to give the corresponding phenols.[14]
Reactions with inorganic compounds[edit]
Complementary to its reactivity toward acids, KOH attacks oxides. Thus, SiO2 is attacked by KOH to give soluble potassium silicates. KOH reacts with carbon dioxide to give potassium bicarbonate:
- KOH + CO2 → KHCO3
Manufacture[edit]
Historically, KOH was made by adding potassium carbonate to a strong solution of calcium hydroxide (slaked lime). The salt metathesis reaction results in precipitation of solid calcium carbonate, leaving potassium hydroxide in solution:
- Ca(OH)2 + K2CO3 → CaCO3 + 2 KOH
Filtering off the precipitated calcium carbonate and boiling down the solution gives potassium hydroxide («calcinated or caustic potash»). This method of producing potassium hydroxide remained dominant until the late 19th century, when it was largely replaced by the current method of electrolysis of potassium chloride solutions.[10] The method is analogous to the manufacture of sodium hydroxide (see chloralkali process):
- 2 KCl + 2 H2O → 2 KOH + Cl2 + H2
Hydrogen gas forms as a byproduct on the cathode; concurrently, an anodic oxidation of the chloride ion takes place, forming chlorine gas as a byproduct. Separation of the anodic and cathodic spaces in the electrolysis cell is essential for this process.[15]
Uses[edit]
KOH and NaOH can be used interchangeably for a number of applications, although in industry, NaOH is preferred because of its lower cost.
Catalyst for hydrothermal gasification process[edit]
In industry, KOH is a good catalyst for hydrothermal gasification process. In this process, it is used to improve the yield of gas and amount of hydrogen in process. For example, production of coke (fuel) from coal often produces much coking wastewater. In order to degrade it, supercritical water is used to convert it to the syngas containing carbon monoxide, carbon dioxide, hydrogen and methane. Using pressure swing adsorption, we could separate various gases and then use power-to-gas technology to convert them to fuel.[16] On the other hand, the hydrothermal gasification process could degrade other waste such as sewage sludge and waste from food factories.
Precursor to other potassium compounds[edit]
Many potassium salts are prepared by neutralization reactions involving KOH. The potassium salts of carbonate, cyanide, permanganate, phosphate, and various silicates are prepared by treating either the oxides or the acids with KOH.[10] The high solubility of potassium phosphate is desirable in fertilizers.
Manufacture of soft soaps[edit]
The saponification of fats with KOH is used to prepare the corresponding «potassium soaps», which are softer than the more common sodium hydroxide-derived soaps. Because of their softness and greater solubility, potassium soaps require less water to liquefy, and can thus contain more cleaning agent than liquefied sodium soaps.[17]
As an electrolyte[edit]
Potassium carbonate, formed from the hydroxide solution leaking from an alkaline battery
Aqueous potassium hydroxide is employed as the electrolyte in alkaline batteries based on nickel-cadmium, nickel-hydrogen, and manganese dioxide-zinc. Potassium hydroxide is preferred over sodium hydroxide because its solutions are more conductive.[18] The nickel–metal hydride batteries in the Toyota Prius use a mixture of potassium hydroxide and sodium hydroxide.[19] Nickel–iron batteries also use potassium hydroxide electrolyte.
Food industry[edit]
In food products, potassium hydroxide acts as a food thickener, pH control agent and food stabilizer. The FDA considers it generally safe as a direct food ingredient when used in accordance with Good Manufacturing Practices.[20] It is known in the E number system as E525.
Niche applications[edit]
Like sodium hydroxide, potassium hydroxide attracts numerous specialized applications, virtually all of which rely on its properties as a strong chemical base with its consequent ability to degrade many materials. For example, in a process commonly referred to as «chemical cremation» or «resomation», potassium hydroxide hastens the decomposition of soft tissues, both animal and human, to leave behind only the bones and other hard tissues.[21] Entomologists wishing to study the fine structure of insect anatomy may use a 10% aqueous solution of KOH to apply this process.[22]
In chemical synthesis, the choice between the use of KOH and the use of NaOH is guided by the solubility or keeping quality of the resulting salt.
The corrosive properties of potassium hydroxide make it a useful ingredient in agents and preparations that clean and disinfect surfaces and materials that can themselves resist corrosion by KOH.[15]
KOH is also used for semiconductor chip fabrication (for example anisotropic wet etching).
Potassium hydroxide is often the main active ingredient in chemical «cuticle removers» used in manicure treatments.
Because aggressive bases like KOH damage the cuticle of the hair shaft, potassium hydroxide is used to chemically assist the removal of hair from animal hides. The hides are soaked for several hours in a solution of KOH and water to prepare them for the unhairing stage of the tanning process. This same effect is also used to weaken human hair in preparation for shaving. Preshave products and some shave creams contain potassium hydroxide to force open the hair cuticle and to act as a hygroscopic agent to attract and force water into the hair shaft, causing further damage to the hair. In this weakened state, the hair is more easily cut by a razor blade.
Potassium hydroxide is used to identify some species of fungi. A 3–5% aqueous solution of KOH is applied to the flesh of a mushroom and the researcher notes whether or not the color of the flesh changes. Certain species of gilled mushrooms, boletes, polypores, and lichens[23] are identifiable based on this color-change reaction.[24]
Safety[edit]
Potassium hydroxide and its solutions are severe irritants to skin and other tissue.[25]
See also[edit]
- Potash
- Soda lime
- Saltwater soap – sailors’ soap
References[edit]
- ^ a b Lide, D. R., ed. (2005). CRC Handbook of Chemistry and Physics (86th ed.). Boca Raton (FL): CRC Press. p. 4-80. ISBN 0-8493-0486-5.
- ^ a b c d e f «potassium hydroxide». chemister.ru. Archived from the original on 18 May 2014. Retrieved 8 May 2018.
- ^ «A18854 Potassium hydroxide». Alfa Aesar. Thermo Fisher Scientific. Archived from the original on 19 October 2015. Retrieved 26 October 2015.
- ^ Seidell, Atherton; Linke, William F. (1952). Solubilities of Inorganic and Organic Compounds. Van Nostrand. Retrieved 2014-05-29.
- ^ Popov, K.; et al. (2002). «7Li, 23Na, 39K and 133Cs NMR comparative equilibrium study of alkali metal cation hydroxide complexes in aqueous solutions. First numerical value for CsOH formation». Inorganic Chemistry Communications. 3 (5): 223–225. doi:10.1016/S1387-7003(02)00335-0. ISSN 1387-7003. Retrieved October 20, 2018.
- ^ a b Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. p. A22. ISBN 978-0-618-94690-7.
- ^ a b c Sigma-Aldrich Co., Potassium hydroxide. Retrieved on 2014-05-18.
- ^ a b c NIOSH Pocket Guide to Chemical Hazards. «#0523». National Institute for Occupational Safety and Health (NIOSH).
- ^ Chambers, Michael. «ChemIDplus — 1310-58-3 — KWYUFKZDYYNOTN-UHFFFAOYSA-M — Potassium hydroxide [JAN:NF] — Similar structures search, synonyms, formulas, resource links, and other chemical information». chem.sis.nlm.nih.gov. Archived from the original on 12 August 2014. Retrieved 8 May 2018.
- ^ a b c d Schultz, Heinz; Bauer, Günter; Schachl, Erich; Hagedorn, Fritz; Schmittinger, Peter (2005). «Potassium Compounds». Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim, Germany: Wiley-VCH. doi:10.1002/14356007.a22_039. ISBN 978-3-527-30673-2.
- ^ Holleman, A. F; Wiberg, E. (2001). Inorganic Chemistry. San Diego: Academic Press. ISBN 978-0-12-352651-9.
- ^ Wells, A.F. (1984). Structural Inorganic Chemistry. Oxford: Clarendon Press. ISBN 978-0-19-855370-0.
- ^ Platonov, Andrew Y.; Kurzin, Alexander V.; Evdokimov, Andrey N. (2009). «Composition of Vapor and Liquid Phases in the Potassium Hydroxide + Methanol Reaction System at 25 °С». J. Solution Chem. 39 (3): 335–342. doi:10.1007/s10953-010-9505-1. S2CID 97177429.
- ^ W. W. Hartman (1923). «p-Cresol». Organic Syntheses. 3: 37. doi:10.15227/orgsyn.003.0037.; Collective Volume, vol. 1, p. 175
- ^ a b Römpp Chemie-Lexikon, 9th Ed. (in German)
- ^ Chen, Fu; Li, Xiaoxiao; Qu, Junfeng; Ma, Jing; Zhu, Qianlin; Zhang, Shaoliang (2020-01-13). «Gasification of coking wastewater in supercritical water adding alkali catalyst». International Journal of Hydrogen Energy. 45 (3): 1608–1614. doi:10.1016/j.ijhydene.2019.11.033. ISSN 0360-3199. S2CID 213336330.
- ^ K. Schumann; K. Siekmann (2005). «Soaps». Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a24_247. ISBN 978-3527306732.
- ^ D. Berndt; D. Spahrbier (2005). «Batteries». Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a03_343. ISBN 978-3527306732.
- ^ «Toyota Prius Hybrid 2010 Model Emergency Response Guide» (PDF). Toyota Motor Corporation. 2009. Archived from the original (PDF) on 2012-03-20.
- ^ «Compound Summary for CID 14797 — Potassium Hydroxide». PubChem.
- ^ Green, Margaret (January 1952). «A RAPID METHOD FOR CLEARING AND STAINING SPECIMENS FOR THE DEMONSTRATION OF BONE». The Ohio Journal of Science. 52 (1): 31–33. hdl:1811/3896.
- ^ Thomas Eisner (2003). For the Love of Insects. Harvard University Press. p. 71.
- ^ Elix, J.A.; Stocker-Wörgötter, Elfie (2008). «Chapter 7: Biochemistry and secondary metabolites». In Nash III, Thomas H. (ed.). Lichen Biology (2nd ed.). New York: Cambridge University Press. pp. 118–119. ISBN 978-0-521-69216-8.
- ^ Testing Chemical Reactions Archived 2009-10-15 at the Wayback Machine at MushroomExpert.com
- ^ Potassium hydroxide, SIDS Initial Assessment Report For SIAM 13. Bern, Switzerland, 6-9 November 2001. Archived 3 January 2018 at the Wayback Machine By Dr. Thaly LAKHANISKY. Date of last Update: February 2002
External links[edit]
- Newscientist article dn10104
- MSDS from JTBaker
- CDC — NIOSH Pocket Guide to Chemical Hazards
Определение и формула
Неорганическое соединение.
Альтернативное название
Едкое кали, калия гидроокись
Формула
KOHKOH
Свойства гидроксида калия
Физические свойства
| Свойство | Описание |
|---|---|
| Внешний вид | Белая гигроскопичная масса |
| Молярная масса | 56,11 г/моль |
| Плотность | при 25°С – 2,044 г/см3 |
| Температура плавления | 405°C |
| Температура кипения | 1325°C |
Химические свойства
В водном растворе диссоциирует на ионы:
KOH⟶OH−+K+KOH longrightarrow OH^- + K^+
Среда раствора сильно щелочная.
При взаимодействии с кислотами происходит нейтрализация:
2KOH+H2SO4=2H2O+K2SO42KOH + H_2SO_4 =2H_2O + K_2SO_4
Гидроксид калия вступает в реакции обмена с образованием нерастворимых гидроксидов или оксидов:
2KOH+2AgNO3=Ag2O↓+H2O+2KNO32KOH + 2AgNO_3 = Ag_2O↓ + H_2O + 2KNO_3,
2KOH+FeCl3=Fe(OH)3↓+3KCl2KOH + FeCl_3 = Fe(OH)_3↓ + 3KCl
Расплавленный KOHKOH реагирует с BeBe, AlAl, GaGa, ZnZn, SnSn, PbPb, SbSb и их оксидами и гидроксидами с образованием солей (напр., KAlO2KAlO_2, K2ZnO2K_2ZnO_2) и выделением соответственно H2H_2 или H2OH_2O:
2KOH+Sn=K2SnO2+H2↑2KOH + Sn = K_2SnO_2 + H_2↑,
2KOH+Al2O3=2KAlO2+H2O2KOH + Al_2O_3 = 2KAlO_2 + H_2O,
2KOH+Be(OH)2=K2BeO2+2H2O2KOH + Be(OH)_2 = K_2BeO_2 + 2H_2O.
В водных растворах образуются гидроксокомплексы:
2KOH+Sn+2H2O=K2[Sn(OH)4]+H2↑2KOH + Sn + 2H_2O = K2[Sn(OH)4] + H2↑,
2KOH+Al2O3+2H2O=2K[Al(OH)4]2KOH + Al_2O_3 + 2H_2O = 2K[Al(OH)_4],
2KOH+Be(OH)2=K2[Be(OH)4]2KOH + Be(OH)_2 = K_2[Be(OH)_4].
Водные растворы KOHKOH и его расплав взаимодействует с BB, SiSi, GeGe и их оксидами и кислотами с образованием соотв. KBO2KBO_2, K[B(OH)4]K[B(OH)_4], K2B4O7K_2B_4O_7, полисиликатов и полигерманатов:
2KOH+2B=2KBO2+H2↑2KOH + 2B = 2KBO_2 + H_2↑ (расплав);
2KOH+B+2H2O=K2[B(OH)4].+H2↑2KOH + B + 2H_2O= K_2[B(OH)_4]. + H_2↑ (водный р-р);
2KOH+2SiO2=K2Si2O5+H2O2KOH + 2SiO_2 = K_2Si_2O_5 + H_2O (водный р-р).
При взаимодействии с углекислым и сернистым газом образуются гидрокарбонаты и гидросульфиты:
KOH+CO2=KHCO3KOH + CO_2 =KHCO_3,
KOH+SO2=KHSO3KOH + SO_2 = KHSO_3.
При взаимодействии с диоксидом азота образуется смесь нитрита и нитрата калия:
KOH+2NO2=KNO2+KNO3+H2OKOH + 2NO_2 = KNO_2 + KNO_3 + H_2O.
При взаимодействии с угарным газом образуется формиат калия:
KOH+CO=HCOOKKOH + CO = HCOOK
Определить присутствие ионов калия можно по фиолетовому окрашиванию пламени, правда, обычно перебивает цвет всегда присутствующий рядом натрий. Тогда пламя нужно рассматривать через синий светофильтр.
Получение
Получение в лаборатории
Гидроксид калия в лаборатории получают пропусканием раствора сульфата калия через анионит или взаимодействием раствора поташа K2CO3K_2CO_3 и известковой воды Ca(OH)2Ca(OH)_2:
K2CO3+Ca(OH)2=CaCO3↓+2KOHK_2CO_3 + Ca(OH)_2 = CaCO_3↓ + 2KOH.
Получение в промышленности
Калия гидроксид получают электролизом водных растворов KClKCl или K2CO3K_2CO_3 с железным катодом:
KCl+H2O=KOH+HCl.KCl + H_2O = KOH + HCl.
Также его производят взаимодействием раствора поташа K2CO3K_2CO_3 и известковой воды Ca(OH)2Ca(OH)_2:
K2CO3+Ca(OH)2=CaCO3↓+2KOHK_2CO_3 + Ca(OH)_2 = CaCO_3↓ + 2KOH
Применение
Гидроксид калия применяют:
● для производства жидкого мыла и соединений калия;
● для очистки газов от COCO, CO2CO_2, SO2SO_2, NO2NO_2, H2SH_2S;
● для осушения NH3NH_3, PH3PH_3, N2ON_2O;
● в щелочных аккумуляторах.
Пример решения задачи
Сколько водорода выделится при растворении избытка цинка в 1 л 50% раствора гидроксида калия (ρ=1,516rho=1,516 г/см3)?
Решение
Вес раствора
mp=ρV=1,516⋅1000=1516m_p= rho V =1,516cdot1000 =1516 г.
Вес KOHKOH
mKOH=1516⋅50%/100%=758m_{KOH}=1516cdot50%/100% =758 г
758758 гtext{г} — xx лtext{л}
2KOH+Zn+2H2O=K2[Zn(OH)4]+H2↑2KOH + Zn + 2H_2O = K_2[Zn(OH)_4] + H_2↑
2 моля — 1 моль
2⋅56,112cdot56,11 гtext{г} — 22,422,4 лtext{л}
112,22112,22 гtext{г} — 22,422,4 лtext{л}
Составляем пропорцию:
112,22112,22 гtext{г} KOHKOH — 22,422,4 лtext{л} H2H_2,
758758 гtext{г} KOHKOH — xx лtext{л} H2H_2.
Отсюда
x=758∗22,4112,22=567x=frac{758ast22,4}{112,22} = 567 г.
1 моль KOHKOH – 74,55574,555 гtext{г},
xx молей KOHKOH – 567567 гtext{г}.
Отсюда
x=567∗174,555=151,3x=frac{567ast1}{74,555} = 151,3 л.
Ответ: 151,3151,3 л.text{л}.
Тест по теме «Гидроксид калия»
Физические свойства
Гидроксид калия KOH — неорганическое соединение. Белый, гигроскопичный, плавится и кипит без разложения. Хорошо растворяется в воде.
Относительная молекулярная масса Mr = 56,11; относительная плотность для тв. и ж. состояния d = 2, 044; tпл = 404º C; tкип = 1324º C
Способы получения
1. Гидроксид калия получают электролизом раствора хлорида калия:
2KCl + 2H2O → 2KOH + H2 + Cl2
2. При взаимодействии калия, оксида калия, гидрида калия и пероксида калия с водой также образуется гидроксид калия:
2K + 2H2O → 2KOH + H2
K2O + H2O → 2KOH
2KH + 2H2O → 2KOH + H2
K2O2 + H2O → 2KOH + H2O2
3. Карбонат калия при взаимодействии с гидроксидом кальция образует гидроксид калия:
K2CO3 + Ca(OH)2 → CaCO3↓ + 2KOH
Качественная реакция
Качественная реакция на гидроксид калия — окрашивание фенолфталеина в малиновый цвет.
Химические свойства
1. Гидроксид калия реагируют со всеми кислотами (и сильными, и слабыми, и растворимыми, и нерастворимыми). При этом образуются средние или кислые соли, в зависимости от соотношения реагентов:
3KOH + H3PO4 → K3PO4 + H2O
2KOH + H3PO4 → K2HPO4 + 2H2O
KOH + H3PO4 → KH2PO4 + H2O
2. Гидроксид калия реагирует с кислотными оксидами. При этом образуются средние или кислые соли, в зависимости от соотношения реагентов:
2KOH(избыток) + CO2 → K2CO3 + H2O
KOH + CO2 (избыток) → KHCO3
3. Гидроксид калия реагирует с амфотерными оксидами и гидроксидами. При этом в расплаве образуются средние соли, а в растворе комплексные соли:
2KOH + Al2O3 → 2KAlO2 + H2O
в растворе образуется комплексная соль — тетрагидроксоалюминат:
2KOH + Al2O3 + 3H2O → 2K[Al(OH)4]
4. С кислыми солями гидроксид калия также может взаимодействовать. При этом образуются средние соли, или менее кислые соли:
KOH + KHCO3 → K2CO3 + H2O
5. Гидроксид калия взаимодействует с простыми веществами-неметаллами (кроме инертных газов, азота, кислорода, водорода и углерода).
При этом кремний окисляется до силиката и выделяется водород:
2KOH + Si + H2O → K2SiO3 + H2
Фтор окисляет щелочь. При этом выделяется молекулярный кислород:
4KOH + 2F2 → 4KF + O2 (OF2) + 2H2O
Другие галогены, сера и фосфор — диспропорционируют в растворе гидроксида калия:
3KOH + P4 + 3H2O = 3KH2PO2 + PH3↑
2KOH(холодный) + Cl2 = KClO + KCl + H2O
6KOH(горячий) + 3Cl2 = KClO3 + 5KCl + 3H2O
Сера взаимодействует с гидроксидом калия только при нагревании:
6KOH + 3S = 2K2S + K2SO3 + 3H2O
6. Гидроксид калия взаимодействует с амфотерными металлами, кроме железа и хрома. При этом в расплаве образуются соль и водород:
2KOH + Zn → K2ZnO2 + H2
В растворе образуются комплексная соль и водород:
2KOH + 2Al + 6Н2О = 2K[Al(OH)4] + 3Н2
7. Гидроксид калия вступает в обменные реакции с растворимыми солями.
Хлорид меди (II) реагирует с гидроксидом калия с образованием хлорида калия и осадка гидроксида меди (II):
2KOH + CuCl2 = Cu(OH)2↓+ 2KCl
Также с гидроксидом калия взаимодействуют соли аммония.
Например, при взаимодействии хлорида аммония и гидроксида калия образуются хлорид калия, аммиак и вода:
NH4Cl + KOH = NH3 + H2O + KCl
8. Гидроксид калия проявляет свойства сильного основания. В воде практически полностью диссоциирует, образуя щелочную среду и меняя окраску индикаторов.
KOH ↔ K+ + OH—
9. Гидроксид калия в расплаве подвергается электролизу. При этом на катоде восстанавливается сам литий, а на аноде выделяется молекулярный кислород:
4KOH → 4K + O2 + 2H2O

Онлайн калькуляторы
На нашем сайте собрано более 100 бесплатных онлайн калькуляторов по математике, геометрии и физике.

Справочник
Основные формулы, таблицы и теоремы для учащихся. Все что нужно, чтобы сделать домашнее задание!

Заказать решение
Не можете решить контрольную?!
Мы поможем! Более 20 000 авторов выполнят вашу работу от 100 руб!
Формула гидроксида калия
Определение и формула гидроксида калия
Формула –
Молярная масса равна г/моль.
Физические свойства – твердое вещество белого цвета, весьма гигроскопичный.
Плавится и кипит без разложения.
Хорошо растворяется в воде, с сильным экзотермическим эффектом, создает сильнощелочную среду.
Химические свойства гидроксида калия
- Гидроксид калия проявляет свойства основных гидроксидов (относится к щелочам), поэтому он реагирует с кислотами:
- Реагирует с оксидами неметаллов:
- Гидроксид калия также реагирует с амфотерными соединениями с образованием комплексных солей:
- Реагирует при сплавлении
с оксидом алюминия:
- Реагирует с несолеобразующими оксидами азота:
Получение
Гидроксид калия можно получить непосредственно из самого калия:
При взаимодействии карбоната калия с гидроксидом кальция:
Применение
Применяется в пищевой промышленности в качестве пищевой добавки .
Используется в химическом синтезе.
Находит применение в качестве электролита в щелочных батарейках.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |
| Гидроксид калия | |
 |
|
 |
|
| Общие | |
|---|---|
| Систематическое наименование | Гидроксид калия |
| Традиционные названия | Кали едкое[1], каустический поташ |
| Химическая формула | KOH |
| Эмпирическая формула | KOH |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдое |
| Молярная масса | 56,1056 г/моль |
| Плотность | 2,044 (25 °C) г/см³ |
| Термические свойства | |
| Температура плавления | 380 [2] °C |
| Температура кипения | 1327 °C |
| Энтальпия образования (ст. усл.) | −425,8 кДж/моль |
| Химические свойства | |
| Растворимость в воде | 112,4 (20 °C) |
| Классификация | |
| Рег. номер CAS | 1310-58-3 |
| Номер ООН | 1813 |
| Регистрационный номер EC | 215-181-3 |
| RTECS | TT2100000 |
Гидрокси́д ка́лия (лат. Kalium hydroxidum, англ. Potassium hydroxide, «калиевый щёлок») — KOH.
Тривиальные названия: едкое кали[1], каустический поташ.
Бесцветные, очень гигроскопичные кристаллы, но гигроскопичность меньше, чем у гидроксида натрия. Водные растворы КОН имеют сильнощелочную реакцию. Получают электролизом растворов KCl, применяют в производстве жидких мыл, для получения различных соединений калия.
Химические свойства
- Взаимодействие с кислотами с образованием соли и воды (реакция нейтрализации):
- Взаимодействие с кислотными оксидами с образованием соли и воды:
- Взаимодействие с переходными металлами в растворе с образованием комплексной соли и водорода:
Также гидроксид калия получают электролизом растворов KCl, обычно с применением ртутных катодов, что дает продукт высокой чистоты, не содержащий примеси хлоридов.
Применение
В пищевой промышленности зарегистрирован в качестве пищевой добавки E525.
Также используется для получения метана, поглощения кислотных газов и обнаружения некоторых катионов в растворах. Применяют в производстве жидких мыл, как исходный продукт для получения различных солей калия и т. д.
В циркониевом производстве используется для получения обесфторенной гидроокиси циркония.
В сфере промышленной мойки продукты на основе гидроксида калия, нагретые до 50-60 °С, применяются для очистки изделий из нержавеющей стали от жира и других масляных веществ, а также остатков механической обработки.
Используется в качестве электролита в щелочных (алкалиновых) батарейках.
Также применяется в ресомации — альтернативном способе «захоронения» тел.
Опасность
Действует на кожу и слизистые оболочки прижигающим образом. Особенно опасно попадание даже малейших частиц гидроксида калия в глаза, поэтому все работы с этим веществом должны проводиться в резиновых перчатках и очках. Гидроксид калия разрушает бумагу, кожу и др. материалы органического происхождения.
См. также
- Щёлочи
- Пищевые добавки
Примечания
- ↑ 1 2 Кали едкое, статья БСЭ
- ↑ Гидроксид калия на XuMuK.Ru
|
Пищевые добавки |
|---|
|
Пищевые красители E1xx | Консерванты E2xx | Антиокислители и регуляторы кислотности E3xx | Стабилизаторы, загустители и эмульгаторы E4xx | Регуляторы рН и вещества против слёживания E5xx | Усилители вкуса и аромата, ароматизаторы E6xx | Антибиотики E7xx | Резерв E8xx | Прочие E9xx | Дополнительные вещества E1xxx Прочие: Воск (E900—909) • Глазурь (E910—919) • Восстановитель (E920—929) • Газ для упаковки (E930—949) • Заменители сахара (E950—969) • Вспениватель (E990—999) |
|
Соединения калия |
|---|
|
Азид калия (KN3) • Амид калия (KNH2) • Ацесульфам (C4H4KNO4S) • Ацетат калия (CH3COOK) • Ацетиленид калия (K2C2) • Бензоат тригидрат калия (Брутто-формула:C7H11KO5) • Бромат калия (KBrO3) • Бромид калия (KBr) • Гексагидроксоплатинат(IV) калия (K2[Pt(OH)6]) • Гексагидроксостибат калия (K[Sb(OH)6]) • Гексанитрокобальтат(III) калия (K3[Co(NO3)6]) • Гексаоксибензол калия (C6(OK)6) • Гексафторогерманат калия (K2[GeF6]) • Гексафторокупрат(III) калия (K3CuF6) • Гексафторомолибдат(III) калия (K3MoF6) • Гексафтороплатинат(V) калия (K[PtF6]) • Гексафторосиликат(IV) калия (K2[SiF6]) • Гексафторфосфат калия (KPF6) • Гексахлоропалладат(IV) калия (K2[PdCl6]) • Гексахлороплатинат(IV) калия (K2[PtCl6]) • Гексахлоростаннат(IV) калия (K2[SnCl6]) • Гексахлорплатинат калия (K2PtCl6) • Гексацианоферрат(II) калия (K4[Fe(CN)6]) • Гексацианоферрат(II) тригидрат калия (K4[Fe(CN)6]•3H2O) • Гексацианоферрат(III) калия (K3[Fe(CN)6]) • Гептафторониобат(V) калия (K2[NbF7]) • Гидрид калия (KH) • Гидрокарбонат калия (KHCO3) • Гидроксид калия (KOH) • Гидроортофосфат калия (K2HPO4) • Гидросульфат калия (KHSO4) • Гидросульфид калия (KHS) • Гидросульфит калия (KHSO3) • Гидрофторид калия (KHF2) • Дигидроарсенат калия (KH2AsO4) • Дигидроортофосфат калия (KH2PO4) • Динитрамид калия (KN(NO2)2) • Дисульфат калия (K2S2O7) • Дисульфит калия (K2S2O5) • Дисульфонатнитроксил калия ((KO3S)2NO) • Дитионат калия (K2S2O6) • Дихлородиамминпалладий ([Pd(NH3)2]Cl2) • Дихромат калия (K2Cr2O7) • Дицианоаргентат(I) калия (K[Ag(СN)2]) • Дицианоаурат(I) калия (K[Au(СN)2]) • Иодат калия (KIO3) • Иодид калия (KI) • Карбонат калия (K2CO3) • Манганат калия (K2MnO4) • Метаванадат калия (KVO3) • Метасиликат калия (K2SiO3) • Метафосфат калия (KPO3) • Надпероксид калия (KO2 или K2O4) • Нитрат калия (KNO3) • Нитрит калия (KNO2) • Озонид калия (KO3) • Оксалат калия (K2C2O4) • Оксалат моногидрат калия (K2C2O4•H2O) • Оксид калия (K2O) • Октахлоромолибдат калия (K4Mo2Cl8) • Ортофосфат калия (K3PO4) • Пербромат калия (KBrO4) • Периодат калия (KIO4) • Перманганат калия (KMnO4) • Пероксид калия (K2O2) • Пероксодикарбонат калия (К2С2О6) • Пероксомоносульфат калия (K2SO5) • Пероксодисульфат калия (K2S2O6(O2)) • Перренат калия (KReO4) • Перхлорат калия (KClO4) • Полисульфиды калия (K2Sn) • Политионаты калия (K2SnO6) • Сегнетова соль (NaKC4H4O6) • Соль Джонсона (K[I(I)2]•H2O) • Соль Цейзе (K[Pt(C2H4)Cl3]•H2O) • Сорбат калия (C6H7KO2) • Сульфат гидрат калия-гадолиния • Сульфат гидрат калия-кальция (K2Ca(SO4)2•H2O) • Сульфат калия (K2SO4) • Сульфат калия-кальция (K2Ca(SO4)2) • Сульфат хрома(III)-калия (KCr(SO4)2) Сульфид калия (K2S) • Сульфит дигидрат калия (K2SO3•2H2O) • Сульфит калия (K2SO3) • Тетрагидроалюминат калия (KAlH4) • Тетрагидроксодиоксоосмат(VI) калия (K2[OsO2(OH)4]) • Тетрагидроортотеллурат калия (K2H4TeO6) • Тетраиодомеркурат(II) калия (K2[HgI4]) • Тетранитроплатинат(II) калия (K2[Pt(NO2)4]) • Тетраоксорутенат(VI) калия (K2RuO4) • Тетрапероксохромат(V) калия (K3CrO8) • Тетрасиликат калия (K2Si4O9•H2O) • Тетрахлоромолибдат(III) калия (KMoCl4) • Тетрахлоропалладат(II) калия (K2[PdCl4]) • Тетрахлороплатинат(II) калия (K2[PtCl4]) • Тетрахлороферрат(III) калия (K[FeCl4]) • Тетрахлорплатинат калия (K2PtCl4) • Тетрацианоникколат(II) калия (K2[Ni(CN)4]) • Тетрацианоплатинат(II) калия (K2[Pt(CN)4]) • Тиосульфат калия (K2SO3S) • Тиоцианат калия (KSCN) • Феррат калия (K2FeO4) • Феррооксалат калия (K3[Fe(C2O4)3]) • Формиат калия (HCOOK) Фталимид калия • Фторид калия (KF) • Фторсульфит калия (KSO2F) • Хлорат калия (KClO3) • Хлорид калия (KCl) • Хлорид-триэтилалюминий калия ((C2H5)3Al•KCl) • Хромат калия (K2CrO4) • Хромит калия (KCrO2) • Цианат калия (KOCN) • Цианид калия (KCN) • Цианоаурат калия (K[Au(CN)2] • Этилксантогенат калия (C2H5OC(S)SK) • |
|
Растворимость кислот, оснований и солей в воде |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
| Гидроксид калия | |
|---|---|
 |
|
 |
|
| Систематическое наименование |
Гидроксид калия |
| Традиционные названия | Кали едкое, каустический поташ |
| Хим. формула | KOH |
| Состояние | твёрдое |
| Молярная масса | 56,1056 г/моль |
| Плотность | 2,044−2,12 г/см³ |
| Т. плав. | 380−406 °C |
| Т. кип. | 1327 °C |
| Энтальпия образования | −425,8 кДж/моль |
| Энтальпия плавления | 7,5 кДж/моль |
| Энтальпия кипения | 128,9 кДж/моль |
| Давление пара | 1 ± 1 мм рт.ст. |
| Растворимость в воде | 117,9 г/100 мл |
| Растворимость в спирте | 38,7 (28 °C) |
| Показатель преломления | 1.409 |
| Рег. номер CAS | ГОСТ 24363-80 ГОСТ 9285-78 |
| Рег. номер CAS | 1310-58-3 |
| PubChem | 14797 |
| Рег. номер EINECS | 215-181-3 |
| SMILES |
[K+].[OH-] |
| InChI |
1S/K.H2O/h;1H2/q+1;/p-1 KWYUFKZDYYNOTN-UHFFFAOYSA-M |
| Кодекс Алиментариус | E525 |
| RTECS | TT2100000 |
| ChEBI | 32035 |
| Номер ООН | 1813 |
| ChemSpider | 14113 |
| Пиктограммы СГС | |
| NFPA 704 | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. |
Гидроксид калия (лат. Kalii hydroxidum) — неорганическое соединение с формулой KOH.
Тривиальные названия: едкое кали, каустический поташ, а также гидрат окиси калия, гидроокись калия, калиевая щёлочь, калиевый щёлок.
Бесцветные, очень гигроскопичные кристаллы, но гигроскопичность меньше, чем у гидроксида натрия. Водные растворы KOH имеют сильнощелочную реакцию. Получают электролизом растворов KCl, применяют в производстве жидких мыл, для получения различных соединений калия.
Химические свойства
- Взаимодействие с кислотами с образованием соли и воды (реакция нейтрализации):
-
- KOH + HCl ⟶ KCl + H2O
-
- 2KOH + H2SO4 ⟶ K2SO4 + 2H2O
- Взаимодействие с кислотными оксидами с образованием соли и воды:
-
- 2KOH + CO2 ⟶ K2CO3 + H2O
-
- 2KOH + SO3 ⟶ K2SO4 + H2O
- Взаимодействие с некоторыми непереходными металлами в растворе с образованием комплексной соли и водорода:
-
- 2Al + 2KOH + 6H2O ⟶ 2K[Al(OH)4] + 3H2↑
Гидроксид калия получают электролизом растворов KCl, обычно с применением ртутных катодов, что дает продукт высокой чистоты, не содержащий примеси хлоридов:
-
- 2KCl + 2H2O ⟶ 2KOH + H2↑ + Cl2↑
Применение
Гидроксид калия является практически универсальным химическим соединением. Ниже приведены примеры материалов и процессы в которых он используется:
- нейтрализация кислот,
- щелочные элементы,
- катализ
- моющие средства,
- буровые растворы,
- красители,
- удобрения,
- производство пищевых продуктов,
- газоочистка,
- металлургическое производство,
- переработка нефти,
- различные органические и неорганические вещества,
- производство бумаги,
- пестициды,
- фармацевтика,
- регулирование pH,
- карбонат калия и другие калийные соединения,
- мыла,
- синтетический каучук.
В пищевой промышленности обозначается как пищевая добавка E525. Используется как регулятор кислотности, в качестве осушителя и средства для снятия кожицы с овощей, корнеплодов и фруктов. Он также используется в качестве катализатора в некоторых реакциях.
Также используется для получения метана, поглощения кислотных газов и обнаружения некоторых катионов в растворах.
Популярное средство в производстве косметической продукции, вступая в реакцию с жирными маслами расщепляется и омыливает при этом масла.
В циркониевом производстве используется для получения обесфторенного гидроксида циркония.
В сфере промышленной мойки продукты на основе гидроксида калия, нагретые до 50-60 °С, применяются для очистки изделий из нержавеющей стали от жира и других масляных веществ, а также остатков механической обработки.
Используется в качестве электролита в щелочных (алкалиновых) батарейках.
Также применяется в ресомации — альтернативном способе «захоронения» тел.
5 % раствор гидроксида калия используется в медицине для лечения бородавок.
В фотографии используется как компонент проявителей, тонеров, индикаторов тиосульфатов и для удаления эмульсии с фотографических материалов.
Производство
В промышленном масштабе гидроксид калия получают электролизом хлористого калия.
Возможны три варианта проведения электролиза:
- электролиз с твердым асбестовым катодом (диафрагменный метод производства),
- электролиз с полимерным катодом (мембранный метод производства),
- электролиз с жидким ртутным катодом (ртутный метод производства).
В ряду электрохимических методов производства самым легким и удобным способом является электролиз с ртутным катодом, но этот метод наносит значительный вред окружающей среде в результате испарения и утечек металлической ртути. Мембранный метод производства самый эффективный, но и самый сложный.
В то время как диафрагменный и ртутный методы были известны соответственно с 1885 и 1892 гг., мембранный метод появился сравнительно недавно — в 1970 гг.
Основной тенденцией в мировом производстве гидроксида калия в последние 10 лет является переход производителей на мембранный метод электролиза. Ртутный электролиз является устаревшей, экономически невыгодной и негативно действующей на окружающую среду технологией. Мембранный электролиз полностью исключает использование ртути. Экологическая безопасность мембранного метода заключается в том, что сточные воды после очистки вновь подаются в технологический цикл, а не сбрасываются в канализацию.
При использовании данного метода решаются следующие задачи:
- исключается стадия сжижения и испарения хлора,
- водород используется для технологического пара, исключаются газовые выбросы хлора и его соединений.
Мировым лидером в области мембранных технологий является японская компания «Асахи Касэй».
В России производство гидроксида калия осуществляется мембранным (ООО «Сода-Хлорат») методом.
Особенностью технологического оформления производства гидроксида калия является тот факт, что на аналогичных установках электролиза можно выпускать как едкое кали, так и каустическую соду. Это позволяет производителям без существенных капиталовложений переходить на производство гидроксида калия взамен каустической соды, производство которой не столь рентабельно, а сбыт в последние годы усложняется. При этом в случае изменений на рынке возможен безболезненный перевод электролизёров на производство ранее выпускавшегося продукта.
Примером перевода части мощностей с производства гидроксида натрия на гидроксид калия может служить ОАО «Завод полимеров КЧХК», начавший промышленный выпуск едкого кали на пяти электролизерах в 2007 году.
Опасность
Очень сильная щёлочь. В чистом виде действует на кожу и слизистые оболочки прижигающим образом. Особенно опасно попадание даже малейших частиц гидроксида калия в глаза, поэтому все работы с этим веществом должны проводиться в резиновых перчатках и очках. Гидроксид калия разрушает бумагу, кожу и др. материалы органического происхождения.
Поиск химических веществ по названиям или формулам.
Справочник содержит названия веществ и описания химических формул (в т.ч. структурные формулы и скелетные формулы).
Введите часть названия или формулу для поиска:
Языки:
По умолчанию |
Все возможные |
Из списка
|
Применить к найденному
Гидроксид калия
Брутто-формула:
HKO
CAS# 1310-58-3
Категории:
Щёлочи
, Регулятор кислотности
PubChem CID: 14797
| ChemSpider ID: 14113
| CHEBI:32035
| CHEMBL2103983
Названия
Русский:
- Гидроксид калия(IUPAC) [Wiki]
- Кали едкое
- гидроокись калия
- калия гидроксид
- каустический поташ
English:
- Caustic potash
- E525
- Potash lye
- Potassia
- Potassium hydrate
- Potassium hydroxide(IUPAC) [Wiki]
Варианты формулы:
KOH
K^+`HO^-
K-O-H
Химический состав
Реакции, в которых участвует Гидроксид калия
-
2{M} + 2H2O = 2{M}OH + H2″|^»
, где M =
Li Na K Rb -
{M}H + H2O -> {M}OH + H2″|^»
, где M =
Na K Li Rb Cs -
Zn + 2{M}OH + 2H2O -> {M}2[Zn(OH)4] + H2″|^»
, где M =
Na K -
2Al + 2{M}OH + 6H2O -> 2{M}[Al(OH)4] + 3H2″|^»
, где M =
Na K -
2Cu(OH)2 + K2S2O6(O2) + 2KOH -> Cu2O3 + 2K2SO4 + 3H2O
И ещё 284 реакции…
Гидроксид калия
-
Гидрокси́д ка́лия (лат. Kalii hydroxidum) — неорганическое соединение с формулой KOH.
Тривиальные названия: едкое кали, каустический поташ, а также гидрат окиси калия, гидроокись калия, калиевая щёлочь, калиевый щёлок.
Бесцветные, очень гигроскопичные кристаллы, но гигроскопичность меньше, чем у гидроксида натрия. Водные растворы KOH имеют сильнощелочную реакцию. Получают электролизом растворов KCl, применяют в производстве жидких мыл, для получения различных соединений калия.
Источник: Википедия
Связанные понятия
Щёлочи (в русском языке происходит от слова «щёлок», возможно, производное от того же корня, что и др.-исл. «skola» — «стирать») — гидроксиды щелочных, щёлочноземельных металлов и некоторых других элементов, например, таллия. К щелочам относятся хорошо растворимые в воде основания. При диссоциации щёлочи образуют анионы OH− и катион металла.
Гидрокси́д на́трия (лат. Nátrii hydroxídum; другие названия — каустическая сода, едкий натр) — самая распространённая щёлочь, химическая формула NaOH. В год в мире производится и потребляется около 57 млн тонн едкого натра.
Петролейный эфир (нефтяной эфир, масло Шервуда) — смесь легких алифатических углеводородов (пентанов и гексанов), получаемая из попутных нефтяных газов и легких фракций нефти. Бесцветная жидкость с температурой кипения 40—70 °C (лёгкий) и 70—100 °C (тяжёлый), и с плотностью 0,650—0,695 г/см3. Петролейный эфир — растворитель жиров, масел, смол и др. Также используется как топливо для бензиновых зажигалок и каталитических грелок. Часто используется в качестве элюента (подвижной фазы) в жидкостной хроматографии…
У́ксусная кислота (эта́новая кислота) CH3COOH — органическое соединение, cлабая, предельная одноосно́вная карбоновая кислота. Соли и сложные эфиры уксусной кислоты называются ацетатами.
Иоди́д ка́лия (иодистый калий) — неорганическое соединение, калиевая соль иодоводородной кислоты с химической формулой KI. Бесцветная кристаллическая соль, желтеющая на свету. Широко используется в качестве источника иодид-ионов. Менее гигроскопична чем иодид натрия. Применяется в медицине как лекарственное средство, в сельском хозяйстве как удобрение, а также в фотографии и аналитической химии.
Упоминания в литературе
Например, при растворении гидроксида калия в во–де выделяется теплота:
Связанные понятия (продолжение)
Пермангана́т ка́лия (лат. Kalii permanganas, распространённое название в быту — марганцо́вка) — марганцовокислый калий, калиевая соль марганцовой кислоты. Химическая формула — KMnO4. Представляет собой тёмно-фиолетовые, почти чёрные кристаллы, при растворении в воде образующие ярко окрашенный раствор цвета фуксии.
Се́рная кислота́ H2SO4 — сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6). При обычных условиях концентрированная серная кислота — тяжёлая маслянистая жидкость без цвета и запаха, с сильнокислым «медным» вкусом. В технике серной кислотой называют её смеси как с водой, так и с серным ангидридом SO3. Если молярное отношение SO3 : H2O < 1, то это водный раствор серной кислоты, если > 1 — раствор SO3 в серной кислоте (олеум).
Бо́рная кислота́ (ортоборная кислота или лат. acidum Boricum) — слабая, одноосновная кислота Льюиса, часто используемая в качестве инсектицида, антисептика, огнезащитного состава, поглотителя нейтронов или предшественника для получения иных химических составов.
Хроматы — соли хромовой кислоты H2CrO4. Устойчивы в нейтральной и щелочной среде, в кислой среде обратимо переходят в дихроматы — соли дихромовой кислоты H2Cr2O7.
Хлорид аммония (хлористый аммоний; техническое название — нашаты́рь; NH4Cl) — соль аммония, белый кристаллический слегка гигроскопичный порошок без запаха.
Гигроскопи́чность (от др.-греч. ὑγρός «влажный» + σκοπέω «наблюдаю») — способность некоторых веществ поглощать водяные пары из воздуха.
Хло́роводоро́д, хло́ристый водоро́д (HCl) — бесцветный, термически устойчивый ядовитый газ (при нормальных условиях) с резким запахом, дымящий во влажном воздухе, легко растворяется в воде (до 500 объёмов газа на один объём воды) с образованием хлороводородной (соляной) кислоты. При −85,1 °C конденсируется в бесцветную, подвижную жидкость. При −114,22 °C HCl переходит в твёрдое состояние. В твёрдом состоянии хлороводород существует в виде двух кристаллических модификаций: ромбической, устойчивой…
Пирокатехи́н (1,2-дигидроксибензол) — органическое соединение, двухатомный фенол, имеющий химическую формулу С6Н4(ОН)2. Один из трёх возможных изомеров дигидроксибензола, два других — гидрохинон и резорцин. Выглядит как бесцветные кристаллы с запахом фенола. Сильный восстановитель.
Со́ли — сложные вещества, которые в водных растворах диссоциируют на катионы металлов и анионы кислотных остатков. ИЮПАК определяет соли как химические соединения, состоящие из катионов и анионов. Есть ещё одно определение: солями называют вещества, которые могут быть получены при взаимодействии кислот и оснований с выделением воды.
У́ксусный ангидри́д (ангидри́д у́ксусной кислоты́), (CH3CO)2O — бесцветная жидкость с резким запахом, растворимая в бензоле, диэтиловом эфире и других органических растворителях. Находит весьма широкое применение в промышленности и органическом синтезе.
Хлорид алюминия (хлористый алюминий) — неорганическое соединение, соль алюминия и соляной кислоты с химической формулой AlCl3.
Хлори́д ка́льция, CaCl2 — кальциевая соль соляной кислоты. Зарегистрирован в качестве пищевой добавки E509. Считается безвредным.
Соля́ная кислота́ (также хлороводоро́дная, хлористоводоро́дная кислота) — раствор хлороводорода (HCl) в воде, сильная одноосновная кислота. Бесцветная, прозрачная, едкая жидкость, «дымящаяся» на воздухе (техническая соляная кислота — желтоватого цвета из-за примесей железа, хлора и пр.). В концентрации около 0,5 % присутствует в желудке человека. Соли соляной кислоты называются хлоридами.
Хлорбензол (фенилхлорид) — ароматическое органическое соединение, имеющее формулу C6H5Cl, бесцветная горючая жидкость с характерным запахом.
Гидра́ты (от др.-греч. ὕδωρ «вода») — продукты присоединения воды к неорганическим и органическим веществам.
Кисло́ты — химические соединения , способные отдавать катион водорода (кислоты Брёнстеда), либо соединения, способные принимать электронную пару с образованием ковалентной связи (кислоты Льюиса).
Азо́тистая кислота HNO2 — слабая одноосновная кислота, существует только в разбавленных водных растворах, окрашенных в слабый голубой цвет, и в газовой фазе. Кислота высокотоксична. Соли азотистой кислоты называются нитритами или азотистокислыми. Нитриты гораздо более устойчивы, чем HNO2, все они токсичны.
Резорцин (резорцинол, 1,3-дигидроксибензол, мета-дигидроксибензол) — органическое соединение c химической формулой С6H4(OH)2, двухатомный фенол. Бесцветные кристаллы со специфическим запахом. Изомерен пирокатехину и гидрохинону, отличаясь от них лишь относительным расположением гидроксильных групп.
Нитробензол — токсичное органическое вещество, имеющее миндальный запах. Формула C6H5NO2.
Щаве́левая кислота, также этандиóвая кислота — органическое соединение, двухосновная предельная карбоновая кислота, с формулой HOOC-COOH, простейшая двухосновная кислота, первый член гомологического ряда двухосновных предельных карбоновых кислот. Принадлежит к сильным органическим кислотам. Обладает всеми химическими свойствами, характерными для карбоновых кислот. Соли и сложные эфиры щавелевой кислоты называются оксалатами. В природе содержится в щавеле, ревене, карамболе и некоторых других растениях…
Аммиа́к (нитрид водорода) — химическое cоединение азота и водорода с формулой NH3, при нормальных условиях — бесцветный газ с резким характерным запахом.
Анили́н (аминобензол, фениламин) — органическое соединение с формулой C6H5NH2, простейший ароматический амин. Представляет собой бесцветную маслянистую жидкость с характерным запахом, немного плотнее воды и плохо в ней растворим, хорошо растворяется в органических растворителях. На воздухе быстро окисляется и приобретает красно-бурую окраску. Ядовит. Название «анилин» происходит от названия одного из растений, содержащих индиго — Indigofera anil (современное международное название растения — Indigofera…
Диметиланилин (N,N-диметиланилин) — органическое соединение, принадлежащее классу третичных аминов. Формально является производным аммиака, в котором атомы водорода замещены на фенильный и два метильных радикала.
Раство́р — гомогенная (однородная) система (точнее, фаза), состоящая из двух или более компонентов и продуктов их взаимодействия.
Тиосульфа́т на́трия (антихлор, гипосульфит, сульфидотриоксосульфат натрия, натрий серноватистокислый) — Na2S2O3 или Na2SO3S, соль натрия и тиосерной кислоты, образует кристаллогидрат Na2S2O3·5H2O.
Циклогексанон — органическое соединение, алициклический кетон, бесцветная маслянистая жидкость с запахом ацетона и мяты.
Тетрагидрофуран (тетраметиленоксид, фуранидин, оксолан) — химическое вещество, циклический простой эфир. Бесцветная легколетучая жидкость с характерным «эфирным» запахом. Важный апротонный растворитель. Широко применяется в органическом синтезе. Химическая формула: C4H8O.
Ацетонитри́л (нитрил уксусной кислоты, этаннитрил, метилцианид) — органическое химическое соединение с формулой CH3CN. Представляет собой бесцветную жидкость со слабым эфирным запахом. Широко используется в органической химии в качестве растворителя.
Амиловый спирт C5H11OH и его изомеры — предельные одноатомные спирты. Известны все 8 изомерных амиловых спиртов.
Азо́тная кислота́ (HNO3) — сильная одноосновная кислота. Твёрдая азотная кислота образует две кристаллические модификации с моноклинной и ромбической решётками.
Глико́ли (дио́лы, двухатомные спирты) — класс органических соединений, содержащих в молекуле две гидроксильные группы. Имеют общую формулу CnH2n(OH)2. Простейшим гликолем является этиленгликоль НО-СН2-СН2-ОН.
Хлорсульфо́новая кислота, HSO3Cl — монохлорангидрид серной кислоты, бесцветная, дымящая на воздухе и резко пахнущая жидкость.
Фтороводоро́д (фтористый водород, гидрофторид, фторид водорода, HF) — бесцветный токсичный газ (при стандартных условиях) с резким запахом, при комнатной температуре существует преимущественно в виде димера H2F2, ниже 19,9°C — бесцветная подвижная летучая жидкость. Смешивается с водой в любом отношении с образованием фтороводородной (плавиковой) кислоты. Образует с водой азеотропную смесь с концентрацией 35,4 % HF.
Хиноли́н (бензопиридин) — органическое соединение гетероциклического ряда. Применяют как растворитель для серы, фосфора и др., для синтеза органических красителей. Производные хинолина используют в медицине (плазмоцид, хинин).
Сульфа́т алюми́ния — сложное неорганическое соединение, соль алюминия и серной кислоты с химической формулой Al2(SO4)3. Выглядит как бесцветные кристаллы, может образовывать кристаллогидраты с различным содержанием воды. Применяется при очистке воды, крашении тканей, дублении кож, как реактив в фотографии, для получения квасцов.
Аминосульфоновая кислота (Сульфаминовая кислота, моноамид серной кислоты, амидосерная кислота) — кислота, формула которой NH2SO2OH (также NH2SO3H). Производные этой кислоты называют сульфаматами.
Растворитель — жидкое, твёрдое или газообразное вещество, способное растворять другие твёрдые, жидкие или газообразные вещества. Обычно используются как органические растворители в химчистках (например, тетрахлорэтилен), как бытовые растворители (например, ацетон, скипидар), для удаления лаков и клея (ацетон, метиловый спирт, этилацетат), в моющих средствах (цитрусовые терпены), в парфюмерии (этанол) и в химическом синтезе. Обычно растворитель и растворяемое вещество одинаковы по своей природе…
Дихлормета́н (метиленхлорид, хлористый метилен, ДХМ, CH2Cl2) — прозрачная легкоподвижная и легколетучая жидкость с характерным для галогенпроизводных запахом. Впервые был синтезирован в 1840 году выдерживанием смеси хлора с хлористым метилом на свету.
Ами́д на́трия — неорганическое вещество с формулой NaNH2, производное аммиака. Представляет собой твёрдое вещество, которое реагирует с водой. Применяется в органическом синтезе.
Спирты́ (от лат. spiritus — дух; устар. алкого́ли, от араб. الكحول аль-кухуль — порошок) — органические соединения, содержащие одну или более гидроксильных групп (гидроксил, −OH), непосредственно связанных с насыщенным (находящимся в состоянии sp³-гибридизации) атомом углерода. Спирты можно рассматривать как производные воды (H−O−H), в которых один атом водорода замещен на органическую функциональную группу: R−O−H.
Этилацетат (этиловый эфир уксусной кислоты) СН3−СОО−CH2−CH3 — бесцветная летучая жидкость с резким запахом.
Раствори́мость — способность вещества образовывать с другими веществами однородные системы — растворы, в которых вещество находится в виде отдельных атомов, ионов, молекул или частиц. Растворимость выражается концентрацией растворённого вещества в его насыщенном растворе либо в процентах, либо в весовых или объёмных единицах, отнесённых к 100 г или 100 см³ (мл) растворителя (г/100 г или см³/100 см³). Растворимость газов в жидкости зависит от температуры и давления. Растворимость жидких и твёрдых…
Сульфид натрия, устар. сернистый натрий, — сложное неорганическое вещество с химической формулой Na2S.
Ацетофенон (метилфенилкетон, C6H5COCH3) — химическое соединение из класса жирноароматических кетонов.
Муравьиная кислота (систематическое наименование: метановая кислота) HCOOH — органическое соединение, первый представитель в ряду насыщенных одноосновных карбоновых кислот. Зарегистрирована в качестве пищевой добавки под обозначением E236. Своё название муравьиная кислота получила потому, что впервые она была выделена в 1670 году английским натуралистом Джоном Рэйем из рыжих лесных муравьёв. В природе также обнаружена у пчёл, в крапиве, хвое. Соли и анионы муравьиной кислоты называются формиатами…
Формула гидроксида калия
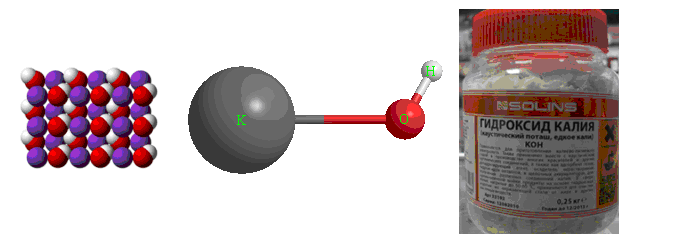
Определение и формула гидроксида калия
ОПРЕДЕЛЕНИЕ
Гидроксид калия (едкий калий) — это сложное химическое соединение, принадлежащее к классу оснований.
Формула – (
K O H
)
Молярная масса равна 56,11 г/моль.
Физические свойства – твердое вещество белого цвета, весьма гигроскопичный.
Плавится и кипит без разложения.
Хорошо растворяется в воде, с сильным экзотермическим эффектом, создает сильнощелочную среду.
Химические свойства гидроксида калия
Гидроксид калия проявляет свойства основных гидроксидов (относится к щелочам), поэтому он реагирует с кислотами:
(
2 K O H+H N O_{3}=K N O_{3}+H_{2} O
)
Реагирует с оксидами неметаллов:
(
2 K O H+C O_{2}=K_{2} C O_{3}+H_{2} O
)
Гидроксид калия также реагирует с амфотерными соединениями с образованием комплексных солей:
(
K O H+A l(O H)_{3}=Kleft[A l(O H)_{4}right]
)
Реагирует при сплавлении (
left(900-1100^{circ} mathrm{C}right)
) с оксидом алюминия:
(
2 K O H+A l_{2} O_{3}=2 K A l O_{2}+H_{2} O
)
Реагирует с несолеобразующими оксидами азота:
(
2 K O H+N O+N O_{2}=2 K N O_{2}+H_{2} O
)
Получение
Гидроксид калия можно получить непосредственно из самого калия:
(
2 K+2 H_{2} O=2 K O H+H_{2} uparrow
)
(
4 K+O_{2}+2 H_{2} O=4 K O H
)
При взаимодействии карбоната калия с гидроксидом кальция:
(
K_{2} C O_{3}+C a(O H)_{2}=C a C O_{3} downarrow+2 K O H
)
Применение
Применяется в пищевой промышленности в качестве пищевой добавки E525.
Используется в химическом синтезе.
Находит применение в качестве электролита в щелочных батарейках.
Примеры решения задач
ПРИМЕР 1
Определите массовую долю гидроксида в растворе, который имеет осмотическое давление 1 атм при (
25^{circ }
)
Гидроксид калия — сильный электролит и диссоциирует нацело с образованием двух частиц:
(
K O H rightarrow K^{+}+O H^{-}
)
Запишем выражение для определения осмотического давления для сильного электролита:
(
pi=i cdot C_{M} cdot R cdot T
)
где i — изотонический коэффициент, равный числу ионов, на которые распадается сильный электролит.
(
i(K O H)=2
)
(
T=25^{circ} mathrm{C}=298 K
)
(
pi=1 mathrm{aTM}=101325 mathrm{ПА}
)
(
R=3,314 Дж/(Мольcdot K)
)
(
C_{M}(K O H)=frac{pi}{i cdot R cdot T}=frac{101325}{2 cdot 8,314 cdot 298}=20,45 моль/м^{3} =0,02045 моль/л
)
Пересчитаем молярную концентрацию в массовую долю, приняв плотность раствора за единицу, так как концентрация мала:
(
omega(K O H)=frac{C_{M}(K O H) cdot M(K O H)}{rho_{s o l u t i o n} cdot 1000}
)
Подставим численные значения:
(
omega(K O H)=frac{0,02045 cdot 56,11}{1 cdot 1000}=1,147 cdot 10^{-3}
)
(
omega(K O H)=0,115 %
)
ПРИМЕР 2
Вычислите pH 0, 001 M раствора KOH в приближении идеального раствора.
Запишем уравнение электролитической диссоциации KOH в водном растворе:
(
K O H rightarrow K^{+}+O H^{-}
)
Из уравнения диссоциации следует, что :
(
C_{M}left(K^{+}right)=C_{M}left(O H^{-}right)=C_{M}(K O H)=0,001
) моль/л
Рассчитаем pH в приближении идеального раствора:
(
p H=14-p O H=14+lg C_{M}left(O H^{-}right)=14+lg 0,001=11
)
pH (идеальный раствор) = 11







![mathsf{2 Al + 2 KOH + 6 H_2O longrightarrow 2 K[Al(OH)_4] + 3 H_2 uparrow}](https://dic.academic.ru/dic.nsf/ruwiki/4336662437d736e1de529b709e1c3810.png)

