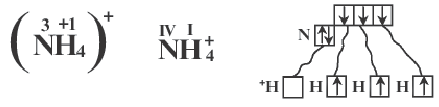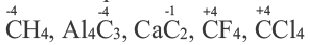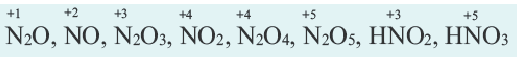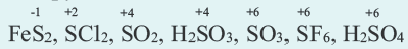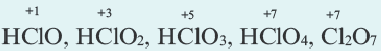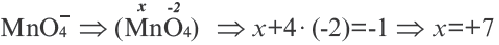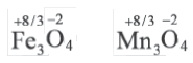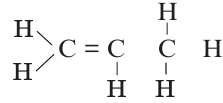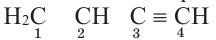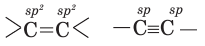Ionic bonding is a type of chemical bonding that involves the electrostatic attraction between oppositely charged ions, or between two atoms with sharply different electronegativities,[1] and is the primary interaction occurring in ionic compounds. It is one of the main types of bonding, along with covalent bonding and metallic bonding. Ions are atoms (or groups of atoms) with an electrostatic charge. Atoms that gain electrons make negatively charged ions (called anions). Atoms that lose electrons make positively charged ions (called cations). This transfer of electrons is known as electrovalence in contrast to covalence. In the simplest case, the cation is a metal atom and the anion is a nonmetal atom, but these ions can be of a more complex nature, e.g. molecular ions like NH+
4 or SO2−
4. In simpler words, an ionic bond results from the transfer of electrons from a metal to a non-metal in order to obtain a full valence shell for both atoms.
It is important to recognize that clean ionic bonding — in which one atom or molecule completely transfers an electron to another — cannot exist: all ionic compounds have some degree of covalent bonding, or electron sharing. Thus, the term «ionic bonding» is given when the ionic character is greater than the covalent character – that is, a bond in which there is a large difference in electronegativity between the two atoms, causing the bonding to be more polar (ionic) than in covalent bonding where electrons are shared more equally. Bonds with partially ionic and partially covalent character are called polar covalent bonds.
Ionic compounds conduct electricity when molten or in solution, typically not when solid. Ionic compounds generally have a high melting point, depending on the charge of the ions they consist of. The higher the charges the stronger the cohesive forces and the higher the melting point. They also tend to be soluble in water; the stronger the cohesive forces, the lower the solubility.[2]
Overview[edit]
Atoms that have an almost full or almost empty valence shell tend to be very reactive. Atoms that are strongly electronegative (as is the case with halogens) often have only one or two empty orbitals in their valence shell, and frequently bond with other molecules or gain electrons to form anions. Atoms that are weakly electronegative (such as alkali metals) have relatively few valence electrons, which can easily be shared with atoms that are strongly electronegative. As a result, weakly electronegative atoms tend to distort their electron cloud and form cations.
Formation[edit]
Ionic bonding can result from a redox reaction when atoms of an element (usually metal), whose ionization energy is low, give some of their electrons to achieve a stable electron configuration. In doing so, cations are formed. An atom of another element (usually nonmetal) with greater electron affinity accepts one or more electrons to attain a stable electron configuration, and after accepting electrons an atom becomes an anion. Typically, the stable electron configuration is one of the noble gases for elements in the s-block and the p-block, and particular stable electron configurations for d-block and f-block elements. The electrostatic attraction between the anions and cations leads to the formation of a solid with a crystallographic lattice in which the ions are stacked in an alternating fashion. In such a lattice, it is usually not possible to distinguish discrete molecular units, so that the compounds formed are not molecular in nature. However, the ions themselves can be complex and form molecular ions like the acetate anion or the ammonium cation.
Representation of ionic bonding between lithium and fluorine to form lithium fluoride. Lithium has a low ionization energy and readily gives up its lone valence electron to a fluorine atom, which has a positive electron affinity and accepts the electron that was donated by the lithium atom. The end-result is that lithium is isoelectronic with helium and fluorine is isoelectronic with neon. Electrostatic interaction occurs between the two resulting ions, but typically aggregation is not limited to two of them. Instead, aggregation into a whole lattice held together by ionic bonding is the result.
For example, common table salt is sodium chloride. When sodium (Na) and chlorine (Cl) are combined, the sodium atoms each lose an electron, forming cations (Na+), and the chlorine atoms each gain an electron to form anions (Cl−). These ions are then attracted to each other in a 1:1 ratio to form sodium chloride (NaCl).
- Na + Cl → Na+ + Cl− → NaCl
However, to maintain charge neutrality, strict ratios between anions and cations are observed so that ionic compounds, in general, obey the rules of stoichiometry despite not being molecular compounds. For compounds that are transitional to the alloys and possess mixed ionic and metallic bonding, this may not be the case anymore. Many sulfides, e.g., do form non-stoichiometric compounds.
Many ionic compounds are referred to as salts as they can also be formed by the neutralization reaction of an Arrhenius base like NaOH with an Arrhenius acid like HCl
- NaOH + HCl → NaCl + H2O
The salt NaCl is then said to consist of the acid rest Cl− and the base rest Na+.
The removal of electrons to form the cation is endothermic, raising the system’s overall energy. There may also be energy changes associated with breaking of existing bonds or the addition of more than one electron to form anions. However, the action of the anion’s accepting the cation’s valence electrons and the subsequent attraction of the ions to each other releases (lattice) energy and, thus, lowers the overall energy of the system.
Ionic bonding will occur only if the overall energy change for the reaction is favorable. In general, the reaction is exothermic, but, e.g., the formation of mercuric oxide (HgO) is endothermic. The charge of the resulting ions is a major factor in the strength of ionic bonding, e.g. a salt C+A− is held together by electrostatic forces roughly four times weaker than C2+A2− according to Coulomb’s law, where C and A represent a generic cation and anion respectively. The sizes of the ions and the particular packing of the lattice are ignored in this rather simplistic argument.
Structures[edit]
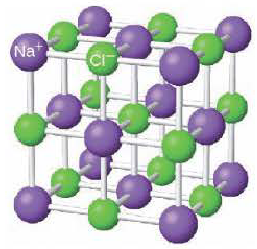
In the rock salt lattice, each sodium ion (purple sphere) has an electrostatic interaction with its eight nearest-neighbour chloride ions (green spheres)
Ionic compounds in the solid state form lattice structures. The two principal factors in determining the form of the lattice are the relative charges of the ions and their relative sizes. Some structures are adopted by a number of compounds; for example, the structure of the rock salt sodium chloride is also adopted by many alkali halides, and binary oxides such as magnesium oxide. Pauling’s rules provide guidelines for predicting and rationalizing the crystal structures of ionic crystals
Strength of the bonding[edit]
For a solid crystalline ionic compound the enthalpy change in forming the solid from gaseous ions is termed the lattice energy. The experimental value for the lattice energy can be determined using the Born–Haber cycle. It can also be calculated (predicted) using the Born–Landé equation as the sum of the electrostatic potential energy, calculated by summing interactions between cations and anions, and a short-range repulsive potential energy term. The electrostatic potential can be expressed in terms of the interionic separation and a constant (Madelung constant) that takes account of the geometry of the crystal. The further away from the nucleus the weaker the shield. The Born–Landé equation gives a reasonable fit to the lattice energy of, e.g., sodium chloride, where the calculated (predicted) value is −756 kJ/mol, which compares to −787 kJ/mol using the Born–Haber cycle.[3][4] In aqueous solution the binding strength can be described by the Bjerrum or Fuoss equation as function of the ion charges, rather independent of the nature of the ions such as polarizability or size [5] The strength of salt bridges is most often evaluated by measurements of equilibria between molecules containing cationic and anionic sites, most often in solution. [6] Equilibrium constants in water indicate additive free energy contributions for each salt bridge. Another method for the identification of hydrogen bonds also in complicated molecules is crystallography, sometimes also NMR-spectroscopy.
The attractive forces defining the strength of ionic bonding can be modeled by Coulomb’s Law. Ionic bond strengths are typically (cited ranges vary) between 170 and 1500 kJ/mol.[7][8]
Polarization power effects[edit]
Ions in crystal lattices of purely ionic compounds are spherical; however, if the positive ion is small and/or highly charged, it will distort the electron cloud of the negative ion, an effect summarised in Fajans’ rules. This polarization of the negative ion leads to a build-up of extra charge density between the two nuclei, that is, to partial covalency. Larger negative ions are more easily polarized, but the effect is usually important only when positive ions with charges of 3+ (e.g., Al3+) are involved. However, 2+ ions (Be2+) or even 1+ (Li+) show some polarizing power because their sizes are so small (e.g., LiI is ionic but has some covalent bonding present). Note that this is not the ionic polarization effect that refers to displacement of ions in the lattice due to the application of an electric field.
Comparison with covalent bonding[edit]
In ionic bonding, the atoms are bound by attraction of oppositely charged ions, whereas, in covalent bonding, atoms are bound by sharing electrons to attain stable electron configurations. In covalent bonding, the molecular geometry around each atom is determined by valence shell electron pair repulsion VSEPR rules, whereas, in ionic materials, the geometry follows maximum packing rules. One could say that covalent bonding is more directional in the sense that the energy penalty for not adhering to the optimum bond angles is large, whereas ionic bonding has no such penalty. There are no shared electron pairs to repel each other, the ions should simply be packed as efficiently as possible. This often leads to much higher coordination numbers. In NaCl, each ion has 6 bonds and all bond angles are 90°. In CsCl the coordination number is 8. By comparison carbon typically has a maximum of four bonds.
Purely ionic bonding cannot exist, as the proximity of the entities involved in the bonding allows some degree of sharing electron density between them. Therefore, all ionic bonding has some covalent character. Thus, bonding is considered ionic where the ionic character is greater than the covalent character. The larger the difference in electronegativity between the two types of atoms involved in the bonding, the more ionic (polar) it is. Bonds with partially ionic and partially covalent character are called polar covalent bonds. For example, Na–Cl and Mg–O interactions have a few percent covalency, while Si–O bonds are usually ~50% ionic and ~50% covalent. Pauling estimated that an electronegativity difference of 1.7 (on the Pauling scale) corresponds to 50% ionic character, so that a difference greater than 1.7 corresponds to a bond which is predominantly ionic.[9]
Ionic character in covalent bonds can be directly measured for atoms having quadrupolar nuclei (2H, 14N, 81,79Br, 35,37Cl or 127I). These nuclei are generally objects of NQR nuclear quadrupole resonance and NMR nuclear magnetic resonance studies. Interactions between the nuclear quadrupole moments Q and the electric field gradients (EFG) are characterized via the nuclear quadrupole coupling constants
- QCC = e2qzzQ/h
where the eqzz term corresponds to the principal component of the EFG tensor and e is the elementary charge. In turn, the electric field gradient opens the way to description of bonding modes in molecules when the QCC values are accurately determined by NMR or NQR methods.
In general, when ionic bonding occurs in the solid (or liquid) state, it is not possible to talk about a single «ionic bond» between two individual atoms, because the cohesive forces that keep the lattice together are of a more collective nature. This is quite different in the case of covalent bonding, where we can often speak of a distinct bond localized between two particular atoms. However, even if ionic bonding is combined with some covalency, the result is not necessarily discrete bonds of a localized character. In such cases, the resulting bonding often requires description in terms of a band structure consisting of gigantic molecular orbitals spanning the entire crystal. Thus, the bonding in the solid often retains its collective rather than localized nature. When the difference in electronegativity is decreased, the bonding may then lead to a semiconductor, a semimetal or eventually a metallic conductor with metallic bonding.
See also[edit]
- Coulomb’s law
- Salt bridge (protein and supramolecular)
- Ionic potential
- Linear combination of atomic orbitals
- Hybridization
- Chemical polarity
- Ioliomics
- Electron configuration
- Aufbau principle
- Quantum numbers
- Azimuthal quantum number
- Principal quantum number
- Magnetic quantum number
- Spin quantum number
References[edit]
- ^ «Ionic bond». IUPAC Compendium of Chemical Terminology. 2009. doi:10.1351/goldbook.IT07058. ISBN 978-0-9678550-9-7.
- ^ Schneider, Hans-Jörg (2012). «Ionic Interactions in Supramolecular Complexes». Ionic Interactions in Natural and Synthetic Macromolecules. pp. 35–47. doi:10.1002/9781118165850.ch2. ISBN 9781118165850.
- ^ David Arthur Johnson, Metals and Chemical Change, Open University, Royal Society of Chemistry, 2002, ISBN 0-85404-665-8
- ^ Linus Pauling, The Nature of the Chemical Bond and the Structure of Molecules and Crystals: An Introduction to Modern Structural Chemistry, Cornell University Press, 1960 ISBN 0-801-40333-2 doi:10.1021/ja01355a027
- ^ Schneider, H.-J.; Yatsimirsky, A. (2000) Principles and Methods in Supramolecular Chemistry. Wiley ISBN 9780471972532
- ^ Biedermann F, Schneider HJ (May 2016). «Experimental Binding Energies in Supramolecular Complexes». Chemical Reviews. 116 (9): 5216–300. doi:10.1021/acs.chemrev.5b00583. PMID 27136957.
- ^ Soboyejo, W.O (2003). Mechanical properties of engineered materials. Marcel Dekker. pp. 16–17. ISBN 0-203-91039-7. OCLC 54091550.
- ^ Askeland, Donald R. (January 2015). The science and engineering of materials. Wright, Wendelin J. (Seventh ed.). Boston, MA. pp. 38. ISBN 978-1-305-07676-1. OCLC 903959750.
- ^ L. Pauling The Nature of the Chemical Bond (3rd ed., Oxford University Press 1960) p.98-100.
External links[edit]
- Ionic bonding tutorial
- Video on ionic bonding
Ionic bonding is a type of chemical bonding that involves the electrostatic attraction between oppositely charged ions, or between two atoms with sharply different electronegativities,[1] and is the primary interaction occurring in ionic compounds. It is one of the main types of bonding, along with covalent bonding and metallic bonding. Ions are atoms (or groups of atoms) with an electrostatic charge. Atoms that gain electrons make negatively charged ions (called anions). Atoms that lose electrons make positively charged ions (called cations). This transfer of electrons is known as electrovalence in contrast to covalence. In the simplest case, the cation is a metal atom and the anion is a nonmetal atom, but these ions can be of a more complex nature, e.g. molecular ions like NH+
4 or SO2−
4. In simpler words, an ionic bond results from the transfer of electrons from a metal to a non-metal in order to obtain a full valence shell for both atoms.
It is important to recognize that clean ionic bonding — in which one atom or molecule completely transfers an electron to another — cannot exist: all ionic compounds have some degree of covalent bonding, or electron sharing. Thus, the term «ionic bonding» is given when the ionic character is greater than the covalent character – that is, a bond in which there is a large difference in electronegativity between the two atoms, causing the bonding to be more polar (ionic) than in covalent bonding where electrons are shared more equally. Bonds with partially ionic and partially covalent character are called polar covalent bonds.
Ionic compounds conduct electricity when molten or in solution, typically not when solid. Ionic compounds generally have a high melting point, depending on the charge of the ions they consist of. The higher the charges the stronger the cohesive forces and the higher the melting point. They also tend to be soluble in water; the stronger the cohesive forces, the lower the solubility.[2]
Overview[edit]
Atoms that have an almost full or almost empty valence shell tend to be very reactive. Atoms that are strongly electronegative (as is the case with halogens) often have only one or two empty orbitals in their valence shell, and frequently bond with other molecules or gain electrons to form anions. Atoms that are weakly electronegative (such as alkali metals) have relatively few valence electrons, which can easily be shared with atoms that are strongly electronegative. As a result, weakly electronegative atoms tend to distort their electron cloud and form cations.
Formation[edit]
Ionic bonding can result from a redox reaction when atoms of an element (usually metal), whose ionization energy is low, give some of their electrons to achieve a stable electron configuration. In doing so, cations are formed. An atom of another element (usually nonmetal) with greater electron affinity accepts one or more electrons to attain a stable electron configuration, and after accepting electrons an atom becomes an anion. Typically, the stable electron configuration is one of the noble gases for elements in the s-block and the p-block, and particular stable electron configurations for d-block and f-block elements. The electrostatic attraction between the anions and cations leads to the formation of a solid with a crystallographic lattice in which the ions are stacked in an alternating fashion. In such a lattice, it is usually not possible to distinguish discrete molecular units, so that the compounds formed are not molecular in nature. However, the ions themselves can be complex and form molecular ions like the acetate anion or the ammonium cation.
Representation of ionic bonding between lithium and fluorine to form lithium fluoride. Lithium has a low ionization energy and readily gives up its lone valence electron to a fluorine atom, which has a positive electron affinity and accepts the electron that was donated by the lithium atom. The end-result is that lithium is isoelectronic with helium and fluorine is isoelectronic with neon. Electrostatic interaction occurs between the two resulting ions, but typically aggregation is not limited to two of them. Instead, aggregation into a whole lattice held together by ionic bonding is the result.
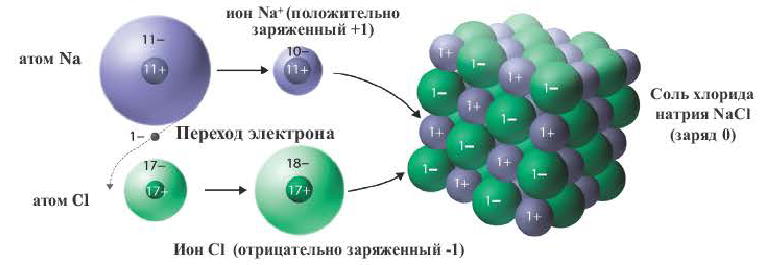
For example, common table salt is sodium chloride. When sodium (Na) and chlorine (Cl) are combined, the sodium atoms each lose an electron, forming cations (Na+), and the chlorine atoms each gain an electron to form anions (Cl−). These ions are then attracted to each other in a 1:1 ratio to form sodium chloride (NaCl).
- Na + Cl → Na+ + Cl− → NaCl
However, to maintain charge neutrality, strict ratios between anions and cations are observed so that ionic compounds, in general, obey the rules of stoichiometry despite not being molecular compounds. For compounds that are transitional to the alloys and possess mixed ionic and metallic bonding, this may not be the case anymore. Many sulfides, e.g., do form non-stoichiometric compounds.
Many ionic compounds are referred to as salts as they can also be formed by the neutralization reaction of an Arrhenius base like NaOH with an Arrhenius acid like HCl
- NaOH + HCl → NaCl + H2O
The salt NaCl is then said to consist of the acid rest Cl− and the base rest Na+.
The removal of electrons to form the cation is endothermic, raising the system’s overall energy. There may also be energy changes associated with breaking of existing bonds or the addition of more than one electron to form anions. However, the action of the anion’s accepting the cation’s valence electrons and the subsequent attraction of the ions to each other releases (lattice) energy and, thus, lowers the overall energy of the system.
Ionic bonding will occur only if the overall energy change for the reaction is favorable. In general, the reaction is exothermic, but, e.g., the formation of mercuric oxide (HgO) is endothermic. The charge of the resulting ions is a major factor in the strength of ionic bonding, e.g. a salt C+A− is held together by electrostatic forces roughly four times weaker than C2+A2− according to Coulomb’s law, where C and A represent a generic cation and anion respectively. The sizes of the ions and the particular packing of the lattice are ignored in this rather simplistic argument.
Structures[edit]
In the rock salt lattice, each sodium ion (purple sphere) has an electrostatic interaction with its eight nearest-neighbour chloride ions (green spheres)
Ionic compounds in the solid state form lattice structures. The two principal factors in determining the form of the lattice are the relative charges of the ions and their relative sizes. Some structures are adopted by a number of compounds; for example, the structure of the rock salt sodium chloride is also adopted by many alkali halides, and binary oxides such as magnesium oxide. Pauling’s rules provide guidelines for predicting and rationalizing the crystal structures of ionic crystals
Strength of the bonding[edit]
For a solid crystalline ionic compound the enthalpy change in forming the solid from gaseous ions is termed the lattice energy. The experimental value for the lattice energy can be determined using the Born–Haber cycle. It can also be calculated (predicted) using the Born–Landé equation as the sum of the electrostatic potential energy, calculated by summing interactions between cations and anions, and a short-range repulsive potential energy term. The electrostatic potential can be expressed in terms of the interionic separation and a constant (Madelung constant) that takes account of the geometry of the crystal. The further away from the nucleus the weaker the shield. The Born–Landé equation gives a reasonable fit to the lattice energy of, e.g., sodium chloride, where the calculated (predicted) value is −756 kJ/mol, which compares to −787 kJ/mol using the Born–Haber cycle.[3][4] In aqueous solution the binding strength can be described by the Bjerrum or Fuoss equation as function of the ion charges, rather independent of the nature of the ions such as polarizability or size [5] The strength of salt bridges is most often evaluated by measurements of equilibria between molecules containing cationic and anionic sites, most often in solution. [6] Equilibrium constants in water indicate additive free energy contributions for each salt bridge. Another method for the identification of hydrogen bonds also in complicated molecules is crystallography, sometimes also NMR-spectroscopy.
The attractive forces defining the strength of ionic bonding can be modeled by Coulomb’s Law. Ionic bond strengths are typically (cited ranges vary) between 170 and 1500 kJ/mol.[7][8]
Polarization power effects[edit]
Ions in crystal lattices of purely ionic compounds are spherical; however, if the positive ion is small and/or highly charged, it will distort the electron cloud of the negative ion, an effect summarised in Fajans’ rules. This polarization of the negative ion leads to a build-up of extra charge density between the two nuclei, that is, to partial covalency. Larger negative ions are more easily polarized, but the effect is usually important only when positive ions with charges of 3+ (e.g., Al3+) are involved. However, 2+ ions (Be2+) or even 1+ (Li+) show some polarizing power because their sizes are so small (e.g., LiI is ionic but has some covalent bonding present). Note that this is not the ionic polarization effect that refers to displacement of ions in the lattice due to the application of an electric field.
Comparison with covalent bonding[edit]
In ionic bonding, the atoms are bound by attraction of oppositely charged ions, whereas, in covalent bonding, atoms are bound by sharing electrons to attain stable electron configurations. In covalent bonding, the molecular geometry around each atom is determined by valence shell electron pair repulsion VSEPR rules, whereas, in ionic materials, the geometry follows maximum packing rules. One could say that covalent bonding is more directional in the sense that the energy penalty for not adhering to the optimum bond angles is large, whereas ionic bonding has no such penalty. There are no shared electron pairs to repel each other, the ions should simply be packed as efficiently as possible. This often leads to much higher coordination numbers. In NaCl, each ion has 6 bonds and all bond angles are 90°. In CsCl the coordination number is 8. By comparison carbon typically has a maximum of four bonds.
Purely ionic bonding cannot exist, as the proximity of the entities involved in the bonding allows some degree of sharing electron density between them. Therefore, all ionic bonding has some covalent character. Thus, bonding is considered ionic where the ionic character is greater than the covalent character. The larger the difference in electronegativity between the two types of atoms involved in the bonding, the more ionic (polar) it is. Bonds with partially ionic and partially covalent character are called polar covalent bonds. For example, Na–Cl and Mg–O interactions have a few percent covalency, while Si–O bonds are usually ~50% ionic and ~50% covalent. Pauling estimated that an electronegativity difference of 1.7 (on the Pauling scale) corresponds to 50% ionic character, so that a difference greater than 1.7 corresponds to a bond which is predominantly ionic.[9]
Ionic character in covalent bonds can be directly measured for atoms having quadrupolar nuclei (2H, 14N, 81,79Br, 35,37Cl or 127I). These nuclei are generally objects of NQR nuclear quadrupole resonance and NMR nuclear magnetic resonance studies. Interactions between the nuclear quadrupole moments Q and the electric field gradients (EFG) are characterized via the nuclear quadrupole coupling constants
- QCC = e2qzzQ/h
where the eqzz term corresponds to the principal component of the EFG tensor and e is the elementary charge. In turn, the electric field gradient opens the way to description of bonding modes in molecules when the QCC values are accurately determined by NMR or NQR methods.
In general, when ionic bonding occurs in the solid (or liquid) state, it is not possible to talk about a single «ionic bond» between two individual atoms, because the cohesive forces that keep the lattice together are of a more collective nature. This is quite different in the case of covalent bonding, where we can often speak of a distinct bond localized between two particular atoms. However, even if ionic bonding is combined with some covalency, the result is not necessarily discrete bonds of a localized character. In such cases, the resulting bonding often requires description in terms of a band structure consisting of gigantic molecular orbitals spanning the entire crystal. Thus, the bonding in the solid often retains its collective rather than localized nature. When the difference in electronegativity is decreased, the bonding may then lead to a semiconductor, a semimetal or eventually a metallic conductor with metallic bonding.
See also[edit]
- Coulomb’s law
- Salt bridge (protein and supramolecular)
- Ionic potential
- Linear combination of atomic orbitals
- Hybridization
- Chemical polarity
- Ioliomics
- Electron configuration
- Aufbau principle
- Quantum numbers
- Azimuthal quantum number
- Principal quantum number
- Magnetic quantum number
- Spin quantum number
References[edit]
- ^ «Ionic bond». IUPAC Compendium of Chemical Terminology. 2009. doi:10.1351/goldbook.IT07058. ISBN 978-0-9678550-9-7.
- ^ Schneider, Hans-Jörg (2012). «Ionic Interactions in Supramolecular Complexes». Ionic Interactions in Natural and Synthetic Macromolecules. pp. 35–47. doi:10.1002/9781118165850.ch2. ISBN 9781118165850.
- ^ David Arthur Johnson, Metals and Chemical Change, Open University, Royal Society of Chemistry, 2002, ISBN 0-85404-665-8
- ^ Linus Pauling, The Nature of the Chemical Bond and the Structure of Molecules and Crystals: An Introduction to Modern Structural Chemistry, Cornell University Press, 1960 ISBN 0-801-40333-2 doi:10.1021/ja01355a027
- ^ Schneider, H.-J.; Yatsimirsky, A. (2000) Principles and Methods in Supramolecular Chemistry. Wiley ISBN 9780471972532
- ^ Biedermann F, Schneider HJ (May 2016). «Experimental Binding Energies in Supramolecular Complexes». Chemical Reviews. 116 (9): 5216–300. doi:10.1021/acs.chemrev.5b00583. PMID 27136957.
- ^ Soboyejo, W.O (2003). Mechanical properties of engineered materials. Marcel Dekker. pp. 16–17. ISBN 0-203-91039-7. OCLC 54091550.
- ^ Askeland, Donald R. (January 2015). The science and engineering of materials. Wright, Wendelin J. (Seventh ed.). Boston, MA. pp. 38. ISBN 978-1-305-07676-1. OCLC 903959750.
- ^ L. Pauling The Nature of the Chemical Bond (3rd ed., Oxford University Press 1960) p.98-100.
External links[edit]
- Ionic bonding tutorial
- Video on ionic bonding
Ионы – это атомы, потерявшие или получившие электроны и, как следствие, некоторый заряд. Для начала хотелось бы напомнить, что ионы бывают двух типов: катионы (положительный заряд ядра больше, чем количество электронов, несущих отрицательный заряд) и анионы (заряд ядра меньше количества электронов). Ионная связь образуется в результате взаимодействия двух ионов с разноименными зарядами.
Ионная и ковалентная связь
Данный тип связи является частным случаем ковалентной. Разность электроотрицательностей в данном случае столь велика (более чем 1,7 по Полингу), что общая пара электронов не частично смещается, а полностью переходит к атому с большей электроотрицательностью. Поэтому образование ионной связи является результатом возникновения сильного электростатического взаимодействия между ионами. Важно понимать, что не существует стопроцентно ионной связи. Данный термин применяется, если «ионные признаки» более выражены (т.е. электронная пара сильно смещена к более электроотрицательному атому).
Механизм ионной связи
Атомы, имеющие практически полную или практически пустую валентную (внешнюю) оболочку, наиболее охотно вступают в химические реакции. Чем меньше пустых орбиталей на валентной оболочке, тем выше шанс, что атом получит электроны извне. И наоборот – чем меньше электронов находится на внешней оболочке, тем вероятнее, что атом отдаст электрон.
Это способность атома притягивать к себе электроны, поэтому атомы с наиболее заполненными валентными оболочками более электроотрицательны.
Типичный металл охотно отдает электроны, тогда как типичный неметалл охотнее их забирает. Поэтому чаще всего ионную связь образуют металлы и неметаллы. Отдельно следует упомянуть другой тип ионной связи – молекулярную. Ее особенность в том, что в роли ионов выступают не отдельные атомы, а целые молекулы.
Схема ионной связи
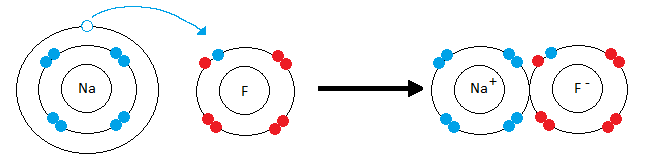
На рисунке схематически изображено формирование фторида натрия. Натрий имеет низкую электроотрицательность и всего один электрон на валентной оболочке (ВО). Фтор – значительно более высокую электроотрицательность, ему не хватает всего одного электрона для заполнения ВО. Электрон с ВО натрия, переходит на ВО фтора, заполняя орбиталь, в следствии чего оба атома приобретают разноименные заряды и притягиваются друг к другу.
Свойства ионной связи
Ионная связь достаточно сильна – разрушить ее при помощи тепловой энергии крайне сложно, а потому вещества с ионной связью имеют высокую температуру плавления. В то же время радиус взаимодействия ионов достаточно низкий, что обуславливает ломкость подобных соединений. Важнейшими ее свойствами являются ненаправленность и ненасыщаемость. Ненаправленность происходит из формы электрического поля иона, которое представляет собой сферу и способно взаимодействовать с катионами или анионами во всех направлениях. При этом поля двух ионов не компенсируются полностью, вследствие чего они вынуждены притягивать к себе дополнительные ионы, образуя кристалл, – это и есть явление, называемое ненасыщаемостью. В ионных кристаллах нет молекул, а отдельные катионы и анионы окружены множеством ионов противоположного знака, количество которых зависит в основном от положения атомов в пространстве.
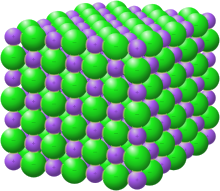
Кристаллы поваренной соли (NaCl) – типичный пример ионной связи.
Таблица веществ с ионной связью
| Название | Формула | Применение и свойства |
|---|---|---|
| Бромид серебра | AgBr | Ионная связь в молекуле разрывается под воздействием фотонов (фотолиз), что широко применяется в фотографии и оптике. |
| Хлорводород | HCl | Как следует из формулы, ионная связь тут образуется между хлором и водородом, а потому водный раствор HCl (соляная кислота), широко применяется для получения различных хлоридов. |
| Оксид кальция | CaO | Негашеная известь. Широко применяется при производстве кирпича. |
| Фторид натрия | NaF | Применяется для укрепления зубной эмали, в производстве керамики. |
Тест по теме «Ионная связь»
Представим, что встретились два атома: атом щелочного металла и атом галогена. У атома металла на внешнем энергетическом уровне — единственный электрон, а атому неметалла как раз не хватает одного электрона, чтобы завершить свой внешний уровень.
Атом металла легко отдаст свой слабо связанный с ядром валентный электрон атому неметалла, который предоставит ему свободное место на внешнем энергетическом уровне. Оба в результате получат заполненные внешние уровни.
Атом металла при этом приобретёт положительный заряд, а атом галогена превратится в отрицательно заряженную частицу. Такие частицы называются ионами.
Ионы — заряженные частицы, в которые превращаются атомы в результате отдачи или принятия электронов.
Образовавшиеся разноимённо заряженные ионы притягиваются друг к другу, и возникает химическая связь, которая называется ионной.
Ионная связь — связь между положительно и отрицательно заряженными ионами.
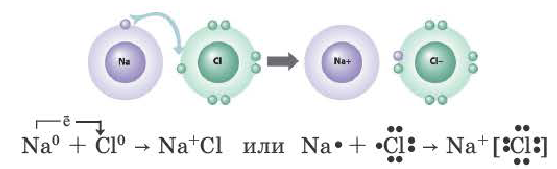
Рассмотрим механизм образования ионной связи на примере взаимодействия натрия и хлора.
Na0+Cl0→Na++Cl−→Na+Cl−
Такое превращение атомов в ионы происходит всегда при взаимодействии атомов типичных металлов и типичных неметаллов, электроотрицательности которых резко различаются.
Ионная связь образуется в сложных веществах, состоящих из атомов металлов и неметаллов.
Рассмотрим другие примеры образования ионной связи.
Пример:
Взаимодействие кальция и фтора
1. Кальций — элемент главной подгруппы второй группы. Ему легче отдать два внешних электрона, чем принять недостающие.
2. Фтор — элемент главной подгруппы седьмой группы. Ему легче принять один электрон, чем отдать семь.
3. Найдём наименьшее общее кратное между зарядами образующихся ионов. Оно равно (2). Определим число атомов фтора, которые примут два электрона от атома кальция: (2) (:) (1) (=) (2).
4. Составим схему образования ионной связи:
Пример:
Взаимодействие натрия и кислорода
1. Натрий — элемент главной подгруппы первой группы. Он легко отдаёт один внешний электрон.
2. Кислород — элемент главной подгруппы шестой группы. Ему легче принять два электрона, чем отдать шесть.
3. Найдём наименьшее общее кратное между зарядами образующихся ионов. Оно равно (2) (:) (1) (=) (2). Определим число атомов натрия, которые отдадут два электрона атому кислорода: (2).
4. Составим схему образования ионной связи:
С помощью ионной связи образуются также соединения, в которых имеются сложные ионы:
.
Значит, ионная связь существует также в солях и основаниях.
Обрати внимание!
Соли аммония
NH4NO3,NH4Cl,NH4SO42
не содержат металла, но образованы ионной связью.
Ионы создают вокруг себя электрическое поле, действующее во всех направлениях. Поэтому каждый ион окружён ионами противоположного знака. Такое соединение представляет собой огромную группу положительных и отрицательных частиц, расположенных в определённом порядке.
Рис. (1). Ионный кристалл
Притяжение между ионами довольно сильное, поэтому ионные вещества имеют высокие температуры кипения и плавления.
Обрати внимание!
Все ионные соединения при обычных условиях — твёрдые вещества.
Примеры веществ с ионной связью:
|
|
|
 |
|
Рис. (2). Питьевая сода |
Рис. (3). Железный купорос |
Рис. (4). Поваренная соль |
Источники:
Рис. 1. Ионный кристалл https://upload.wikimedia.org/wikipedia/commons/e/eb/Sodium_chloride_crystal.png
Рис. 2. Питьевая сода https://pixabay.com/images/id-768950/ 8.06.2021
Рис. 3. Железный купорос https://upload.wikimedia.org/wikipedia/commons/thumb/a/ab/Iron%28II%29-sulfate-heptahydrate-sample.jpg/1280px-Iron%28II%29-sulfate-heptahydrate-sample.jpg
Рис. 4. Поваренная соль https://upload.wikimedia.org/wikipedia/commons/9/93/Chlorid_sodn%C3%BD.JPG
Содержание:
Ионная связь:
Ионы образуются в результате отдачи или присоединения электронов атомами. Атомы, отдающие свои валентные электроны, превращаются в положительно заряженные ионы, а атомы, принимающие эти электроны в отрицательно заряженные ионы. Ионы это заряженные частицы. Положительно заряженные ионы называются катионами, а отрицательно заряженные ионы анионами. Катионы в основном образуются от металлов и ионов аммония. Неметаллы в одиночку не образуют катионов (кроме H+). Из курса физики известно, что положительно и отрицательно заряженные ионы взаимно притягивают друг друга. Следовательно, между положительно и отрицательно заряженными ионами существуют взаимные силы притяжения.
Химическая связь, образованная между ионами в результате действия электростатических сил притяжения, называется ионной связью. Полученное при этом соединение носит название ионного или гетерополярного соединения. Ионная связь образуется между металлами и неметаллами, т.е. между атомами элементов с резко отличающимися электроотрицательностями. Самая сильная ионная связь возникает в солях кислородсодержащих и бескислородных кислот (например, между металлами (щелочные и щелочноземельные металлы) и галогенами), в основаниях. Следовательно, молекула хлорида натрия состоит из ионов натрия (Na+) и хлорид-ионов (Cl).
Свойства ионной связи
Ионной связи присущ целый ряд характерных свойств:
- В соединениях с ионной связью кристаллы состоят не из молекул, а из множества ионов с противоположными зарядами.
- В обычных условиях бывают в твердом состоянии, не проводят электрический ток.
- Расплавы и водные растворы ионных соединений проводят электрический ток.
- Соединения с ионной связью хорошо растворяются в полярных растворителях, легко вступают в химические реакции.
В солях, образованных щелочными металлами с одинаковыми галогенами, по мере возрастания порядкового номера металла, ионная связь усиливается, что объясняется активностью металла (например, в ряду LiF, NaF, K.F, RbF, CsF ). В различных галогенидах одних и тех же металлов по мере возрастания порядкового номера галогена, ионная связь ослабляется (например, NaF, NaCl, NaBr, NaI). Это объясняется ослаблением окислительных способностей (неметаллических свойств) галогена. В солях аммония также между ионом аммония (NH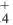
В соединениях с ионной связью число ионных связей равно произведению числа катионов на валентность.
В солях, в составе которых содержится кислород и ион аммония, в том числе и в основаниях, имеются как ионная, так и полярная ковалентная связи.
В основаниях число полярных ковалентных связей равно числу гидроксильных групп.
В нормальных солях число полярных ковалентных связей равно произведению валентности центрального элемента на его индекс. В кислых же солях число полярных ковалентных связей равно произведению суммы валентности центрального элемента и количества H на индекс кислотного остатка.
Если в соединениях разница электроотрицательностей элементов больше 1,7, то это соединение с ионной связью, а если меньше 1,7, с ковалентной связью.
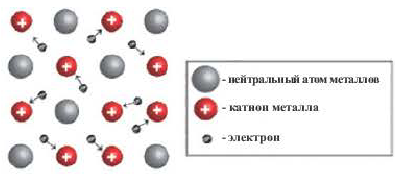
Металлическая связь
Химическая связь, образованная между положительно заряженными ионами металлов и относительно свободными электронами кристаллических решеток, называется металлической связью. Атомы металлов легко отдают свои валентные электроны и превращаются в положительно заряженные ионы. Огносительно свободные электроны, оторвавшись от атомов, движутся между положительными ионами металлов, образуя металлическую связь, те. электроны словно цементируют положительные ионы кристаллической решетки металлов.
Металлическая связь обладает целым рядом характерных свойств:
- При образовании металлической связи валентные электроны относятся не к двум атомам, а ко всему кристаллу.
- Высокая электро- и теплопроводность металлов, их плавление при высокой температуре и способность отражать свет объясняются металлической связью.
- Металлическая связь характерна для металлов и их расплавов.
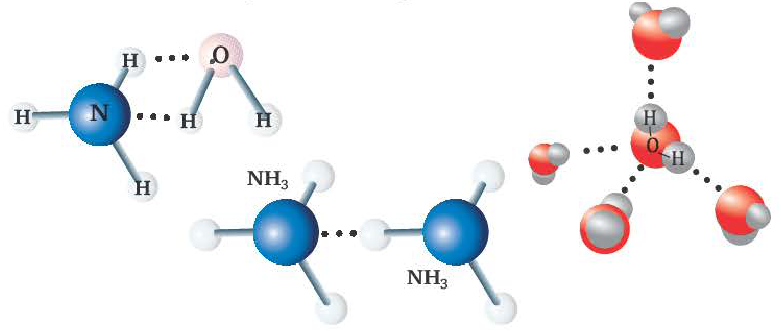
Водородная связь
Химическая связь, образованная между атомом водорода одной молекулы и атомом более сильного электроотрицательного элемента (O,N,F) другой или же аналогичной молекулы, называется водородной связью.
Характерные свойства водородной связи:
- Водородная связь обозначается 3-мя точками.
- Водородная связь в 15 20 раз слабее ковалентной связи.
- Образуется в таких веществах, как NH3, Н2O, HF, в том числе между органическими веществами, содержащими группы ОН, NH2 COOH и др.
- Водородная связь может быть как межмолекулярной, так и внутримолекулярной.
Вода, HF, спирты, водные растворы спиртов образуют межмолекулярные водородные связи. Для белков и многих органических соединений характерна внутримолекулярная водородная связь.
Радиус атома водорода очень маленький и при перемещении или отдаче своего единственного электрона другому атому он становится положительно заряженным. За счет этого водород одной молекулы взаимодействует с находящимися в составе других молекул (HF, Н2О) атомами электроотрицательных элементов с частично отрицательным зарядом.
Образование водородной связи
За счет водородной связи действительная формула воды имеет следующий вид: (H2O)n
При переходе того или иного вещества, образующего водородную связь, из жидкого состояния в газообразное состояние, водородная связь разрывается, а в обратном процессе вновь восстанавливается.
Вода, находясь в твердом (лед) и жидком состояниях, образует водородную связь. При переходе же в газообразное состояние водородная связь разрывается.
При 1 и 2 превращениях водородная связь сохраняется, при третьем состоянии -разрывается, а при четвертом — восстанавливается. Увеличение объема воды при понижении температуры (т.е. объем льда бывает больше объема жидкой воды одинаковой массы, а плотность — меньше) объясняется наличием водородной связи. Эго связано с тем, что при понижении температуры происходит образование более упорядоченной структуры молекул и в результате их «упаковочная» плотность уменьшается.
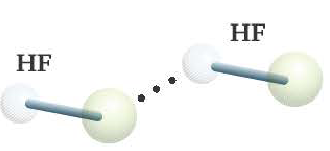
Одна из причин того, что фтористая кислота является слабой кислотой, заключается в ассоциации друг с другом молекул HF посредством водородной связи. Вот почему действительная формула фтороводородной кислоты следующая: (HF)n.
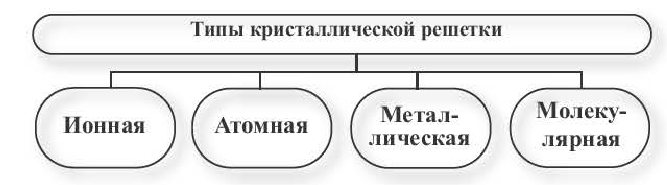
Типы кристаллических решеток
Кристаллические и аморфные вещества:
При механическом раздроблении кусочка хлорида натрия или другого твердого вещества образуются кристаллы определенной формы. Такие вещества называют кристаллическими веществами. Однако существуют и такие твердые вещества (стекло, куски смолы), которые при раздроблении под действием удара образуют осколки неопределенной формы. Такие вещества называют аморфными, т.е. бесформенными веществами.
Частицы (атомы, ионы и т.д.) твердых веществ, располагаясь в строгом порядке, образуют различного типа кристаллические решетки. Точки, в которых размещены частицы, называются узлами кристаллической решетки.
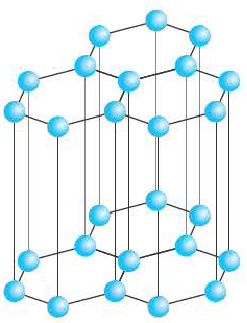
В графите атомы углерода на одной плоскости расположены близко друг к другу, а на разных плоскостях на отдаленном расстоянии друг от друга. Расположение атомов углерода, находящихся на разных плоскостях, в отдалении друг от друга приводит к расслоению графита на чешуйки. Свидетельством тому являются оставленные карандашом следы на бумаге (чешуйки графита).
В зависимости от вида частиц, расположенных в узлах кристаллической решетки, и характера связи между ними, различают четыре типа кристаллической решетки.
В отличие от кристаллических веществ, в аморфных веществах частицы расположены не в такой закономерности, а неупорядоченно.
 |
Профессор Худу Мамедов (1927 1988) являлся член корреспондентом НАНА, доктором геолого минералогических наук, почетным членом Коралевской Академии Великобритании. Его основные научные труды от носятся к области ристаллохимии. Исследовал молекулярное и кристаллическое строения более 50 ти органических комплексных соединений слигандами. |
Ионная кристаллическая решетка. Кристаллические решетки, в узлах которых содержатся соединенные ионными связями положительно и отрицательно заряженные ионы, называются ионными кристаллическими решетками. Ионные кристаллические решетки характерны для оксидов металлов, оснований и солей: NaCl, KCl, NaBr, KBr, N2CO3, Na2SO4, Fe2O3, Ca(OH)2 и др.
Строение кристаллической решетки поваренной соли
Строение кристаллической решетки графита
Из-за сильного притяжения между ионами веществ с ионной кристаллической решеткой, эти вещества отличаются относительной тугоплавкостью, малой летучестью и определенной твёрдостью.
Атомные кристаллические решетки
Кристаллические решетки, в узлах которых содержатся отдельные атомы, связанные друг с другом ковалентной связью, называются атомными кристаллическими решетками.
В атомных кристаллических решетках атомы, как и ионы, располагаются в пространстве в различных положениях, образуя в результате различной формы кристаллы. Например, в узлах кристаллической решетки как алмаза, так и графита содержатся атомы углерода. Однако вследствие их различного расположения, кристаллы алмаза обладают формой тетраэдра, а кристаллы графита слоистой формой.
| Аллотропические видоизменения углерода | Состояния гибридизации углерода | Xимический cocтав | Тип кристаллической решетки | Cтроение кристаллической решетки |
| Алмаз | sp3 | Одинаковый (C) | Атомный | тетраэдрическое |
| Графит | sp2 | слоистое | ||
| Карбин | sp | линейное |
Хотя тип кристаллической решетки аллотропических видоизменений углерода и одинаковый, однако у них различное строение. Примерами веществ, образующих атомную кристаллическую решетку, являются В, С, Si, SiC (карборунд), SiO2, красный и черный фосфор.
Так как в атомных кристаллических решетках этих веществ ковалентные связи между атомами обладают прочностью, для них характерны большая твердость и высокая температура плавления.
Хотя SiC и SiOi обладают атомной кристаллической решеткой, связь между их атомами образована посредством полярной ковалентной связи.
Молекулярная кристаллическая решетка
Кристаллические решетки, в узлах которых содержатся полярные и неполярные молекулы, связанные между собой межмолекулярными силами, называются молекулярными кристаллическими решетками. Молекулярные вещества образуют кристаллические решетки молекулярного типа.
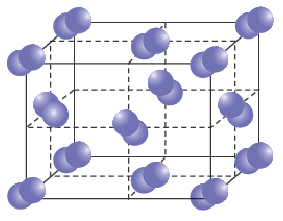
Строение кристаллической решетки йода
Вещества, находящиеся при комнатной температуре в твердом состоянии и образованные только посредством ковалентной связи, в обычных условиях имеют молекулярную кристаллическую решетку, а газообразные, жидкие вещества образуют молекулярную кристаллическую решетку лишь в определенных условиях. В качестве примера веществ с молекулярными кристаллическими решетками в обычных условиях можно привести белый фосфор (Р4), кристаллическую серу (S8), Н3РО4, иод (I2), НРО3, Р2О5, глюкозу (C6H12O6), сахарозу (C12H22O11) и др.
В молекулярных кристаллических решетках веществ с неполярными ковалентными связями (H2, N2, О2, О3, F2, Сl2, Вr2, l2, Р4, S8) связи между молекулами создаются лишь слабыми межмолекулярными силами. В веществах с неполярной ковалентной связью межмолекулярное притяжение слабое. Вследствие этого они обладают очень низкой температурой плавления.
В кристаллических решетках веществ с полярной ковалентной связью (кроме SiC и SiO2) действуют межмолекулярные и электростатические силы притяжения. Значит, только вещества, образованные посредством полярной ковалентной и неполярной ковалентной связи, создают молекулярную кристаллическую решетку. Например, H2O, HCl, HBr, HI, CO2, HNO3, H2SO4, большинство органических веществ и др.
Металлические кристаллические решетки
Кристаллические решетки, в узлах которых содержатся отдельные атомы или ионы металлов, связанные общими электронами, называются металлическими кристаллическими решетками. Большинство металлов (Na, Ca, Fe, Al, Cu и др.), а также расплавов, образуют металлические кристаллические решетки.
Многие свойства металлов электрическая проводимость, теплопроводность, ковкость и др. объясняются свободным движением электронов, образующих металлическую связь.
Некоторые физические свойства веществ зависят от типов кристаллических решеток. В этой связи существует такая закономерность: при известном строении веществ можно заранее предсказать их свойства, и наоборот, если известны свойства веществ, то можно определить их строение.
Вещества, обладающие молекулярной кристаллической решеткой, называются молекулярными (состоят из молекул), а обладающие ионной, атомной и металлической кристаллическими решетками немолекулярными (состоят из атомов или ионов) веществами.
Валентность
Валентность элементов относится к основным понятиям химии.
Валентность — это свойство атомов элементов присоединять или замещать определенное число атомов других элементов. Понятие валентности было введено в науку в 1852 году Эдуардом Франклендом.
Данное определение валентности носит несколько формальный характер, так как не дает представления о природе, свойствах вещества. C развитием учения о химической связи содержание понятия «валентность» в настоящее время обычно выражается так:
Валентность это свойство атомов элементов создавать определенное число ковалентных химических связей.
Валентность определяется числам ковалентных связей, посредством которых в соединениях один атом связывается с другими атомами.
Согласно представлениям о ковалентной связи, независимо от способа образования общих электронных пар, валентность определяется числом общих электронных пар, связывающих атомы в молекуле.
Как вам известно, числовое значение валентности связано с положением элемента в периодической системе химических элементов Д.И.Менделеева. Высшая валентность элемента по числовому значению равна номеру его группы в периодической системе. Некоторые элементы не подчиняются этой закономерности (например, N, О, F). Это связано с тем, что из-за отсутствия в их атомах незаполненных орбиталей, они не могут возбуждаться. Максимальная валентность в соответствующем соединении того или иного элемента определяется числом орбиталей, участвующих в образовании связей в его атоме.
Образование связи в соответствии с валентностью элемента
В образовании иона аммония (NH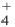
Степень окисления
Степень окисления это условный заряд, который приходится на долю каждого атома в молекуле. Степень окисления может принимать отрицательные, нулевые, положительные и дробные значения. Значение степени окисления определяется числом электронов, отданных атому другого элемента или полученных от атома данного элемента.
| Элементы | Степень окисления, проявляемая в соединениях |
| Li, Na, К, Rb, Cs | + 1 |
| Be, Mg, Ca, Sr, Ba, Ra, Zn | +2 |
| Al | +3 |
| F | -1 |
Для определения степени окисления каждого элемента в соединениях используются нижеприведенные данные. В таблице даны элементы с постоянной степенью окисления в соединениях.
Степень окисления у других элементов бывает переменной.
Степень окисления водорода в его соединениях с металлами и кремнием равна 1 (например: ВН3, SiH4, NaH, CaH2 и др.), а во всех других соединениях+1.
Вот почему в периодической таблице водород записан как в подгруппе 1А, так и в подгруппе VIIA.
Степень окисления кислорода в пероксидах равна 1 (H2O2, Na2O2, CaO2 и др), в супероксидах 1 /2 (КО2), фтористых соединениях (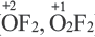
Углерод в своих соединениях проявляет степень окисления -4 ÷ +4.
Степень окисления азота в его соединениях с металлами (например, в нитридах Na3N, AIN, Ca3N2 и др.), аммиаке (NH3) равна -3, а в кислородсодержащих соединениях от +1 ÷ +5.
Степень окисления фосфора в его соединениях с металлами, фосфидах (Na3P, K3P, Ca3P2, AlP и др.), фосфине (PH3) равна -3, а в других соединениях +3 и +5 (P2S3, P2O3, P2O5, PCl5, HPO3, H3PO3, H3PO4 и др.).
Степень окисления серы в сульфидах равна -2 (H2S, Na2S, FeS, P2S3, P2S5, CS2, и др.), а в других соединениях -1 ÷ +6 .
Из галогенов хлор, бром и йод только в соединениях с металлами проявляют степень окисления 1, а в кислородсодержащих соединениях +l÷+-7.
Степень окисления элементов в простых веществах всегда равна нулю.
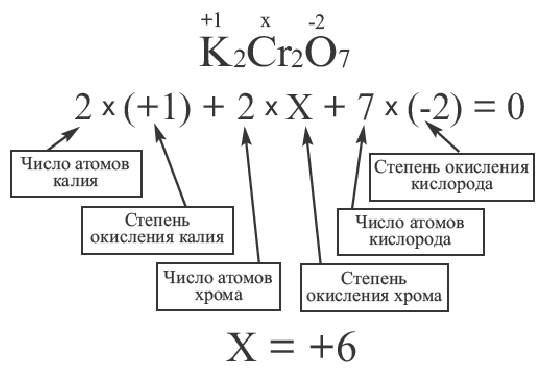
Алгебраическая сумма значений степени окисления элементов в сложных веществах всегда равна нулю. Следуя этому правилу, можно легко вычислить степень окисления любого химического элемента, если известны степень окисления других химических элементов в соединении. Неизвестная степень окисления элемента всегда принимается за х.
В сложных ионах алгебраическая сумма степеней окисления элементов равна заряду иона. Неизвестная степень окисления элемента в сложном ионе принимается за х. Записав в скобках формулу иона, за скобками (справа сверху) отмечают его заряд.
У большинства элементов самая высокая степень окисления соответствует номеру группы, в которой данный элемент размещается (кроме F, О, Fe, Си, Ag, Au). Самая низкая степень окисления любого неметалла (кроме H и В) определяется путем вычитания числа 8 от номера группы, где он расположен.
| Группа | VI | VII | V | IV |
| Элемент | S | Cl | N | C |
| Самая низкая степень окисления | 6 8=-2 | 7 8=-1 | 5 8=-3 | 4 8=-4 |
Металлы никогда не проявляют отрицательной степени окисления. Самая низкая степень окисления у них равна нулю.
В большинстве случаев степень окисления элемента по своему численному значению совпадает с его валентностью. Но такое бывает не всегда. Например: углерод трехвалентный только в угарном газе (СО), во всех остальных соединениях он четырехвалентный. Кислород трехвалентный только в ионе гидроксония (Н3О+) и угарном газе, во всех остальных соединениях он двухвалентный. В таких соединениях, как Аl4С3, CO2, CCl4, CF4, CS2, численные значения степени окисления и валентности у углерода совпадают.
При определении степени окисления посредством общего баланса отданных и полученных электронов ее среднее значение иногда может быть выражено дробным числом.
При разных степенях окисления атомов одного элемента в соединении степени окисления выражаются дробными числами. Среднее значение вычисляется способом электронного баланса.
Значение степени окисления, в отличие от заряда иона, проставляется над химическим знаком элемента (вначале ставится знак заряда, а затем число).
| Степень окисления | +2 Fe |
+3 Fe |
-2 S |
+6 S |
| Заряд иона | Fe2+ | Fe3+ | S2- | S6+ |
Пример №1
Сколько процентов от числа валентных электронов азота (7N 2s22p3) создают связь по механизму обмена?
Решение: В атоме азота из 5-ти валентных электронов 3 одиночные.
Значит, (3/5) ∙ 100%=60% участвуют в механизме обмена.
Каждая электронная пара, образующая химическую связь, обозначается по одной валентной линии, формулы молекул изображаются графически.
Пример №2
Определите отношения между а, b, с.
| Соли | Число донорно-акцепторных связен |
| (NH4)2SO4 | а |
| NH4Cl | b |
| (NH4)3PO4 | c |
Решение: Число донорноакцепторных связей в солях аммония равно числу ионов аммония.
Тогда: a=2; b=l; с=3
Ответ: b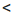
Пример №3
Определите количество а) полярных ковалентных и b) неполярных ковалентных связей в молекуле соединения:
Решение: Полярная ковалентная связь образуется между атомами двух разных неметаллов. В таком случае, в данном соединении N(пол.ков.связь) N(C Н)связь N(H) 6
А неполярная ковалентная связь образуется между атомами одного вида (в представленном соединении это линии между атомами углерода). Тогда N(κeпoл.ков.связь.) = 3
Ответ: а=6; b=3
Пример №4
Определите общее число орбиталей, участвующих в образовании химических связей в соединении Н3С CH2 СН3.
Решение: Кроме угарного газа (СО), во всех соединениях углерода все 4 орбитали внешнего электронного слоя участвуют в образовании связи. Поскольку атом H имеет 1 орбиталь, его орбиталь тоже участвует в образовании связи. В таком случае, общее число орбиталей, участвующих в образовании связи: N(оpб.)o6щ. N(C) • 4 + N(H) 3•4 + 8 20
Пример №5
Определите в данном соединении гибридное состояние углерода.
Решение:
- Химические реакции
- Теория электролитической диссоциации
- Электролиты и неэлектролиты в химии
- Металлы в химии
- Периодический закон Д. И. Менделеева
- Химические связи
- Ковалентная связь
- Валентность и степень окисления