 Вопросно-ответный конспект
Вопросно-ответный конспект
Алгоритм
1. Запишите название конспектируемого текста и его выходные данные.
2. Прочитайте текст, осмысливая его содержание.
3. Прочитайте текст второй раз, разбивая его на отрывки.
4. Выделите в каждом отрывке основную мысль.
5. Составьте вопрос к основной мысли для каждого отрывка.
6. Запишите точный ответ на каждый из вопросов.
Плановый конспект
Основой планового конспекта является план, каждому пункту которого соответствует определённая часть конспекта) текста.
Алгоритм
1. Запишите название конспектируемого текста и его выходные данные.
2. Прочитайте текст, осмысливая его основное содержание.
3. Составьте сложный план текста — основу конспекта.
4. Запишите своими словами основные положения и выводы, факты и доказательства, примеры и иллюстрации, соответствующие пунктам и подпунктам плана. (Обратите внимание! Если пункт плана не требует дополнительных пояснений, он не сопровождается текстом.)
5. Прочитайте ещё раз текст параграфа и проверьте полноту составленного конспекта.
6. Прочитайте конспект и при необходимости исправьте стилистические ошибки, расставьте знаки препинания.
7. Доработайте конспект, используя:
а) систему выделений в тексте (подчёркивание, отступы, пустые строки, рамки), сокращений, условных обозначений;
б) определённые цвета для выделения той или иной информации (формулы, даты, заголовки, цитаты и др.).
Обратите внимание!
Составляя конспект:
1) оставляйте большие поля для дополнений, за- меток, записи незнакомых терминов имён, требующих разъяснений;
2) соблюдайте правила цитирования (цитату заключайте в кавычки, давайте ссылку на источник с указанием страницы);
3) пишите компактно, чтобы на странице умещалось как можно больше текста;
4) избегайте излишнего цитирования, стремления сохранить стилистическую особенность текста.
Обзорный конспект
Обзорный конспект раскрывает конкретную тему с использованием нескольких источников.
Алгоритм
1. Запишите название конспекта.
2. Подберите и проанализируйте источники информации, содержащие материал по данной теме.
3. Составьте простой план по рассматриваемой теме, включающий все основные положения (ключевые понятия), которые она охватывает.
4. Составьте сложный план текста — основу конспекта, обобщая близкие по содержанию пункты простого плана.
5. Запишите своими словами основные положения и выводы, факты и доказательства, примеры и иллюстрации, соответствующие пунктам и подпунктам плана. (Обратите внимание! Если пункт плана не требует дополнительных пояснений, он не сопровождается текстом.)
6. Прочитайте конспект, проверяя полноту раскрытия темы.
7. Прочитайте конспект и при необходимости исправьте стилистические ошибки, расставьте знаки препинания.
8. Доработайте конспект, используя:
а) систему выделений (подчёркивание, отступы, пустые строки, рамки), сокращений, условных обозначений;
б) определённые цвета для выделения той или иной информации (формулы, даты, заголовки, цитаты и др.).
9. Составьте список литературы.
Текстуальный (цитатный) конспект
Текстуальный конспект построен из высказываний автора, изложенных им фактов.
Алгоритм
1. Запишите название конспектируемого текста и его выходные данные.
2. Прочитайте текст и отметьте в нём основное содержание, главные мысли.
3. Выделите те цитаты, которые войдут в конспект.
4. Выпишите цитаты, используя правила их сокращения (можно использовать разные формы записи).
Хронологический конспект
Хронологический конспект отражает хронологическую последовательность событий на фоне показа самих событий.
Алгоритм
1. Запишите название конспектируемого текста и его выходные данные.
2. Прочитайте текст, осмысливая его содержание.
3. Прочитайте текст второй раз, разбивая его на отрывки, в которых описываются определённые временные интервалы.
4. Выделите в каждом отрывке основное событие и кратко охарактеризуйте его.
5. Сформулируйте итоговый вывод о развитии событий в течение определённого времени.
6. Прочитайте конспект, проверяя полноту раскрытия темы.
Обновлено: 09.01.2023
Персональный сайт учителя химии Сазонова В.В.
Вопросно-ответный конспект
Алгоритм
1. Запишите название конспектируемого текста и его выходные данные.
2. Прочитайте текст, осмысливая его содержание.
3. Прочитайте текст второй раз, разбивая его на отрывки.
4. Выделите в каждом отрывке основную мысль.
5. Составьте вопрос к основной мысли для каждого отрывка.
6. Запишите точный ответ на каждый из вопросов.
Плановый конспект
Основой планового конспекта является план, каждому пункту которого соответствует определённая часть конспекта) текста.
Алгоритм
1. Запишите название конспектируемого текста и его выходные данные.
2. Прочитайте текст, осмысливая его основное содержание.
3. Составьте сложный план текста — основу конспекта.
4. Запишите своими словами основные положения и выводы, факты и доказательства, примеры и иллюстрации, соответствующие пунктам и подпунктам плана. ( Обратите внимание! Если пункт плана не требует дополнительных пояснений, он не сопровождается текстом.)
5. Прочитайте ещё раз текст параграфа и проверьте полноту составленного конспекта.
6. Прочитайте конспект и при необходимости исправьте стилистические ошибки, расставьте знаки препинания.
7. Доработайте конспект, используя:
а) систему выделений в тексте (подчёркивание, отступы, пустые строки, рамки), сокращений, условных обозначений;
б) определённые цвета для выделения той или иной информации (формулы, даты, заголовки, цитаты и др.).
1) оставляйте большие поля для дополнений, за- меток, записи незнакомых терминов имён, требующих разъяснений;
2) соблюдайте правила цитирования (цитату заключайте в кавычки, давайте ссылку на источник с указанием страницы);
3) пишите компактно, чтобы на странице умещалось как можно больше текста;
4) избегайте излишнего цитирования, стремления сохранить стилистическую особенность текста.
Обзорный конспект
Обзорный конспект раскрывает конкретную тему с использованием нескольких источников.
Алгоритм
1. Запишите название конспекта.
2. Подберите и проанализируйте источники информации, содержащие материал по данной теме.
3. Составьте простой план по рассматриваемой теме, включающий все основные положения (ключевые понятия), которые она охватывает.
4. Составьте сложный план текста — основу конспекта, обобщая близкие по содержанию пункты простого плана.
5. Запишите своими словами основные положения и выводы, факты и доказательства, примеры и иллюстрации, соответствующие пунктам и подпунктам плана. (Обратите внимание! Если пункт плана не требует дополнительных пояснений, он не сопровождается текстом.)
6. Прочитайте конспект, проверяя полноту раскрытия темы.
7. Прочитайте конспект и при необходимости исправьте стилистические ошибки, расставьте знаки препинания.
8. Доработайте конспект, используя:
а) систему выделений (подчёркивание, отступы, пустые строки, рамки), сокращений, условных обозначений;
б) определённые цвета для выделения той или иной информации (формулы, даты, заголовки, цитаты и др.).
9. Составьте список литературы.
Текстуальный (цитатный) конспект
Текстуальный конспект построен из высказываний автора, изложенных им фактов.
Алгоритм
1. Запишите название конспектируемого текста и его выходные данные.
2. Прочитайте текст и отметьте в нём основное содержание, главные мысли.
3. Выделите те цитаты, которые войдут в конспект.
4. Выпишите цитаты, используя правила их сокращения (можно использовать разные формы записи).
Хронологический конспект
Хронологический конспект отражает хронологическую последовательность событий на фоне показа самих событий.
Алгоритм
1. Запишите название конспектируемого текста и его выходные данные.
2. Прочитайте текст, осмысливая его содержание.
3. Прочитайте текст второй раз, разбивая его на отрывки, в которых описываются определённые временные интервалы.
4. Выделите в каждом отрывке основное событие и кратко охарактеризуйте его.
5. Сформулируйте итоговый вывод о развитии событий в течение определённого времени.
Конспекты по химии 8 класс собраны по порядку на этой странице. Они помогут вам наглядно показать учебный материал на своих уроках, а ученик с их помощью сможет самостоятельно изучить любую тему урока по видео или конспекту. Это готовые материалы для учителя химии, которые можно удобно использовать на каждом своем уроке.
1. Предмет химии. вещества
Химия 8 класс
2. Роль химии в нашей жизни
Химия 8 класс
3. Знаки химических элементов
Химия 8 класс
4. Химическая формула. Относителная атомная и молекулярная масса
Химия 8 класс
5. Основные сведения о строении атома. состав атомных ядер
Химия 8 класс
6. Порядковый номер элемента. Изотопы
Химия 8 класс
7. Структура периодической таблицы элементов
Химия 8 класс
8. Строение электронных оболочек атома
Химия 8 класс
9. Ионная связь
Химия 8 класс
10. Ковалентная неполярная связь
Химия 8 класс
Получайте новое первыми
Лицензия на право ведения образовательной деятельности №5251 от 25.08.2017 г.
Химия – это наука о веществах, их свойствах, превращениях веществ и явлениях, сопровождающих эти превращения.
Химия 8 класс
Первоначальные химические понятия. Кислород. Горение. Водород. Вода. Растворы. Количественные отношения в химии. Важнейшие классы неорганических соединений. Периодический закон и строение атома. Строение вещества. Химическая связь.
Химия 9 класс
Электролитическая диссоциация. Кислород и сера. Азот и фосфор. Углерод и кремний. Общие свойства металлов. Металлы IA—IIIA-групп периодической таблицы химических элементов. Железо. Металлургия. Краткий обзор важнейших органических веществ (Углеводороды, производные углеводородов).
Справочники для ОГЭ
Специальные конспекты по химии, в которых в сжатой форме повторяются основные школьные темы, для экспресс-подготовки к Основному Государственному Экзамену по химии.
Химия 10 класс
Химия 11 класс
Справочники для ЕГЭ
Специальные конспекты по химии, в которых в сжатой форме повторяются основные школьные темы, для экспресс-подготовки к Единому Государственному Экзамену по химии.
Решения задач по химии
Источники идей и источники цитат для конспектов по Химии:
(с) Цитаты из вышеуказанных учебных пособий использованы на сайте в незначительных объемах, исключительно в учебных и информационных целях (пп. 1 п. 1 ст. 1274 ГК РФ).
Выберите удобный метод и повысьте эффективность занятий.
Для чего нужен конспект? Конспектирование — отличная возможность систематизировать знания и запомнить самую важную информацию на уроке, вебинаре или при подготовке доклада. В этой статье мы поговорим о том, как составлять конспекты, используя различные методы.
Что такое конспект
Конспектирование — это процесс осмысленной переработки текста, аудио- и видеоматериала с целью улучшить запоминание информации. Написание конспекта позволяет выделить смысловые части, зафиксировать ключевые идеи, выявить закономерности и систематизировать информацию. Конспекты составляются в виде тезисов, выписок, вопросов, в сжатом виде отражающих и уточняющих необходимую информацию.
Виды конспектов
Ведение конспектов существенно облегчает усвоение учебного материала. Выделяют несколько видов конспектов:
- Плановый конспект строится на основе плана, информация в конспекте раскрывает каждый его пункт.
- Конспект-схема помогает за счёт схем сформировать логические связи.
- Текстуальный конспект состоит из цитат, логически связанных между собой.
- Свободный конспект содержит выписки, тезисы, цитаты.
- Тематический конспект раскрывает определённую тему, например, отражает хронологию событий.
Методы конспектирования
Существует несколько методов конспектирования, которые подразумевают под собой способы записи конспектов. Остановимся подробнее на самых популярных и эффективных методах конспектирования.
Метод Корнелла
В середине прошлого века профессор Корнелльского университета Вальтер Паук разработал метод конспектирования, ставший впоследствии суперпопулярным у студентов. Он так и называется — метод Корнелла.
Когда полезен
Для обработки больших объёмов информации, например, на продолжительных и информативных вебинарах.
Предметы
- история,
- обществознание,
- литература,
- русский язык,
- биология,
- химия,
- география.
Как использовать этот метод конспектирования:
- Возьмите лист А4 или обычный тетрадный лист. Проведите две горизонтальные линии: одну вверху (там будет дата и заголовок), вторую — внизу, чтобы под ней можно было записать 5-6 предложений, суммирующих содержание конспекта на этой странице.
- Затем проведите вертикальную линию и разделите середину листа на две части. Правая колонка должна быть в два раза шире левой.
- Во время вебинара в правую широкую колонку нужно записывать основные сведения, которые сообщает учитель. Между предложениями лучше оставлять немного пустого пространства, чтобы была возможность в них ещё что-то дописать. После занятия в левую колонку перенесите всю самую важную информацию: правила, формулы, даты, имена.
- В течение суток после урока заполните нижнее поле, там нужно записать краткое резюме всей лекции.
Метод боксов
Этот метод составления конспектов схож с предыдущими, но суть в том, чтобы заключать каждый блок темы в небольшие квадраты. Так проще воспринимать информацию, поскольку фокусируешься только на выделенном аспекте темы. Факты не путаются между собой, их легче запомнить.
Когда полезен:
- при изучении иностранных слов, дат, биографий исторических личностей;
- для сопоставления нескольких понятий.
Предметы:
- история,
- обществознание,
- литература,
- русский язык,
- английский язык.
Как использовать:
Метод нумерации
Суть этого вида конспектирования заключается в том, чтобы присваивать порядковый номер каждой записываемой мысли. При этом тренируется лаконичность и чёткость мышления, а в конспекте потом легко ориентироваться.
Когда полезен метод
Для записывания длинных лекций, особенно если преподаватель порой перескакивает с одной мысли на другую.
Предметы:
- история,
- обществознание,
- литература,
- русский язык,
- английский язык,
- химия,
- биология,
- география,
- геометрия,
- физика.
Как использовать:
Метод таблиц
Таблицы — это очень наглядно. Их можно использовать не только на истории, но и на других уроках.
Когда полезен:
- при рассмотрении тем с одинаковыми критериями,
- при конспектировании большого количества фактов,
- чтобы свести несколько элементов в одну систему,
- чтобы разобраться в плюсах и минусах чего-либо.
Предметы:
- история,
- обществознание,
- литература,
- русский язык,
- английский язык,
- биология,
- география.
Как использовать этот метод написания конспекта:
- Возьмите тетрадный лист или лист А4 и, расположив его горизонтально, начертите нужное количество столбцов. При вертикальном расположении листа колонки могут получиться слишком узкими, будет неудобно писать.
- Изучая те или иные темы, вносите данные в соответствующие столбцы.
- Когда таблица будет готова, отложите конспект на несколько часов, а потом вновь обзорно взгляните на него. Сравните факты и понятия, отметьте сходства и различия, плюсы и минусы, проанализируйте связи.
Метод индексов
Стрелочки, рамки, схемы, таблицы, графики, рисунки и прочие визуальные средства — прекрасные помощники в понимании связей и запоминании ключевых понятий. Используйте их при оформлении конспектов.
Можно вкраплять их в текст или ставить на полях для привлечения внимания. Например, если преподаватель продиктовал незнакомое понятие и не дал определение, можно поставить рядом яркий значок, чтобы потом разобраться с новым термином.
Когда полезен
Когда нужно записывать быстро, но при этом структурировать информацию.
Предметы:
- история,
- обществознание,
- литература,
- русский язык,
- английский язык,
- химия,
- биология,
- география,
- геометрия,
- физика,
- информатика.
Как конспектировать методом индексов:
Метод ментальных карт
Карта мыслей, на первый взгляд, кажется гораздо сложнее и запутаннее обычного конспекта. В ней ключевая идея находится в центре, а от неё тянутся ветки мыслей и объяснений. Но на самом деле она намного эффективнее: во время составления и отрисовки ментальной карты вы пропускаете информацию через себя и лучше её запоминаете.
Когда полезен:
- для разбора больших сложных тем,
- для анализа литературных произведений,
- при написании эссе,
- в подготовке докладов.
Предметы:
- история,
- обществознание,
- литература,
- русский язык,
- английский язык,
- биология,
- география.
Как использовать этот метод ведения конспектов:
- В центре карты напишите главную мысль. От неё проведите несколько линий и отметьте все ключевые идеи, относящиеся к теме. На эти ветки добавляйте новые пункты, раскрывающие предыдущие, и так далее.
- Пишите кратко и старайтесь не расширять карту дальше четвёртого уровня. Объединяйте темы из разных веток, добавляйте заметки и идеи. Делайте всё, чтобы не только удобно расположить мысли на карте, но и заставить её работать на вас.
Инструкции по составлению карты мыслей у нас посвящена отдельная статья. Обязательно прочтите и используйте этот эффективный метод создания конспектов!
Надеемся, что наша статья была для вас полезна, и вы поняли основные правила конспектирования. Использование конспектов существенно облегчит ваше обучение и поможет лучше запоминать материал по разным предметам. Теперь вы знаете, как правильно писать конспекты, и сможете успешно применять в учёбе самые эффективные методы конспектирования.
Записали!
Скоро с вами свяжется консультант, расскажет об обучении в нашей онлайн-школе.
Проверьте вашу электронную почту — там письмо о том, что стоит сделать перед консультацией.
Записали!
Скоро с вами свяжется консультант, расскажет об обучении в нашей онлайн-школе.
Проверьте вашу электронную почту — там письмо о том, что стоит сделать перед консультацией.
Записали!
Скоро с вами свяжется консультант, расскажет об обучении в нашей онлайн-школе.
Проверьте вашу электронную почту — там письмо о том, что стоит сделать перед консультацией.
У нас вы сможете учиться в удобном темпе, делать упор на любимые предметы и общаться со сверстниками по всему миру.
Простейшие понятия: вещество, молекула, атом, химический элемент
Что такое химия? Где мы встречаемся с химическими явлениями? Везде. Сама жизнь — это бесчисленное множество разнообразных химических реакций, благодаря которым мы дышим, видим голубое небо, ощущаем изумительный запах цветов…
Что изучает химия? Химия изучает вещества, а также химические процессы, в которых участвуют эти вещества.
Что такое вещество — понятно: это то, из чего состоит окружающий нас мир и мы сами. Но что такое химический процесс (явление)?
К химическим явлениям относятся процессы, в результате которых изменяется состав или строение молекул, образующих данное вещество. Изменились молекулы — изменилось вещество (оно стало другим!), — изменились его свойства:
- свежее молоко стало кислым;
- зелёные листья стали жёлтыми;
- сырое мясо при обжаривании изменило запах.
Все эти изменения — следствие сложных и многообразных химических процессов. Итак,
химия — это наука о веществах и их превращениях.
При этом исследуются не всякие превращения, а только такие, при которых
- обязательно изменяется состав или строение молекул;
- никогда не изменяется состав и заряд ядер атомов.
Вещество — это то, из чего состоят окружающие нас предметы. Каждому абсолютно чистому веществу (таких в природе, кстати, не существует) приписывают определённую химическую формулу, которая отражает его состав, например:
Наименьшая частица вещества, которая отражает его качественный и количественный состав, называется молекулой.
Молекулы состоят из атомов. Атомы в молекуле соединены при помощи химических связей. Каждый атом обозначается при помощи символа (химического знака):
Число атомов в молекуле обозначают при помощи индекса:
- О2 — это молекула вещества кислорода, состоящая из двух атомов кислорода;
- Н2О — это молекула вещества воды, состоящая из двух атомов водорода и одного атома кислорода.
Но! Если атомы не связаны химической связью, то их число обозначают при помощи коэффициента:
Аналогично изображают число молекул:
- 2Н2 — две молекулы водорода;
- 3Н2О — три молекулы воды.
Почему атомы водорода и кислорода имеют разное название, разный символ? Потому что это атомы разных химических элементов.
Химический элемент — это частицы с одинаковым зарядом ядер их атомов.
Что такое ядро атома? Почему заряд ядра является признаком принадлежности атома к данному химическому элементу? Чтобы ответить на эти вопросы, следует уточнить: изменяются ли атомы в химических реакциях? Из чего состоит атом*?
* Подробнее о строении атома будет рассказано в уроке 3.
Атом не имеет заряда, хотя и состоит из положительно заряженного ядра и отрицательно заряженных электронов:
В ходе химических реакций число электронов любого атома может изменяться, но заряд ядра атома в химических реакциях НЕ МЕНЯЕТСЯ!
Каждому химическому элементу присвоен химический символ (знак), порядковый номер в таблице Менделеева (порядковый номер равен заряду ядра атома); определённое название и, для некоторых химических элементов, особое прочтение символа в химической формуле (табл. 1).
Подведём итог. Вещества состоят из молекул, молекулы состоят из атомов, атомы с одинаковым зарядом ядра относятся к одному и тому же химическому элементу.
Но, если вещество состоит из молекул, то любое изменение состава или строения молекулы приводит к изменению самого вещества, его свойств.
Вопрос. Чем отличаются химические формулы веществ: Н2О и Н2О2?
Хотя по составу молекулы этих веществ отличаются на один атом кислорода, сами вещества по свойствам сильно отличаются друг от друга. Воду Н2О мы пьём и жить без неё не можем, а Н2О2 — перекись водорода, пить нельзя, а в быту её используют для обесцвечивания волос.
Вопрос. А чем отличаются химические формулы веществ:
Состав этих веществ — аллозы (А) и глюкозы (Б) — одинаков — С6Н12О6. Отличаются они строением молекул, в данном случае — расположением групп ОН в пространстве. Глюкоза — универсальный источник энергии для большинства живых организмов, а аллоза практически не встречается в природе и не может быть источником энергии.
Простые и сложные вещества. Валентность
Вещества бывают простые и сложные. Если молекула состоит из атомов одного химического элемента, — это простое вещество:
- Алмаз — атомы углерода находятся в вершинах воображаемых тетраэдров;
- Графит — атомы углерода находятся в одной плоскости;
Молекулы сложных веществ состоят из атомов разных химических элементов:
Как известно, в состав сложных веществ входят атомы разных химических элементов. Эти атомы соединяются между собой химическими связями: ковалентными, ионными, металлическими.
Валентность атомов некоторых химических элементов постоянна (табл. 2).
Для других атомов валентность можно определить (вычислить) из химической формулы вещества.
Строго говоря, по нижеизложенным правилам определяют не валентность, а степень окисления (см. урок 7). Но поскольку в некоторых соединениях числовые значения этих понятий совпадают, то иногда по формуле можно определять и валентность.
При этом следует учитывать изложенное выше правило о химической связи.
Сделаем практические выводы.
1. Если один из атомов в молекуле одновалентен, то валентность второго атома равна числу атомов первого элемента (см. на индекс!):
2. Если число атомов в молекуле одинаково, то валентность первого атома равна валентности второго атома:
3. Если у одного из атомов индекс отсутствует, то его валентность равна произведению валентности второго атома на его индекс:
Задание 1.2. Определите валентности элементов в соединениях:
Вначале укажите валентности атомов, у которых она постоянна! Аналогично определяется валентность атомных групп (ОН), (РО4), (SО4) и так далее.
Задание 1.3. Определите валентности атомных групп (в формулах выделены курсивом):
Обратите внимание! Одинаковые группы атомов (OH), (РО4), (SO4) имеют одинаковые валентности во всех соединениях.
Зная валентности атома или группы атомов можно составить формулу соединения. Для этого пользуются правилами:
- Если валентности одинаковы, то и число атомов одинаково, т. е. индексы не ставим:
- Если валентности кратны (одно число делится на другое), то число атомов элемента с меньшей валентностью определяем делением:
Задание 1.4. Составьте химические формулы соединений:
Уравнения химических реакций
Вещества, состав которых отражают химические формулы, могут участвовать в химических процессах (реакциях). Графическая запись, соответствующая данной химической реакции, называется уравнением химической реакции. Например, при сгорании (взаимодействии с кислородом) угля происходит химическая реакция:
Выполняя этот закон, необходимо в уравнениях химических реакций расставлять коэффициенты так, чтобы число атомов каждого химического элемента не изменялось в результате реакции. Например, при разложении бертолетовой соли КClO3, получается соль КСl и кислород О2:
Число атомов калия и хлора одинаково, а кислорода — разное. Уравняем их:
Теперь изменилось число атомов калия и хлора до реакции. Уравняем их:
Теперь между правой и левой частями уравнения можно поставить знак равенства:
Полученная запись показывает, что при разложении двух молекул КClO3 получается две молекулы КСl и три молекулы кислорода O2. Число молекул показывают при помощи коэффициентов.
При подборе коэффициентов необязательно считать отдельные атомы. Если в ходе реакции не изменился состав некоторых атомных групп, то можно учитывать число этих групп, считая их единым целым:
Последовательность действий такова:
1. Определим валентность исходных атомов и группы PO4:
2. Перенесём эти числа в правую часть уравнения:
3. Составим химические формулы полученных веществ по валентностям составных частей:
5. Число атомов натрия и хлора до реакции теперь стало равным шести; доставим соответствующий коэффициент:
Эти правила образуют Алгоритм составления уравнений химических реакций обмена, так как, пользуясь этой последовательностью, можно уравнять схемы многих химических реакций, за исключением более сложных окислительно-восстановительных реакций (см. урок 7).
Химические реакции бывают разных типов. Основными являются:
1. Реакции соединения:
Здесь из двух и более веществ образуется одно вещество:
2. Реакции разложения:
Здесь из одного вещества получаются два вещества и более веществ:
3. Реакции замещения:
Здесь реагируют простое и сложное вещества, образуются также простое и сложное вещества, причём простое вещество замещает часть атомов сложного вещества:
4. Реакции обмена:
Здесь реагируют два сложных вещества и получаются два сложных вещества. В ходе реакции сложные вещества обмениваются своими составными частями:
Существуют и другие типы химических реакций.
Задание 1.5. Расставьте коэффициенты в предложенных выше примерах.
Задание 1.6. Расставьте коэффициенты и определите тип химической реакции:
Выводы
Вещества бывают простые и сложные. Состав веществ показывают при помощи химических формул. Формулы веществ составляют, учитывая валентности составных частей этих веществ. Запись химического процесса при помощи формул называется уравнением химической реакции. Химические реакции бывают разных типов: обмена, замещения, разложения, соединения и другие.
Читайте также:
- Кубический сантиметр и измерение объема 4 класс пнш конспект
- В с высоцкий песня о волге конспект урока
- План конспект урока географическая карта 3 класс
- Конспект занятия по развитию речи в старшей группе на тему профессии родителей
- Spotlight 9 illusions конспект урока
Конспекты по предмету «ХИМИЯ»
Изучение Химии шаг за шагом. Онлайн-учебник и сборник задач.
Химия – это наука о веществах, их свойствах, превращениях веществ и явлениях, сопровождающих эти превращения.
Конспекты по кодификатору ОГЭ
Конспекты по кодификатору ЕГЭ
Химия 8 класс
Первоначальные химические понятия. Кислород. Горение. Водород. Вода. Растворы. Количественные отношения в химии. Важнейшие классы неорганических соединений. Периодический закон и строение атома. Строение вещества. Химическая связь.
- Вещества и их свойства. Чистые вещества и смеси
- Физические и химические явления
- Атомы, молекулы и ионы
- Простые и сложные вещества
- Химические элементы и их знаки
- Относительная атомная масса
- Закон постоянства состава веществ
- Химическая формула. Индекс. Коэффициент
- Массовая доля элемента в соединении
- Химия 8 класс Все формулы и определения
- Оксиды (названия, классификация, получение)
- Свойства оксидов
- Основания (названия, получение, свойства)
- Строение атома. Массовое число
- Строение электронных оболочек атомов
- Периодическая система химических элементов
- Закономерности изменения свойств элементов
- Строение веществ. Электроотрицательность
- Химическая связь: ковалентная, ионная, металлическая
- Валентность химических элементов
- Определение валентности + примеры
- Кислород: характеристика, свойства, получение
- Кислоты: классификация, свойства, получение
- Соли: классификация, свойства, получение
- Амфотерные оксиды и гидроксиды
- Водород: характеристика, получение
- Химические свойства водорода. Применение
- Вода. Свойства воды. Водные растворы
Химия 8 класс. Контрольные (УМК Габриелян)
Проверить знания за 8 класс (онлайн-тесты)
Химия 9 класс
Электролитическая диссоциация. Кислород и сера. Азот и фосфор. Углерод и кремний. Общие свойства металлов. Металлы IA—IIIA-групп периодической таблицы химических элементов. Железо. Металлургия. Краткий обзор важнейших органических веществ (Углеводороды, производные углеводородов).
Химия 9 класс. Контрольные (УМК Рудзитис)
Справочники для ОГЭ
Специальные конспекты по химии, в которых в сжатой форме повторяются основные школьные темы, для экспресс-подготовки к Основному Государственному Экзамену по химии.
Химия 10 класс
Химия 10 класс. Контрольные (УМК Габриелян)
Химия 11 класс
Справочники для ЕГЭ
Специальные конспекты по химии, в которых в сжатой форме повторяются основные школьные темы, для экспресс-подготовки к Единому Государственному Экзамену по химии.
Решения задач по химии
Конспекты по кодификатору ОГЭ
Конспекты по кодификатору ЕГЭ
Источники идей и источники цитат для конспектов по Химии:
- Учебник по химии для 8 класса / Г. Е. Рудзитис, Ф. Г. Фельдман. — М. : Просвещение.
- Учебник по химии для 9 класса / Г. Е. Рудзитис, Ф. Г. Фельдман. — М. : Просвещение.
- Ковалевская Н.Б. ХИМИЯ в таблицах и схемах. 8 класс. Для самостоятельной работы в школе и дома — М.: «Издат-Школа XXI век», 2004.
- ОГЭ. Универсальный справочник по химии / Е.Ю. Шапаренко. — Москва : Эксмо.
- Задачи по химии и способы их решения. 8—9 кл. / О. С. Габриелян, П. В. Решетов, И. Г. Остроумов. — М.: Дрофа.
- Сборник задач и упражнений по химии: Школьный курс / В. В. Еремин, Н. Е. Кузьменко. — М.: ООО «Издательский дом «ОНИКС 21 век»: ООО «Издательство «Мир и Образование», 2005
- Справочник по химии: 8-9 классы. ФГОС / А.Д. Микитюк — М.: Издательство «Экзамен», 2019
- ЕГЭ. Химия: алгоритмы выполнения типовых заданий / Е.В. Крышилович, В.А. Мостовых — М.: Эксмо, 2018
- Химия. Самоучитель. Книга для тех, кто хочет сдать экзамены, а также понять и полюбить химию / Е. Н. Френкель. — Москва : Издательство АСТ, 2017
(с) Цитаты из вышеуказанных учебных пособий использованы на сайте в незначительных объемах, исключительно в учебных и информационных целях (пп. 1 п. 1 ст. 1274 ГК РФ).
ИГРА–ПУТЕШЕСТВИЕ · 8 КЛАСС
Цель урока. Повторить классификацию веществ, типы химических реакций и признаки их классификации; научить учащихся применять полученные знания о типах химических реакций на практике – составлять уравнения химических реакций, определять типы химических реакций.
Задачи.
Образовательные: систематизировать знания учащихся о классификации веществ, типах химических реакций; продолжить формирование умений наблюдать, записывать уравнения и предвидеть продукты химических реакций; продолжить формирование умения при написании реакций обмена, применения условий течения реакций между растворами до конца; подготовить учащихся к пониманию обратимых и необратимых реакций, теории электролитической диссоциации.
Развивающие: совершенствовать умения школьников при составлении химических уравнений, при выполнении лабораторных опытов; совершенствовать умения учащихся сравнивать и обобщать; развивать память, устойчивое внимание, самостоятельное мышление, умение слушать и слышать другого человека; развивать аналитическое мышление.
Воспитательные: продолжить формирование диалектико-материалистического мышления учащихся.
Форма учебного процесса: классный урок.
Тип урока: урок обобщения и систематизации знаний учащихся.
Вид урока: урок игра-путешествие.
Система оценивания. На каждом этапе учащимся, выполняющим задания у доски, а также активно работающим на своих местах, выдаются аурики (от лат. aurum – золото) – показатель работоспособности и активности учащихся на уроке, которые ребята подклеивают в свои «Наградные листы». К концу урока у учащихся накапливается определенное количество ауриков, по которым легко оценивать их работу на уроке: 3 аурика – оценка «5», 2 аурика – «4», 1 аурик – «3».
Оборудование и реактивы. Штатив с пробирками, таблица «Угадай слово», шифровки, специальное оформление маршрута путешествия (изображение горы, цветочная поляна, снежное облако), карточки с заданиями, лист ватмана для суперигры «Крестики-нолики», аурики;
на столах учащихся: схема-конспект урока с заданиями, условные знаки поездов (красный кружок и зеленый треугольник); наградные листы, анкеты для учащихся; разбавленные растворы серной кислоты, хлорида магния, карбоната натрия, гидроксида натрия, фенолфталеин.
ХОД УРОКА
I. Организационный момент
Приветствие.
II. Сообщение темы, цели урока, мотивация учащихся
Учитель.
Эти явления знаете вы,
В природе и в быту встречаются они,
А отличают эти явления взаимные превращения,
При которых образуются всегда новые вещества.
Что же это за явления?
Ученики. Химические реакции.
Учитель. Тема нашего урока «Типы химических реакций». Сегодня на уроке мы должны систематизировать все полученные вами знания о химических реакциях, их типах и условиях протекания, для того чтобы в дальнейшем вы могли правильно описывать химические свойства веществ, а также предсказывать возможности их получения, ведь нас с вами окружают вещества и постоянно происходящие с ними изменения. Кроме того, хорошо овладев этой темой, вы без труда сможете осуществлять цепочки химических превращений, решать всевозможные химические задачи. А для этого мы с вами совершим восхождение к вершине горы.
На горе вас ждет сюрприз,
Там еще и суперприз!
Чтобы гору перейти и к вершине нам дойти,
Нужно многое постичь, надо много сил вложить:
Не бояться отвечать и вопросы задавать,
Уравнения химических реакций писать,
Знать, как их отличать,
Все задания выполнять, друг у друга проверять.
Цель свою тогда достигнем –
О типах реакций все постигнем!
Девиз нашего урока – «Достичь вершины – не свалиться в пропасть!».
Итак, в путь! Желаю удачи! У каждого из вас на столе лежит наградной лист. По пути к вершине «химической горы» я вам буду давать аурики – показатель вашей активности. А вы эти аурики будете приклеивать в свои наградные листы (см. приложение).
Чтобы достичь цели, т.е. добраться до вершины горы, мы должны преодолеть 5 этапов:
1) «Шифровка»;
2) «Угадай слово»;
3) «Письмо»;
4) «Химический букет»;
5) «Химический снегопад».
III. Актуализация знаний, умений, навыков учащихся
Учитель. Прежде чем мы начнем путешествие по горам, нам надо добраться до их подножия. Предлагаю вам воспользоваться услугами химической железной дороги. В вашем распоряжении два вида поездов: скорый поезд (красный кружок); пассажирский поезд (зеленый треугольник). Ребята, какой из них быстрее?
Ученики. Скорый поезд.
Учитель. В зависимости от уверенности в своих знаниях по изученным ранее темам, вы должны сейчас выбрать удобный для себя поезд. Посмотрите внимательно задания, написанные в схеме-конспекте нашего урока, и сделайте свой выбор. На столах у вас лежат условные знаки поездов, прошу поднять знак выбранного вами вида поезда. Фигуры не опускайте, т.к. я должен выбрать машинистов и дать им «руль» управления. Они будут выполнять задание у доски. Все остальные также должны выполнить задания на своих рабочих местах. Напоминаю, эти задания находятся в схеме-конспекте нашего урока.
Учитель выбирает двух «машинистов» и приглашает их к доске.
Звучит фонограмма: «Из средней общеобразовательной школы № 20 отправляются скорый и пассажирский поезда до станции «Химические горы». Будьте внимательны и осторожны!».
Учитель. Можем ехать, т.е. выполнять задания.
Задание для пассажирского поезда. Запишите формулы веществ в соответствующие столбцы таблицы: H2, Na2S, Al, CuCl2, Mg, KI, S, Ca(OH) 2, O3, FeBr3 (табл. 1).
Таблица 1
|
Простые вещества |
Сложные вещества |
|
………………….. |
………………….. |
|
………………….. |
………………….. |
|
………………….. |
………………….. |
|
………………….. |
………………….. |
|
………………….. |
………………….. |
Задание для скорого поезда. Запишите формулы веществ в соответствующие столбцы таблицы: P2O5, I2, HNO3, Ca(OH)2, Na2O, K2SO4, Fe, H3PO4, N2, Na2SiO3, LiOH, Cu (табл. 2).
Таблица 2
|
Простые вещества |
Сложные вещества |
||||
|
металлы |
неметаллы |
оксиды |
основания |
кислоты |
соли |
|
……… |
……… |
……… |
……… |
……… |
……… |
Проверка выполненных заданий осуществляется с использованием сигнальных карточек. За выполнение задания для пассажирского поезда – 2 аурика, скорого – 3 аурика.
Учитель. Ребята, давайте подведем итог нашей поездки и скажем, чем отличаются простые вещества от сложных, физические явления от химических.
Учащиеся отвечают на вопросы.
Учитель. Мы прибыли к подножию «химической горы». А теперь, вперед – в горы! Прохождение каждого этапа маршрута я буду отмечать звездочкой.
IV. Обобщение и систематизация понятий
1-й э т а п «Шифровка»
Учитель. Поскольку мы только начинаем выполнять восхождение в горы, то этот этап пройдем парами. На каждой парте лежит шифровка (см. шифровки 1–3). Посмотрите на нее внимательно.
Задание. В левой части листа записаны уравнения химических реакций, в правой – беспорядочно расставлены точки с цифрами; каждой цифре соответствует сумма коэффициентов в написанных в левом столбце уравнениях реакций. Ваша задача: расшифровать замаскированный химический элемент. Для этого необходимо по порядку уравнивать химические реакции, подсчитывать сумму коэффициентов в уравнении, находить соответствующие точки и последовательно с помощью маркеров соединять их друг с другом. Если вы правильно выполните задание, то узнаете, какой химический элемент спрятался за цифрами.
Ответ. Шифровки 1 – N; 2 – P; 3 – O.
За правильное выполнение задания выдаются аурики.
Учитель. Итак, 1-й этап позади, отмечаем звездочкой.
2-й э т а п «Угадай слово»
Учитель.
Химических реакций известно в мире много,
И каждая в отдельности важна, поверьте мне.
Реакции мы делим на типы очень строго.
Какие это типы? Поведайте вы мне.
Ученики. Существует четыре типа химических реакций: реакции соединения, разложения, замещения, обмена.
Учитель. Что называется реакцией соединения, разложения, замещения, обмена?
Ученики отвечают на поставленные вопросы.
Учитель. Давайте выполним следующее задание.
Задание. К какому типу химических реакций нужно отнести уравнения, приведенные в таблице «Угадай слово»? Необходимо правильно определить тип химической реакции, найти соответствующую букву, из букв сложить слово (табл. 3).
Таблица 3
«Угадай слово»
|
Уравнения реакций |
Типы химических реакций |
|||
|
соединения |
разложения |
замещения |
обмена |
|
|
Mg + 2HCl = MgCl2 + H2 |
Б |
В |
П |
З |
|
2Fe(OH) 3 = Fe2O3 + 3H2O |
Г |
И |
К |
Д |
|
2Ca + O2 = 2CaO |
С |
Ж |
С |
Ф |
|
K3PO4 + 3AgNO3 = Ag3PO4 + 3KNO3 |
Н |
У |
Т |
Ь |
|
2HgO = 2Hg + O2 |
А |
М |
Р |
П |
|
Br2 + 2KI = 2KBr + I2 |
Ш |
Л |
О |
И |
Один человек работает у доски, остальные на своих местах.
Учитель. Ребята, у кого получилось слово «Письмо», поднимите сигнальные карточки – зеленые треугольники – вверх.
Друзья, вы правильно определили типы химических реакций, и мы получили название 3-го этапа нашего путешествия. А 2-й этап мы преодолели.
Учитель прикрепляет звездочку.
3-й э т а п «Письмо»
Учитель. Ребята, пока мы преодолевали этапы, нам по химической почте пришло видеописьмо. Давайте узнаем, что в нем.
Это письмо от одного из персонажей пьесы Н.В. Гоголя «Ревизор», от Аммоса Федоровича Ляпкина-Тяпкина. Все знают этого судью, но не все знают, что он очень увлекается химией. Вот что он сообщает.
Видеофрагмент:
«Многоуважаемые коллеги-химики 8-го класса!
Недавно я познакомился с одним из типов химических реакций – реакциями обмена. Несмотря на мои обширные познания в области химических наук, у меня возникла проблема – в моем распоряжении есть следующие реактивы: растворы серной кислоты, карбоната натрия, хлорида магния, гидроксида натрия. Все эти вещества сложные и, следовательно, они должны вступать в реакции обмена, но на практике оказалось, что не все они между собой взаимодействуют или… взаимодействуют, но я ничего не наблюдал. Почему? Чего я не учел? Помогите мне, пожалуйста, разрешить эту проблему. Буду вам премного благодарен. Искренне ваш коллега – судья А.Ф. Ляпкин-Тяпкин.
Р. S. Вместе с письмом высылаю вам все перечисленные реактивы».
Учитель. Ну, что, ребята, поможем Ляпкину-Тяпкину разобраться с его проблемой? Но прежде чем мы начнем выполнять практическое задание, давайте разберемся: о каком типе химических реакций пишет Ляпкин-Тяпкин.
Ученики. Реакции обмена.
Учитель. Что необходимо помнить при проведении реакций обмена?
Ученики. Условия протекания реакций обмена: выделение газа, выпадение осадка, образование воды.
Учитель.
Если выделится газ – это раз,
И получится вода – это два,
А еще нерастворимый осаждается продукт.
«Есть осадок», – говорим мы.
Это третий важный пункт.
Химик правила обмена не забудет никогда:
В результате непременно будет газ или вода,
Или выпадет осадок – вот тогда порядок!
Задание. С реактивами, полученными от Ляпкина-Тяпкина, давайте проведем лабораторные опыты, иллюстрирующие реакции обмена, и вы запишете соответствующие уравнения реакций с учетом правил написания реакций обмена в своих схемах-конспектах. И помните о правилах техники безопасности при выполнении лабораторных опытов – пробирки и склянки держим на уровне глаз, работаем аккуратно и с малым количеством реактивов.
Пробирка № 1. H2SO4 + Na2CO3 —> наблюдается выделение газа.
Пробирка № 2. Na2CO3 + MgCl2 —> наблюдается выделение осадка.
Пробирка № 3. NaOH + H2SO4 —> видимых изменений нет, образование воды.
Учащиеся выполняют лабораторные опыты и записывают соответствующие уравнения реакций в схеме-конспекте урока. Двое учащихся (по одному из каждой группы) выполняют задания у доски.
В схеме-конспекте (табл. 4) записано:
Таблица 4
|
Условия |
Уравнения реакций |
|
Выделение газа |
H2SO4 + Na2CO3 —> ………. |
|
Выделение осадка |
Na2CO3 + MgCl2 —> ………. |
|
Образование воды |
NaOH + H2SO4 —> ………. |
Учитель. Друзья, просигнализируйте мне карточками, у кого первое и второе уравнения получились такими же, как записано на доске?
Ребята, сейчас вы провели опыты, демонстрирующие условия протекания реакций обмена: выделение газа, осадка и образование воды. Однако в третьей пробирке вы ничего не наблюдали. Объясню, почему. Реакция между кислотами и основаниями – это частный случай реакции обмена, и называется она реакцией нейтрализации.
Основание и кислота –
Два непримиримых врага,
Сразу вступают в реакцию,
Название которой – нейтрализация.
Соль и Н2О нам получить дано.
Показ видеофрагмента «Хамелеон».
Учитель. Ребята, сейчас вы увидели животное. Вы узнали его? Что вы можете о нем рассказать?
Ученики. Это хамелеон. Он изменяет свою окраску в зависимости от внешних условий.
Учитель. А как вы думаете, почему я его вам сейчас показал? Какие химические вещества, подобно хамелеону, меняют свою окраску? Как они называются?
Ученики. Индикаторы: лакмус, фенолфталеин, метиловый оранжевый.
Учитель. Теперь вернемся к реакции нейтрализации. Я продемонстрирую ее вам. Для того чтобы наглядно была видна эта реакция, в реакционную смесь добавим несколько капель индикатора фенолфталеина. Фенолфталеин в нейтральной, а также в кислой среде – бесцветный, а в щелочной – малиновый.
Д е м о н с т р а ц и я:
NaOH + фенолфталеин + H2SO4 —> обесцвечивание раствора.
Ученики записывают третье уравнение реакции в схеме-конспекте.
Учитель. Итак, третий этап позади, мы помогли господину Ляпкину-Тяпкину разобраться в его проблеме, и я могу смело прикрепить звездочку, а также наградить вас ауриками. Но прежде чем мы перейдем к 4-му этапу, я предлагаю немного отдохнуть и устроить «стрельбу глазами».
Задание «Стрельба глазами».
1. В периодической системе найдите самый активный элемент-неметалл. (F.)
2. Переведите свой взгляд влево, на элемент, стоящий в том же периоде в III группе. (B.)
3. Переведите взгляд вниз и влево, на самый активный металл. (Fr.)
4. Переведите взгляд вверх и вправо, на элемент, атомы которого образуют вещество, поддерживающее горение. (O.)
5. Переведите взгляд вниз и влево, на элемент, атомы которого образуют металл, используемый в градусниках. (Hg.)
6. Переведите взгляд вверх и вправо, на элемент с относительной атомной массой 35,5. (Cl.)
7. Переведите взгляд вниз и влево, на элемент, давший группе элементов название «лантаноиды».(La.)
8. Переведите свой взгляд вверх и вправо, на самый электроотрицательный элемент. (F.)
9. Переведите свой взгляд вниз и влево, на элемент, атомы которого образуют драгоценный металл желтого цвета. (Au.)
4-й э т а п «Химический букет»
Учитель.
На химической поляне
Чудо-формулы цветут
Соберем давайте с вами
Из цветов букеты тут.
В центре цветов записаны формулы веществ.
|
Формула |
АВ |
А |
В |
СД |
С |
Д |
СВ |
АД |
|
Количество цветков, шт. |
4 |
4 |
4 |
4 |
4 |
4 |
4 |
4 |
Учитель. Задание. Из химических цветов собрать соответствующие букеты химических реакций(табл. 5).
Таблица 5
|
Название «букета» |
Уравнения из химических «цветов» |
|
Реакция соединения |
|
|
Реакция разложения |
|
|
Реакция замещения |
|
|
Реакция обмена |
По одному ученику из группы приглашают к доске составлять «букеты», остальные на своих местах записывают схемы реакций в своих схемах-конспектах.
Учитель. Вот и 4-й этап позади (прикрепляет звездочку).
V. Установление общих закономерностей
Учитель. Друзья! Мы почти достигли цели. Впереди последний этап – «Химический снегопад».
5-й э т а п «Химический снегопад»
Учитель.
Снег идет, и снег кружится.
Он ковром везде ложится.
Приглашаю всех я вас
Поиграть в снежки сейчас.
Ребята, мы с вами сейчас повторили и обобщили тему «Типы химических реакций», и я предлагаю вам оценить себя с помощью снежинок. Но снежинки у нас необыкновенные – химические. На снежинках разного цвета написаны задания разной степени трудности. Вы должны выбрать для себя задания по силам и на оценку, которая вас устраивает. Тексты с заданиями у вас записаны в схеме-конспекте.
Задание на «3» «Синяя снежинка». Расставьте коэффициенты в уравнениях химических реакций, укажите типы химических реакций (табл. 6).
Таблица 6
|
Уравнение реакции |
Тип химической реакции |
|
а) Al + Cr2O3 —> Al2O3 + Cr |
|
|
б) Li + N2 —> Li3N |
|
|
в) K2S + CuCl2 —> CuS + KCl |
|
|
г) N2O —> N2 + O2 |
Задание на «4» «Голубая снежинка». Допишите уравнения реакций, расставьте коэффициенты, укажите типы химических реакций (табл. 7).
Таблица 7
|
Уравнение реакции |
Тип химической реакции |
|
а) Ca + Cl2 —> ………. |
|
|
б) HNO3 + Cu(OH) 2 —> ………. |
|
|
в) Mg + TiCl4 —> ………. |
|
|
г) AgBr —> ……………… |
Задание на «5» «Белая снежинка». Допишите практически осуществимые уравнения реакций, расставьте коэффициенты, укажите типы химических реакций (табл. 8).
Таблица 8
|
Уравнение реакции |
Тип химической реакции |
|
а) Mg + O2 —> ………. |
|
|
б) Fe3O4 + Al —> ………. |
|
|
в) H3PO4 + HCl —> ………. |
|
|
г) Ba(OH)2 + H2SO4 —> ………. |
|
|
д) H2O —> …………… |
Учитель. Кто желает у доски выполнить задания?
Желающие работают у доски, остальные на своих местах пишут уравнения в схеме-конспекте.
Проводится проверка выполненных заданий, раздаются аурики.
Учитель. Вот и все! (Прикрепляет последнюю звездочку.) Мы достигли цели! Кто-то из вас пришел к вершине горы без поражений, а кто-то был почти у края пропасти. Теперь давайте посмотрим, что же за сюрприз нас ожидает.
На вершине горы – два конверта: «Сюрприз» и «Суперприз».
Учитель вскрывает конверт «Сюрприз», в котором находятся кружочки с изображением отметок «3», «4», «5».
Учитель. Ребята, покажите свои наградные листы. А теперь обмениваем заработанные вами аурики на оценки: 3 аурика – одна «5»; 2 аурика – одна «4». (Учитель раздает оценки.)
А теперь, ребята, вспомните, какие слова были произнесены мною в самом начале урока?.. «На горе вас ждет сюрприз, там еще и суперприз…» Итак, суперигра! Принять участие в ней может тот, кто имеет не менее одной пятерки.
Суперприз на горе.
Кто рискнет своей пятеркой,
Тот получит сразу две!
Учитель вскрывает пакет «Суперприз» и читает задание.
Задание суперигры «Крестики-нолики». За 30 с необходимо найти выигрышный путь, состоящий из уравнений реакций замещения (табл. 9).
Таблица 9
|
Fe2O3 + 3H2 = 3H2O + 2Fe |
4NO2 + 2H2O + O2 = 4HNO3 |
4AgNO3 = 2Ag2O + 4NO2 + O2 |
|
Cl2 + 2KI = 2KCl + I2 |
Na2SO4 + BaCl2 = BaSO4 + 2NaCl |
2Zn + O2 = 2ZnO |
|
2Al + 6HCl = 2AlCl3 + 3H2 |
Cu(OH)2 = CuO + H2O |
2HCl + Zn = ZnCl2 + H2 |
VI. Домашнее задание
Учитель. В ваших схемах-конспектах записано домашнее задание, которое вы должны выполнить к следующему уроку. Каждый выбирает себе задание на ту оценку, которая его устраивает.
Задание на «3». Расставьте коэффициенты в уравнениях химических реакций, укажите типы химических реакций (табл. 10).
Таблица 10
|
Уравнение реакции |
Тип химической реакции |
|
а) Al + O2 —> Al2O3 |
Реакция…………….. |
|
б) MnO2 + H2 —> Mn + H2O |
Реакция…………….. |
|
в) H2O2 —> H2 + O2 |
Реакция…………….. |
|
г) HNO3 + Fe(OH)3 —> Fe(NO3)3 + H2O |
Реакция…………….. |
Задание на «4». Допишите уравнения реакций, расставьте коэффициенты, укажите типы химических реакций (табл. 11).
Таблица 11
|
Уравнение реакции |
Тип химической реакции |
|
а) AgI —>……….. |
Реакция…………….. |
|
б) MgO + H2SO4 —>……….. |
Реакция…………….. |
|
в) Al + HCl —>……….. |
Реакция…………….. |
|
г) Na + Cl2 —>……….. |
Реакция…………….. |
Задание на «5». Допишите практически осуществимые уравнения реакций, расставьте коэффициенты, укажите типы химических реакций (табл. 12).
Таблица 12
|
Уравнение реакции |
Тип химической реакции |
|
а) HNO3 + Mg (OH) 2 —> ………….. |
Реакция…………….. |
|
б) FeCl3 + Zn —>……….. |
Реакция…………….. |
|
в) CH4 —>……….. |
Реакция…………….. |
|
г) KOH + Ca (OH) 2 —> ………….. |
Реакция…………….. |
|
д) Ba + O2 —>……….. |
Реакция…………….. |
VII. Подведение итогов
Учитель. Сегодня на уроке мы систематизировали ваши знания по теме «Типы химических реакций». И я думаю, что в дальнейшем вам не составит труда описывать химические свойства веществ, осуществлять цепочки химических превращений, решать задачи. Спасибо вам за хорошую, плодотворную и интересную работу.
План-конспект урока химии в 8 классе в соответствии с требованиями ФГОС, представленный Карповой Стеллой Сергеевной, учителем химии Алексеевской СОШ №1 Алексеевского муниципального района
Тема урока: «Оксиды»
Класс: 8
УМК: О.С. Габриелян
Тип урока: урок изучения нового материала
Цель урока: сформировать понятие об оксидах как об одном из классов химических соединений; рассмотреть состав, строение, номенклатуру, свойства.
Задачи:
Образовательные задачи:
-
дать понятие об оксидах
-
продолжить формирование умения составлять формулы веществ, используя валентность элементов, названия веществ.
-
закрепить знания химической номенклатуры для бинарных соединений
-
показать значение оксидов в природе и жизни человека.
Развивающие задачи:
-
Развивать речевые навыки, наблюдение и умение делать выводы
-
Развивать умение работать коллективно
-
Развивать критическое мышление
-
Развивать интерес к химической науке
Воспитательные задачи:
-
Воспитывать умение работать в атмосфере поиска, творчества, прививать чувство ответственности за выполненную работу, самостоятельность, общительность, коммуникабельность.
ТАВСО:
Оборудования: ПК учителя, мультимедийная установка, дидактические карточки.
Реактивы: оксида кальция, оксид кремния (IV) SiO2, оксид меди (I) CuO, оксид железа (III) Fe2O3, вода, бусы из агата, углекислый газ; лотки для лабораторного оборудования, протоколы для выполнения лабораторного опыта.
Планируемые результаты обучения:
Предметные:
-
продолжить формировать систему предметных знаний;
-
сформировать умение переводить из одной знаковой системы в другую (формула-название, название-формула);
-
овладение терминологией;
-
сформировать способность применять знания для практических задач.
Метапредметные:
-
научить планировать собственную деятельность;
-
научить осуществлять контроль и оценку своей деятельности.
Личностные:
-
сформировать устойчивый интерес к поиску решения проблемы;
-
саморазвитие и самосовершенствование.
Литература для учителя: Габриелян. И.Г. Остроумов. Настольная книга для учителя. Дрофа, М.-2008.
Литература для учащихся: Габриелян О.С. Химия — 8 класс. Учебник для общеобразовательных учебных заведений. Дрофа, М.-2012.
План-конспект урока
|
Этапы урока |
Время |
Деятельность учителя |
Деятельность учащихся |
|
1. Организационный момент |
1 мин. |
Здравствуйте, ребята! (проверка готовности к уроку) |
Приветствуют учителя. |
|
2. Мотивация |
2 мин. |
На демонстрационном столе находятся разные на первый взгляд вещи: вода, речной песок, негашеная известь, бусы из агата. Как вы считаете, почему сегодня на уроке я демонстрирую их вам? Что же их объединяет? Ответ на вопрос предполагаю получить в конце урока после изучения новой темы. |
Ученики рассматривают вещи: воду, речной песок, негашеную известь, бусы из агата и предполагают, что их объединяет. |
|
3. Актуализация знаний. |
7 мин. |
На предыдущих уроках вы научились определять степень окисления элементов по формуле и составлять формулы по степеням окисления. Вспомните эти действия и выполните задания на карточках №1 (Приложение*). |
Выполняют задания на карточках, делают самопроверку. |
|
4. Изучение нового материала |
23 мин. |
-Что вы заметили общего в формулах, с которыми работали? -Верно. Эти вещества называются оксиды. И тема нашего урока: «Оксиды». (Тема записывается на доске) -Сформулируем определение оксидов, ответив на 3 вопроса. а) какие вещества по составу? б) сколько элементов в составе? в) какой элемент обязательно входит в состав оксидов, его валентность? — (создание проблемной ситуации и ее решение) Ребята, а это оксид? H2O2 -Дайте определение оксидам. — Сейчас мы попытаемся понять, каким же образом образуются оксиды? (На доске написаны формулы пяти оксидов). Взгляните на формулу первого оксида СО, как вы думаете, какие простые вещества вступали в реакцию, чтобы образовался данный оксид? Запишем уравнение реакции: C + O2 = 2CO (учитель записывает уравнение реакции). -Значит оксиды образуются в результате реакции простых веществ с кислородом. Кто хочет на доске записать уравнения реакций получения остальных оксидов? -Итак, ребята, теперь давайте посмотрим, как же давать названия оксидам. Единственный момент, на который вы должны обратить внимание: постоянную или переменную валентность имеет элемент, входящий в состав оксида. Давайте дадим название оксиду СО. Это соединение сложное, состоит из двух элементов, один из которых кислород. Значит, это оксид. -Оксид какого элемента? -Углерод имеет постоянную или переменную валентность? -В данном случае его валентность II. Оксид СО называют «оксид углерода (II)». -Кто хочет попробовать у доски дать название другим оксидам? -Сейчас ребята, переходим к изучению физических свойств оксидов. Для этого выполним лабораторный опыт. В ваших лабораторных лотках стоят образцы оксидов, а на столах лежат протоколы (Приложение*), которые необходимо заполнить, вы будете определять агрегатное состояние, цвет и запах выданных вам оксидов. Но прежде чем приступить к выполнению опыта вспомним основные правила техники безопасности, которые вы должны соблюдать. |
— Учащиеся выделяют общие признаки в формулах, работая в паре (Вещества, состоящие из двух элементов, один из которых кислород). — Записывают тему урока в тетради. -Учащиеся в тетради делают краткую запись, отвечая на вопросы. (1. Сложные вещества. 2. Состоят из 2 х.э. 3. О, II) -Это не оксид, т.к. валентность кислорода равна 1. -(Оксиды — это сложные вещества, состоящие из двух химических элементов, один из которых кислород c валентностью II) Учащиеся записывают определение в тетрадь. -Углерод и кислород. (один ученик работает у доски): 2Cl2 + 7O2 = 2Cl2O7 4Fe + 3O2 = 2Fe2O3 Ca + O2 = 2CaO 4Al + 3O2 = 2Al2O3 -Углерода. — Переменную. (один ученик работает у доски) 2Cl2 + 7O2 = 2Cl2O7 (оксид хлора (VII)) 4Fe + 3O2 = 2Fe2O3 (оксид железа (III)) Ca + O2 = 2CaO (оксид кальция) 4Al + 3O2 = 2Al2O3 (оксид алюминия). Один из учащихся отвечает с места. Учащиеся заполняют протокол. |
|
5. Закрепление изученного материала. |
8 мин. |
А теперь – физкультминутка. Но она у нас сегодня необычная и напрямую связана с темой нашего урока. На слайде вам будет показана формула вещества. Если оно является оксидом — вам нужно встать. Н2SO4, FeО, NН3, P2О3, NaН, Li2О, NO2, Н2, О2, НNО3, PbO Присаживайтесь. Продолжаем наш урок. Итак, с какими бинарными соединениями мы познакомились на сегодняшнем уроке? — Какие вещества мы называем оксидами? Мы научились с вами отличать оксиды от других веществ, называть их, составлять их формулы. Я предлагаю вам проверить себя: насколько хорошо вы овладели новыми знаниями. У вас на столах лежат карточки №2 (Приложение*) |
Ученики делают физкультминутку. -Оксиды. Один ученик отвечает с места. Учащиеся работают в парах. Самоконтроль по шаблону. |
|
6. Домашнее задание |
1 мин. |
Учитель озвучивает и комментирует домашнее задание: Изучить §41, упр.1; 2 (письменно) |
Записывают домашнее задание |
|
7. Подведение итогов. Рефлексия. |
3 мин. |
Наш урок подошел к завершению. Посмотрите, какие цели поставили в начале урока. Можно ли считать, что наши цели на урок достигнуты? Д. Хевелси говорил: «Мыслящий ум не чувствует себя счастливым, пока ему не удается связать воедино разрозненные факты им наблюдаемые». Посмотрим на демонстрационный стол. Надеюсь, что теперь вы можете ответить на вопрос, что объединяет воду, речной песок, негашеную известь и бусы из агата? Какую оценку вы поставите классу за работу на уроке и почему? Оцените свою деятельность на уроке и класса, нарисуйте в тетради смайлик веселый, грустный или нейтральный. Спасибо за урок! До свидания! |
Учащиеся делают выводы. Ответы учеников (их объединяет то, что все эти вещи – оксиды). Самооценка учеников. |
Приложение*
Карточка №1
1.Определите степень окисления по формуле:
Al2O3, Ag2O, FeO, N2O, SO2
2.Составьте формулы веществ по степеням окисления: CuO SiO ZnO SO PO.
Карточка №2
Выпишите в столбик из перечня химических формул веществ формулы оксидов и дайте им названия:
MgO, KOH, O3, SO3, SO2, Al2S3, CaCO3, Аl2O3, Mg(OH)2, CO2, Na2N, HCl, CaO, H2CO3, P2O5, FeCl3, Na2O, H2SO4, СuО, Cu2O, HNO3, NH3.
Лабораторный опыт №5
Ознакомление с образцами оксидов
Выполнение опыта:
1) Рассмотрите выданные вам образцы оксидов и ознакомьтесь с ними по плану: а) агрегатное состояние б) цвет в) запах
2) Занесите результаты в таблицу:
Таблица 1.
Физические свойства оксидов
|
Формула оксида |
Название оксида |
Агрегатное состояние |
Цвет |
Запах |
|
CaO |
||||
|
SiO2 |
||||
|
CuO |
||||
|
Fe2O3 |
||||
|
H2O |
||||
|
CO2 |
Сделайте вывод: в каком агрегатном состоянии могут быть оксиды? Какого они могут быть цвета?
Вывод: План-конспект нужен учителю, так как он поможет не сбиться с ритма урока, правильно рассчитать продолжительность того или иного этапа, своевременно его завершить. Я думаю, что мой план конспект урока по химии для 8 класса достаточно хороший и его можно использовать на уроке.
Использованная литература:
1. Урок химии по теме «Оксиды» // Интернет-ресурс: https://videouroki.net/razrabotki/urok-khimii-po-tiemie-oksidy.html
2. Урок по теме «Оксиды» // https://nsportal.ru/shkola/khimiya/library/2012/01/21/urok-po-teme-oksidy
3. Урок химии в 8 классе «Оксиды» (ФГОС) // Интернет-ресурс: https://multiurok.ru/files/urok-khimii-v-8-klassie-oksidy-fgos.html
4. Конспект урока химии для 8 класса по теме «Оксиды» // Интернет-ресурс: https://www.alllessons.ru/chemistry/konspekt-uroka-himii-dlya-8-klassa-po-teme-oksidy.html
5. Урок химии по теме «Оксиды» 8 класс // Интернет-ресурс: https://kopilkaurokov.ru/himiya/uroki/urok-khimii-po-tiemie-oksidy-8-klass
6. План-конспект урока по теме «Оксиды. Классификация. Получение и свойства». 8-й класс // Интернет-ресурс: http://открытыйурок.рф/статьи/651563/
7. Конспект урока по химии в 8 классе «Оксиды» // http://инфо-дети.рф/publikatsii/414-konspekt-uroka-po-khimii-v-8-klasse-oksidy
8. Конспект урока химии для 8 класса по теме «Оксиды» УМК «Химия. 8 класс» // Интернет-ресурс: http://pandia.ru/text/80/009/19082.php
9. Конспект открытого урока по химии в 8-м классе «Оксиды. Состав. Классификация» // Интернет-ресурс: http://открытыйурок.рф/статьи/573574/
10. Урок химии 8 класс Тема «Оксиды» // Интернет-ресурс: https://nsportal.ru/shkola/khimiya/library/2018/01/22/urok-himii-8-klass-tema-oksidy
11. Личный опыт.
Как быстро конспектировать лекции?
Как быстро конспектировать лекции? Это важный вопрос, который интересует каждого примерного студента на протяжении всего обучения в университете. Прежде чем говорить о секретах так называемого «быстрописания», необходимо выяснить, для чего вообще необходимы конспекты.
Польза конспектов
Конспект – это сжатое содержание пройденной темы в письменном виде, которое позволяет восстановить в памяти и запомнить новую информацию при подготовке домашнего задания.
Свои первые конспекты школьник начинает писать в старших классах, причем по русскому языку даже тема предусмотрена: «Как правильно конспектировать лекции».
Не стоит игнорировать эту важную информацию, иначе вместо понятного и доступного содержания перед глазами окажется сплошная «каша».
Если ученик научится правильно составлять конспекты, то в университете на лекциях проблем не будет возникать, а заполненная тетрадка станет верной подсказкой при дальнейшей подготовке к экзаменам.
Советуем почитать: Зачем писать лекции и конспекты?
Когда студент приходит на первый курс, то в течение семестра ему предстоит исписать ни одну толстую тетрадь.
Как правило, обучение, по большей части, состоит из таких конспектов, которые в течение полугода не пишутся, а в преддверие зачетной недели и экзаменов выпрашиваются у примерных студентов.
Здесь важно понять, что на сессии такими знаниями все равно никто не поделится, ведь это верный способ успешно сдать экзамены, получить стипендию и с чистой совестью отдыхать на заслуженных каникулах.
Переоценить пользу этого справочного материала просто невозможно, так что уже с первого курса требуется взять за главное правило учебы – примерно писать конспекты.
Это позволит избежать массу проблем, которые в дальнейшем становятся главным препятствием на пути к высшему образованию и долгожданному статусу «Молодой специалист».
Общие сведения о конспектах
Итак, в конспекте отражены темы лекции, причем во всех подробностях и с акцентом на главной мысли.
Каждый студент должен вести конспект, а для этого приходить на лекцию с тетрадью и набором разноцветных ручек.
Как правило, конспектирование новой темы начинается с даты и названия, а, чтобы надписи не сливались, желательно отступить несколько строк от пройденного ранее материала.
Сильные моменты и важные мысли требуется выделять цветом, а писать так, чтобы по приходу домой содержание новой темы не превращалось в самую настоящую шараду.
Если студент не знает, как правильно вести конспект, то должен обратиться к помощи всемирной паутины либо посетить школьную учительницу русского языка.
Она по старой памяти обязательно освежит упущенные в свое время знания, научит грамотно составлять конспект, а после успешно им пользоваться при очередной подготовке к предстоящей сессии.
Если говорить о пользе конспектов, то обязательно стоит выделить следующие моменты:
• заменяет учебники и посещение студенческой библиотеки;
• становится отличной шпаргалкой на экзамене;
• содержит только важную информацию по теме, то есть написан «без воды»;
• повторяет ценные мысли преподавателя по теме;
• не занимает в рюкзаке много места;
• гарантирует базовый уровень знаний по предмету;
• становится законной подсказкой на практических занятиях;
• тренирует память и скорость написания;
• участвует в выставлении итоговой оценки по предмету;
• характеризует студента с образцовой стороны.
Так что вполне очевидно, что эта вещь просто незаменима в студенчестве, а исписанные тетради желательно не выбрасывать, а сохранять на будущее: мало ли, при защите диплома пригодится, или можно найти подсказку на важный вопрос уже в статусе «молодого специалиста».
Умные люди и в 40 лет свято хранят свои студенческие конспекты: одни, как память, а другие, как неисчерпаемый источник ценной информации во все времена.
Предметы и конспекты
Многие студенты ошибочно полагают, что только точные науки требуют обязательного конспектирования лекций.
На самом деле это не так, поскольку экзамены в будущем сдают и экономисты, и гуманитарии, и историки, и юристы.
Важно понимать, что ведение конспекта – это неотъемлемая составляющая учебного процесса, которая является не только «подсказкой» при ответе, но и своего рода проверочной работой для студента и преподавателя.
Конечно, точные науки больше обращаются к старым конспектам, однако и другие специальности не исключают помощь этих исписанных разными пастами тетрадок.
Советуем почитать: Как правильно писать конспект?
Если студент приходит на лекцию, то конспект писать обязательно! Исключение составляют лишь те пары, на которых преподаватель лично избавляет от этой привычной в студенчестве обязанности! В остальном, ручка в течение 1 часа 20 минут должна находиться в действии.
На заметку: если преподаватель видит, что студент открыто игнорирует написание конспекта, то сначала виду не подаст, а в дальнейшем (на экзамене) обязательно припомнит старую обиду.
Дело в том, что часть педагогов настаивают на конспектировании новых тем по своим предметам; мало того, по итогам семестра проверяют их присутствие в рукописном варианте.
Если конспекты отсутствуют, то можно не рассчитывать на быстрый допуск к экзамену, а итоговая оценка будет обязательно снижена, что негативно отразится на будущей стипендии (поставит ее получение под большой вопрос).
Многие студенты уже поплатились за свою лень, когда за ночь переписывали по 48 страниц конспекта, чтобы наутро угодить строгому преподавателю.
Но такой подход можно смело назвать «отпиской», ведь важная информация по теме в таком огромном количестве и в сжатые сроки все равно не отложится в голове, а превратится в «кашу» и неудовлетворительную оценку за ответ на экзамене.
Лучше всего все делать своевременно, а не в последнюю минуту!
Правила составления конспекта
Итак, если студент решил, что отныне конспект – его вечный друг и помощник, то должен научиться его правильно составлять.
Как упоминалось выше, новая тема должна быть обозначена датой и цветом, а содержание не сливаться в одну «простынь».
Однако есть и другие важные моменты, на которых обязательно следует акцентировать свое внимание.
1. На паре преподаватель говорит много и не всегда по теме, именно поэтому студент должен находить в его бесконечных речах то «луч света», которое «прольет истину» на новую тему. Именно эти важные мысли требуется заносить в свой конспект.
2. Не стоит писать мысли в строчку, желательно выбрать цитатную манеру написания, то есть каждая новая идея с новой строки. Между соседними цитатами желательно делать пропуск – для лучшего восприятия информации, так сказать.
3. Все, что преподаватель пишет, рисует или изображает на доске мелом, должно быть законспектировано (графически либо тезисно). Он акцентирует на этом внимание, значит – такая информация особенно важна для студента!
4. В конспекте приветствуются сокращения и аббревиатуры, а цифры должны писаться знаками, а не прописью. Такой сжатый подход позволяет запротоколировать больше полезной информации, да и суть написанного все равно не теряется. Главное – потом разобраться в содержании, поэтому составлять конспект желательно в своем привычном стиле.
5. Конспект – это не только сплошной текст со знаками препинания, это также нужные рисунки, графики, формулы, диаграммы, схемы и таблицы. Именно такие графические помощники заметно сокращают время на написание новой темы, легко запоминаются при подготовке к экзамену, а также всегда перед глазами.
Так что в написании конспекта нет ничего сложного, главное – задаться целью и учитывать все пожелания проверяющего преподавателя.
Советуем почитать: Как заслужить доверие преподавателя?
Например, некоторые педагоги выдвигают свои индивидуальные требования по ведению конспекта; не нужно спорить и, тем более, доказывать собственную правоту.
Если учесть все пожелания, то можно рассчитывать на благосклонность преподавателя при ответе на экзамене и выставлении итоговых оценок в зачетную книжку.
Как ускорить написание конспекта?
Есть такие преподаватели, которые считают, что студент не пишет, а слушает конспект. Сложно будет записать в тетрадь что-то полезное, но все же реально.
Действовать требуется по вышеописанной схеме, не забывая о цифрах, сокращениях и аббревиатурах.
Есть еще несколько секретов быстрого конспектирования:
1. Использование графического конспекта, то есть новая тема не написана, а изображена на чистых листах графически.
2. Использование диктофона, однако в домашних условиях придется все же переписать часть услышанного монолога в записи.
3. Использование конспекта – плана, когда студенту приходится самостоятельно дорабатывать новую тему по определенному на пару плану (в точной последовательности).
4. Увеличение скорости написания, но этот опыт приходит с годами обучения – больше практики.
5. Использование интернет – конспекта, когда студент находит информацию по теме на тематических сайтах и форумах всемирной паутины.
Вывод: Так или иначе, выход найдется, просто важно не ругать про себя суетливого преподавателя, а выбрать для себя ту манеру конспектирования, которая позволит отложить в памяти и сознании как можно больше ценной и полезной информации по конкретному предмету.
Каждый учащийся вуза делает свой выбор – как ему будет удобней учиться.
Большинство студентов по выпуску из университета согласны, что все свои экзамены сдали исключительно благодаря везению и конспектам.
Многие из них хранят до сих пор. Так может стоит воспользоваться этим ценным знанием и самому наконец-то завести хотя бы несколько конспектов по особенно важным предметам? Того глядишь, и учеба будет даваться гораздо легче!
Теперь вы знаете о том, как быстро конспектировать лекции.
С уважением, команда сайта советстуденту.рф
Анна Кислякова
Способы конспектирования и записи лекций
Конспектирование – это умение быстро мысленно произвести анализ текста и записать на бумаге самое важное. Существует большое разнообразие способов конспектирования лекций.
Однако, подобным навыкам, к сожалению, нигде специально не обучают. В то же время, умение конспектировать очень важно для студентов и школьников. Без умения быстро и грамотно писать лекции нельзя рассчитывать на получение хороших знаний.
Но как овладеть этим навыком? Какой способ конспектирования выбрать?
Для тех, кто хочет овладеть навыками конспектирования и записи лекций, есть хорошая новость – существуют способы и технологии эффективного конспектирования лекций, которые разработали для себя люди, добившиеся успехов в различных областях. Взяв их на вооружение, можно овладеть умением конспектирования, значительно облегчив себе жизнь.
Метод конспектирования Корнелла
Около полувека назад жил профессор по имени Вальтер Паук, преподававший в Корнелльском университете (отсюда и название), разработавший способ записи лекций, который по сей день популярен среди учащихся, особенно в американских учебных заведениях. В чем же заключается метод конспектирования Корнелла?
Лист бумаги (формат А4) необходимо разлиновать таким образом, чтобы вверху появилась горизонтальная колонка для даты и оглавления и внизу для записи главной мысли лекции, сформулировав ее несколькими предложениями. Оставшееся свободное пространство листа расчерчивается одной продольной линией, образуя две колонки – правая должна быть широкой, левая – узкой.
Конспектирование методом Корнелла осуществляется в правую колонку с промежутками для добавления, в случае необходимости, информации, а левая используется для выписывания в нее ключевых названий, фраз, цифровых данных. После лекций посредством анализа информации, содержащейся в правой колонке, выводится главная мысль и фиксируется в нижнем поле.
Суть данного способа записи лекций заключена в повторении информации, при ее анализе для выведения главных мыслей и идей, что способствует лучшему усвоению знаний. Но, при невыполнении последнего этапа, теряется вся практическая польза данного способа конспектирования, и он становится обычным записыванием лекции.
Способ конспектирования Билла Гейтса
Данная технология эффективного конспектирования была впервые отмечена Робом Ховардом.
Предприниматель Роб Ховард однажды во время деловой встречи с Гейтсом обратил внимание на то, что во время переговоров миллионер все темы и данные, представляющие интерес, записывал вручную, не прибегая к помощи электронных носителей.
Взглянув в его блокнот, бизнесмен увидел страницу, расчерченную на квадратные блоки, каждый из которых был заполнен данными определенной тематики.
Существует мнение, что способ конспектирования, используемый Гейтсом, – трансформированная копия способа квадратов. Использовать его можно, переделав под себя и свои цели. Например, размеры, формы и разделение по темам геометрических фигур могут быть абсолютно разными.
Технология эффективного конспектирования по методу ментальных карт
В семидесятых годах прошлого века известный телеведущий передачи «Думай головой», транслируемой одним из британских каналов, Тони Бьюзен использовал метод ментальных карт в своей программе.
Так и получил распространение этот способ конспектирования, который широко применяется и по сей день.
Особенно он популярен на западе среди людей, практикующих мозговой штурм для генерирования решений и идей.
Как же записывать лекции данным способом? Метод заключается в том, что на листе в центре чертится круг, допустима любая удобная геометрическая фигура, внутри которого пишется лекция.
Затем, рисуются еще квадраты (круги), содержащие основные мысли, определения, цифры, и соединяются прямыми линиями с блоком в центре.
Для записи лекций с помощью данного способа рекомендуется использовать разноцветные ручки, чтобы визуально выделять тексты определенной тематики, тем самым облегчая восприятие и запоминание.
Способ конспектирования лекций по методу красной строки
Все вышеперечисленные способы конспектирования созданы людьми для собственного удобства и имеют особенности, которые могут не совсем устроить других.
Поэтому тем, кто хочет освоить навыки конспектирования с использование более легкой методики, можно предложить способ, являющийся вариантом классического конспектирования.
Смысл его состоит в записи лекции с использованием красной строки для каждого нового предложения и проставлением порядкового номера.
Способ удобен тем, что при появлении связи последующих абзацев с начальными, можно поставить ссылку в виде номера нужного предложения и впоследствии, не просматривая всей лекции, быстро найти необходимые данные. Этот способ помогает составлять аккуратный, структурированный конспект, схожий с перечнем, что улучшает восприятие и запоминание информации.
Метод течения как технология эффективного конспектирования лекции
Консультант Скотт Янг утверждает, что лекция приносит пользу в том случае, если она непросто записывается, но вдумчиво прослушивается и анализируется.
Понятно, что при конспектировании все внимание направлено на запись информации, а не на мысленную обработку. Данная технология конспектирования предполагает запись только главных идей и мыслей с добавлением личных умозаключений.
Конечно, при этом конспект будет иметь значительные отличия от самой лекции, поэтому иметь диктофон на занятиях просто необходимо.
Как же развить умение конспектирования?
Умение и навыки конспектирования вырабатываются постепенно. Обычно у усердных студентов через некоторое время формируется свой индивидуальный способ грамотного конспектирования, и вопрос о том, как записывать лекции отпадает сам собой.
Вы можете комбинировать выше приведенные методы и технологии и выработать, таким образом, свой уникальный способ конспектирования. Здесь, как и в любом другом деле, главное не лениться и не сдаваться при первых же неудачах.
Помните: все приходит с опытом!
Необычные методы конспектирования
- Метод течения
- Метод Корнелла
- Метод Билла Гейтса
- Ментальные карты
- Метод красной строки
Быстрое конспектирование — один из важнейших навыков для тех, кто учится в школе или вузе.
Казалось бы, этому вопросу необходимо уделить внимание в первую очередь, чтобы облегчить ученикам процесс сохранения информации на бумаге. Но, как ни странно, быстрому конспектированию не учат совсем — притом, что это напрямую влияет на успехи в учебе.
Много ли студентов вообще способны разобрать то, что в спешке написали на лекциях?
Поэтому сегодня мы с вами поговорим о нестандартных методах конспектирования, изобретенных успешными людьми для собственного пользования — они пригодятся тем, кто предпочитает сохранять данные на бумаге, не доверяя электронике.
Метод течения
Недавно коуч Скотт Янг изобрел довольно оригинальный метод конспектирования, призванный не столько записывать информацию, сколько выражать мнение слушателя.
Он заключается в том, чтобы не просто пассивно прослушивать лекцию, а вникать в сказанное, анализировать и формировать собственные идеи на основе полученной информации. В конспект записываются основные тезисы лекции и ваши размышления по поводу услышанного.
Само собой, подобный конспект будет кардинально отличаться от того, что излагает преподаватель, поэтому для сохранения самого текста лекции лучше подстраховаться с помощью диктофона.
Метод Корнелла
Он получил свое название от Корнелльского университета, где преподавал придумавший его профессор Вальтер Паук. С того времени прошло больше полувека, но метод и сейчас пользуется успехом среди преподавателей и студентов, особенно в американских колледжах.
Для конспекта вам понадобится лист формата А4, ручка и линейка. Сверху страницы проведите горизонтальную черту, отделив ею поле для даты и заглавия.
Таким же образом отделите нижнюю часть страницы — в это поле вы напишете несколько предложений, в которых сконцентрируйте главную мысль лекции.
У вас останется средняя часть листа — ее необходимо расчертить вертикальной линией на большую правую колонку и маленькую левую.
Конспектируйте лекцию или параграф учебного пособия в большой колонке так, как вы привыкли это делать в тетради. Желательно оставлять после предложений небольшие промежутки, чтобы по мере необходимости что-то туда добавить.
Затем нужно заполнить узкую колонку — выписать ключевые даты, фамилии и названия напротив того места, где они встречаются в тексте.
В течение последующих суток заполните нижнюю часть страницы — несколькими фразами обрисуйте суть того, что написали в большой колонке.
Этот метод хорош тем, что вынуждает человека все время возвращаться к конспектам, пересматривать их и тем самым лучше запоминать информацию. Но если записи не дорабатывать, то метод Корнелла теряет свою главную идею и превращается в обычный короткий конспект.
Метод Билла Гейтса
В начале двухтысячных годов Роб Ховард, занимавшийся предпринимательской деятельностью, встретился с Биллом Гейтсом на переговорах. Это знакомство принесло ему много интересных наблюдений, поэтому Ховард поделился впечатлениями с читателями своего блога.
Наиболее поразительным было то, что один из самых богатых людей планеты не использовал для своих записей ноутбук или диктофон. Он все писал от руки на бумаге.
Ховард заглянул в блокнот собеседника и заметил, что страница разделена на несколько квадратов, в каждом из которых размещалась информация определенной тематики. К примеру, один из блоков отводился под вопросы, возникавшие у Билла в ходе общения.
Есть мнение, будто метод Билла Гейтса — не что иное, как несколько переделанный метод Корнелла, поэтому его можно трансформировать согласно потребностям пользователя, а не просто бездумно копировать. Размещение, величина квадратов и их тематика могут быть любыми — лишь бы они выполняли свое назначение.
Ментальные карты
На западе широко используется эта техника сохранения информации. Ее распространение связано с именем британского телеведущего и психолога Тони Бьюзена, активно применявшего ментальные карты в семидесятых годах минувшего века в своей телевизионной передаче «Думай головой» (Би-Би-Си). Сегодня этот метод довольно популярен среди тех, кто использует мозговой штурм для поиска новых идей.
Для начала нужно нарисовать в центре страницы круг или квадрат, в котором вы напишете тему лекции. После этого от центрального блока с помощью лучей отводите новые квадраты или круги, помещая в них важные понятия и данные.
При использовании этой техники лучше писать ручками разных цветов, чтобы ответвления разных тематик объединялись с помощью цвета.
Получить больше информации о правилах составления ментальных карт, вы сможете в одной из наших статей.
Метод красной строки
Если все вышеперечисленные методики кажутся вам слишком уж неординарными, предлагаем воспользоваться способом, не сильно отличающимся от классического конспектирования.
Заключается он в том, что вы записываете лекцию привычным способом, но каждое новое предложение начинаете с новой, красной строки, и при этом нумеруете их по порядку.
Таким образом, каждое предложение получает свой персональный номер.
Это поможет отсылать читателя (то есть самого себя) к разным частям конспекта с помощью цифровых пометок. К примеру, если в тексте имеется связь с каким-то фактом, указанном в начальных абзацах, то не нужно рисовать неудобные стрелки, а достаточно написать: «см. № 48». И тогда записи будут выглядеть намного аккуратнее, а структура, похожая на список, поможет в усвоении информации.
, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Викиум
Способы конспектирования и записи лекций. Приемы записи и конспектирования информации
Быстро и эффективно записать конспект со слов преподавателя, чтобы потом понять свои же закорючки и подготовиться к экзамену — непосильная задача для многих студентов. Перед сессией многие ксерокопируют и переписывают чужие труды вместо того, чтобы научиться самим правильно конспектировать.
В нашей статье мы расскажем о методах и приемах скоростного конспектирования, которые пригодятся не только в университете, но и в дальнейшей жизни.
Как происходит работа над конспектом?
Работа делится на 3 этапа:
- записываем важные моменты лекции;
- делаем краткие пометки и замечания, возникающие по ходу лекции;
- подводим итоги и проводим анализ — делаем собственные выводы по теме.
Помните, что каждую новую тему необходимо начинать с новой страницы, иначе запутаетесь и все ваши труды окажутся напрасными.
Метод ментальных карт
Метод ментальных карт или mind mapping — популярная техника записи, суть которой заключается в том, что основной текст конспекта размещается в середине листа.
Проще говоря, вы пишете основную мысль или понятие в середине страницы, заключаете его в кружок или рамку (как вам удобнее) и начинаете с помощью стрелок, которые расходятся в разные стороны, записывать ключевые идеи и слова, связанные с основным понятием.
Если вы любитель мозговых штурмов и готовы научиться виртуозно менять цвета ручек (а они вам пригодятся, чтобы делать стрелки более заметными), то этот метод для вас.
Метод «стрелочек»
Метод предложений
Метод предложений очень схож со стандартным методом стенограммы. Суть его заключается в том, что вы пытаетесь записать все, что говорит преподаватель. Главное отличие от метода стенограммы — каждое предложение записывается с новой строчки и нумеруется по порядку.
Нумерация помогает не запутаться во время чтения конспекта и отсылает от одного предложения к другому с помощью одной маленькой пометки (например, «см. №69») — больше не нужно разбираться в запутанных стрелках, которые перечеркивают пол страницы и вдобавок половину записей.
Ну а если осваивать эти методы конспектирования вам не хочется или не под силу, то студенческий сервис всегда готов прийти на помощь. Курсовые, дипломные, рефераты, контрольные и другие учебные работы — напишем все, что вы не законспектировали.
В школе и институте редко учат искусству конспектирования, хотя именно это умение может оказаться одним из ключевых навыков, обеспечивающих успех в учебе. Как структурирует свои пометки Билл Гейтс, что такое метод Корнелла и кто больше всех пропагандировал mind-mapping — 5 полезных техник конспектирования для тех, кто по-прежнему предпочитает бумагу и ручку.
Метод ментальных карт (mind-mapping)
Mind-mapping — это популярная техника записи, по правилам которой начинать нужно всегда в середине листа. В кружочке или в рамочке прямо по центру страницы нужно указать главное понятие, о котором пойдет речь в конспекте.
И потом с помощью ответвлений в разные стороны записывать в новых кружочках ключевые слова и идеи, с ним связанные. Если вы собираетесь использовать этот метод, лучше запастись ручками как минимум трех разных цветов, чтобы делать более заметными разные ответвления.
Главным популяризатором этой техники был Тони Бьюзан — английский психолог и телеведущий, который активно использовал метод ментальных карт в середине 1970-х годов в своей телепередаче «Use Your Brain». Сегодня к этому методу часто прибегают любители мозговых штурмов.
Метод течения (flow method)
Если вы устали стенографировать в своих конспектах, можно попробовать этот, недавно сформулированный коучем Скоттом Янгом, метод конспектирования. В основе его лежит такая идея: слушать лекцию — это не пассивный процесс, чтобы по-настоящему получить от лекции пользу, нужно думать и развивать собственные идеи.
Современные методы конспектирования. Способы и технологии эффективного конспектирования лекций
В школе и институте редко учат искусству конспектирования, хотя именно это умение может оказаться одним из ключевых навыков, обеспечивающих успех в учебе. Как структурирует свои пометки Билл Гейтс, что такое метод Корнелла и кто больше всех пропагандировал mind-mapping — 5 полезных техник конспектирования для тех, кто по-прежнему предпочитает бумагу и ручку.
Метод конспектирования Корнелла
Быстро записать лекцию со слов преподавателя, оформить конспект так, чтобы через месяц он пригодился в подготовке к экзамену — навык, которому не учат ни в школе, ни в ВУЗах.
Диктофоны, видеокамеры — студенты применяют любые технические новинки, чтобы облегчить трудный учебный процесс.
статьи
Но, оказывается, что доверяя технике сделать точную копию урока, студенту впоследствии приходится тратить втрое больше времени на повторение пройденного. А потому пока нет лучшего изобретения для конспектирования, чем простая ручка и бумага.
Преподаватель Cornell University (США) профессор Walter Pauk предложил ученикам колледжей методику быстрой записи лекции на бумагу. Американским студентам новшество пришлось по душе, и метод конспектирования Корнелла (так назвали предложение Паука) стали применять учащиеся других стран.
В чем суть методики?
Рассказывая о придуманной методике, профессор Паук в своей книге предлагает не механическое перенесение слов оратора в тетрадь, а фиксирование главных тезисов темы с последующей самостоятельной доработкой текста.
Шаблон конспекта по методу Корнелла
Работа над материалом проходит в три этапа:
- Запись важных моментов лекции.
- Краткие пометки, замечания, возникающие по ходу предмета.
- Итог — домашний анализ пройденного, выраженный несколькими фразами.
Такой подход к предмету, поможет студентам не только запомнить материал, но и легко ориентироваться в теме, быть готовыми к вопросам на экзамене.
На конкретном примере
Рассмотрим пример на русском языке, как пишутся конспекты по методу Корнелла.
Есть следующий исходный текст:
«В 13 году до н. э. Август вернулся из длительной экспедиции на Запад, где он инспектировал положение дел в Галии и Испании. Сенаторы решили отметить его возвращение и постановили воздвигнуть на Форуме (главном месте Рима) памятник Августу.
И не просто грандиозный каменный монумент, архитектура которого будет напоминать великие деяния императора, а жертвенник — религиозное сооружение, где Август и его приближенные смогут воздать хвалу богам.
Но император выбрал другое место Рима – Марсово поле».
Образец краткой записи того текста, который приведен выше:
С чего начать?
Лист (формат А4) или тетрадную страничку надо разлиновать. Проведите вертикальные линии:
- сверху — для названия темы;
- снизу — для личных выводов об услышанном на лекции (5-6 предложений).
После, одной горизонтальной линией, разделите лист на две неравные колонки:
- левая (5 см) — для вопросов, относящихся к теме.
- правая — для краткой записи основных моментов.
Можно для начала скачать готовый шаблон, а после разлиновывать лист самим.
Приступаем к работе
- Основные идеи лектора заносите в правую колонку. Буквально записывать слова не нужно, достаточно выделить ключевой момент.
- Пользуйтесь личной системой сокращения (жертвенник — жер.).
- Оставляйте пробелы после предложений.
Позже заполните их своими фразами.
- В левой колонке в течение урока вставляйте возможные вопросы по теме: «Почему это произошло? Когда случилось?».
- В короткий срок (уже дома) вернитесь к своим заметкам, заполните пробелы в основной колонке и запишите личные выводы под нижней горизонтальной линией. Без этой доработки метод Корнелла становится бесполезным, обращая ваш труд в обычное конспектирование.
- Перечертите необходимые диаграммы и таблицы. Наглядные картинки упрощают понимание материала.
Как готовиться к экзамену?
- В подготовительный период сосредоточьте внимание на резюме (в конце конспекта) и вопросы в левой колонке.
- Закройте правую часть и ответьте на потенциальные вопросы, которые составили сами.
- Выделите маркером главную мысль изучаемой темы.
Такая проработка материала, в отличие от утомительной зубрежки, даст положительные всходы.
Понимая причины, логику, последовательность событий, даже самый робкий ученик докажет, что он разбирается в предмете.
Кому подходит?
Предложенная система удобна для записи предметов, основанных на точно сформулированных темах, имеющих логический порядок.
Если в изучаемом предмете темы плавно перетекают в следующие, а способы их исследования меняются, то метод Корнелла лучше заменить другим видом конспектирования.
Итог
Корнелльским методом студенты пользуются давно (более 60 лет). И отзывы учеников, изучивших эту нетрудную систему, доказывают ее эффективность:
Ангелина, СамГУ (Самарский университет):
«Прочитала книгу Паука в оригинале, так как русского варианта не нашла. И заразилась его идеей нового подхода к конспектам. Не всегда получалось дорабатывать сделанную на лекции запись. Но к экзамену подошла со счетом 18:7, т. е.
18 листов с личными пометкам, вопросами и выводами, а 7 листов написанных по старинке, без домашней проработки. И мне казалось, что вижу эти 7 листов впервые. Ничего не помнила! Зато «проработанные» 18 лекций почти не пришлось учить.
Всего 20 минут самостоятельного анализа, сэкономили часы в предэкзаменационный период!»
«Как записывать лекции? Cornell note taking!»
P.S. Рекомендую другие статьи:
Культуры знание облегчает понимание
Самостоятельное проживание: какой опыт и уроки можно из него вынести
Что выбрать для учебы: ПК, ноутбук или планшет?
ТОП-20 профессий будущего: мировые тенденции
Хочу поступить в немецкий колледж (Studienkolleg)


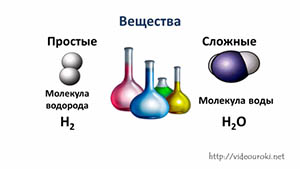


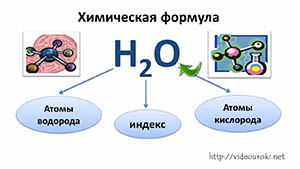
















-p-1080.jpg)
.jpg)


%D0%B0.jpg)
.jpg)






















































