О «Спутник Лайт»
«Спутник Лайт» является первым компонентом (рекомбинантный аденовирус человека 26 серотипа (rАd26)) вакцины «Спутник V» — первой в мире зарегистрированной вакцины против коронавируса.
Вакцина «Спутник Лайт», как и «Спутник V» создана на проверенной и хорошо изученной платформе аденовирусных векторов человека, которые вызывают обычную простуду и с которыми человечество мирно сосуществует тысячелетиями.
Безопасность вакцины «Спутник Лайт», первого компонента «Спутника V», подтверждена реальными данными по вакцинации в ОАЭ, Бахрейне, Аргентине, России, Мексике, Сербии, Сан-Марино, Филиппинах, Ливии, Парагвае, Венгрии, Азербайджане и Беларуси.
«Спутник Лайт», первый компонент «Спутник V» — безопасная и одобренная отдельная однокомпонентная вакцина
доказанная эффективность против заражения,
выше, чем у большинства зарубежных двухдозных вакцин
Эффективность против госпитализации и тяжелых случаев еще выше
«Спутник Лайт» — идеальный бустер:
- для людей, ранее переболевших COVID-19;
- для ревакцинации после Спутник V или других вакцин.
«Спутник Лайт», как отдельная вакцина, высокоэффективен против Дельта и других новых штаммов COVID-19
эффективность против
заражения штаммом Дельта

эффективность для
возрастной группы до 60 лет

выше, чем у большинства зарубежных двухдозных вакцин
- Эффективность против госпитализации и тяжелых случаев еще выше
В качестве бустера защита «Спутника Лайт» против штамма Дельта приближается к защите Спутник V
эффективность
против заражения

эффективность
против госпитализации

Вакцина «Спутник Лайт» в качестве бустера существенно повышает вируснейтрализующую активность против штамма Омикрон
сформировались антитела
к штамму Омикрон

«Спутник Лайт» обеспечивает длительную защиту, которая даже увеличивается в течение 4-6 месяцев после вакцинации.
В течение того же периода эффективность других зарубежных вакцин против штамма Дельта значительно снижается до уровня ниже 50%.
Безопасность и эффективность «Спутник Лайт» подтверждена реальными данными по вакцинации во многих странах, а также более чем 20 публикациями в ведущих международных научных изданиях.
- «Спутник Лайт» показал свою безопасность и высокую эффективность в комбинации с вакцинами AstraZeneca, Sinopharm и Moderna в совместных клинических международных исследованиях.
- Этот подход «вакцинного коктейля», впервые в мире был предложен командой «Спутник V».
«Спутник Лайт», первый компонент Спутник V – одна из ключевых вакцин в рамках программы иммунизации в Аргентине
40 000
35 000
30 000
25 000
20 000
15 000
10 000
5 000
Более чем в 35 раз меньше новых случаев COVID-19 за 4 месяца
- новые случаи
- новые случаи (в среднем за 7 дней)
июнь, 2021
июль, 2021
авг, 2021
сент, 2021
окт, 2021
Источник: JHU CSSE COVID-19 Data
Фаза I/II исследования безопасности и иммуногенности «Спутник Лайт» продемонстрировала следующие результаты:
- Иммунизация вакциной «Спутник Лайт» позволяет выработать антиген-специфические IgG антитела у 96,9% вакцинированных лиц на 28-й день;
- Вируснейтрализующие антитела вырабатываются на 28-й день после иммунизации у 91,67% лиц, получивших укол вакцины «Спутник Лайт».
- Клеточный иммунный ответ к S-белку SARS-CoV-2 формируется у 100% вакцинированных уже на 10-й день;
- Иммунизация вакциной «Спутник Лайт» лиц, у которых есть предсуществующий иммунитет к SARS-CoV-2, позволяет более чем в 40 раз увеличить уровень антиген-специфических IgG антител у 100% вакцинированных уже на 10-й день;
- Серьезных нежелательных явлений после иммунизации препаратом «Спутник Лайт» не зарегистрировано.
(Redirected from Sputnik Lite)
| Vaccine description | |
|---|---|
| Target | SARS-CoV-2 |
| Vaccine type | Viral vector |
| Clinical data | |
| Routes of administration |
Intramuscular |
| Legal status | |
| Legal status |
Full list of Sputnik Light authorizations |
Sputnik Light (Russian: Спутник Лайт, romanized: Sputnik Layt or Lajt[1]) is a single dose COVID-19 vaccine developed by the Gamaleya Research Institute of Epidemiology and Microbiology.[2] It consists of the first dose of the Sputnik V vaccine, which is based on the Ad26 vector, and it can be stored at a normal refrigerator temperature of 2–8 °C (36–46 °F).[3] The institute says this version would be ideally suited for areas with acute outbreaks, allowing more people to be vaccinated quickly.[4] It will also be used as a third (booster) dose for those who received Sputnik V at least 6 months earlier.[5]
Effectiveness[edit]
A vaccine is generally considered effective if the estimate is ≥50% with a >30% lower limit of the 95% confidence interval.[6]
As of September 2021, no study on Sputnik Light reported confidence intervals, so it is not possible to know the accuracy of the estimates. Effectiveness is generally expected to slowly decrease over time.[7]
A real-world study with participants aged 60–79 years in Argentina found that the single-injection vaccine is 79% (95% CI, 75–82%) effective in preventing infections, 88% (95% CI, 80–92%) effective against hospitalization, and 85% (95% CI, 75–91%) against death.[8] A phase III clinical trial in Russia also found an efficacy of 79%.[9][10] According to Nextstrain, lineage B.1.1.317 was the dominant variant in Russia during the study period (5 December 2020 to 15 April 2021),[9] while in Argentina (29 December 2020 to 21 March 2021)[8] lineage N.5 dominated at first, but soon many lineages coexisted in similar proportions.
Preliminary data from a study in Moscow in July 2021 indicate that the vaccine is 70% (95% CI, 64–75%) effective against symptomatic disease from the Delta variant for three months after vaccination.[11]
Composition[edit]
Composition, manufacturing sites and procedures, logistics and concerns about adverse effects and quality control are the same as the first dose of the Sputnik V vaccine. As a result, issues related to the second dose, such as the possible presence of replication-competent particles, do not apply to Sputnik Light.
Clinical trials[edit]
In January 2021, Sputnik Light commenced phase I/II trials.[12]
In February, Sputnik Light commenced phase III trials.[10]
Heterologous prime-boost vaccination[edit]
In August 2021, RDIF announced that preliminary results from a study on heterologous prime-boost vaccination indicate that it is safe to administer Sputnik Light as the first dose, then the Oxford–AstraZeneca, Moderna or Sinopharm BIBP vaccine as the second dose, as well as the homologous course consisting of Sputnik Light as the second dose.[13]
[edit]
Full authorization
Emergency authorization
Allowed for travel
Although Sputnik Light was not authorized by Ukraine or international organizations, tens of thousands of doses were shipped by Russia for use in non-government controlled parts of the eastern Donbas region from January 2021.[14] Ukrainian officials criticized the move.[15]
References[edit]
- ^ Filipenok A, Gubernatorov E (6 May 2021). «В России зарегистрировали вакцину «Спутник Лайт»» [Sputnik Light vaccine registered in Russia]. RBC (in Russian). Retrieved 7 May 2021. Lay summary.
- ^ «Russia Approves Single-Dose Sputnik Light Covid Vaccine For Use». NDTV Coronavirus. Agence France-Presse. 6 May 2021.
- ^ «Single dose vaccine, Sputnik Light, authorized for use in Russia» (Press release). Russian Direct Investment Fund. 6 May 2021. Retrieved 7 May 2021.
- ^ «Russia authorises single-dose Sputnik Light COVID vaccine for use -RDIF». Reuters. Moscow. 6 May 2021. Retrieved 29 June 2021.
- ^ «Russia launches Sputnik Light vaccine into wide circulation». reuters. Moscow. 29 June 2021. Retrieved 25 June 2021.
- ^ Krause P, Fleming TR, Longini I, Henao-Restrepo AM, Peto R (September 2020). «COVID-19 vaccine trials should seek worthwhile efficacy». Lancet. 396 (10253): 741–743. doi:10.1016/S0140-6736(20)31821-3. PMC 7832749. PMID 32861315.
WHO recommends that successful vaccines should show an estimated risk reduction of at least one-half, with sufficient precision to conclude that the true vaccine efficacy is greater than 30%. This means that the 95% CI for the trial result should exclude efficacy less than 30%. Current US Food and Drug Administration guidance includes this lower limit of 30% as a criterion for vaccine licensure.
- ^ Khoury DS, Cromer D, Reynaldi A, Schlub TE, Wheatley AK, Juno JA, et al. (May 2021). «Neutralizing antibody levels are highly predictive of immune protection from symptomatic SARS-CoV-2 infection». Nature Medicine. 27 (7): 1205–1211. doi:10.1038/s41591-021-01377-8. ISSN 1546-170X. PMID 34002089. S2CID 234769053.
- ^ a b González S, Olszevicki S, Salazar M, Calabria A, Regairaz L, Marín L, et al. (1 October 2021). «Effectiveness of the first component of Gam-COVID-Vac (Sputnik V) on reduction of SARS-CoV-2 confirmed infections, hospitalisations and mortality in patients aged 60-79: a retrospective cohort study in Argentina». EClinicalMedicine. 40: 101126. doi:10.1016/j.eclinm.2021.101126. ISSN 2589-5370. PMC 8435263. PMID 34541480.
- ^ a b «Single dose vaccine, Sputnik Light, authorized for use in Russia» (Press release). Russian Direct Investment Fund. 6 May 2021. Retrieved 29 June 2021.
The single dose Sputnik Light vaccine demonstrated 79.4% efficacy according to analyzed data taken from 28 days after the injection was administered as part of Russia’s mass vaccination program between 5 December 2020 and 15 April 2021.
- ^ a b Clinical trial number NCT04741061 for «Study to Evaluate Efficacy, Immunogenicity and Safety of the Sputnik-Light (SPUTNIK-LIGHT)» at ClinicalTrials.gov
- ^ Dolzhikova IV, Gushchin VA, Shcheblyakov DV, Tsybin AN, Shchetinin AM, Pochtovyi AA, et al. (14 October 2021). «One-shot immunization with Sputnik Light (the first component of Sputnik V vaccine) is effective against SARS-CoV-2 Delta variant: efficacy data on the use of the vaccine in civil circulation in Moscow» (Preprint). doi:10.1101/2021.10.08.21264715. S2CID 238747906 – via medRxiv.
- ^ Clinical trial number NCT04713488 for «An Open Study on the Safety, Tolerability, and Immunogenicity of «Sputnik Light» Vaccine» at ClinicalTrials.gov
- ^ «Combination of the first component of Sputnik V vaccine (Sputnik Light vaccine) with vaccines by AstraZeneca, Sinopharm and Moderna demonstrates high safety profile during the study in Argentina’s Buenos-Aires province» (Press release). Moscow: Russian Direct Investment Fund. 4 August 2021. Retrieved 5 August 2021.
- ^ «Moscow Plays Up Donbas As Part Of The Ukraine Conflict». Warsaw Institute. 30 July 2021. Retrieved 4 August 2021.
- ^ «Residents of ORDLO can become ‘guinea pigs’ for Russian pharmacists — Defense Ministry». Interfax Ukraine. Retrieved 4 August 2021.
{{cite web}}: CS1 maint: url-status (link)
(Redirected from Sputnik Lite)
| Vaccine description | |
|---|---|
| Target | SARS-CoV-2 |
| Vaccine type | Viral vector |
| Clinical data | |
| Routes of administration |
Intramuscular |
| Legal status | |
| Legal status |
Full list of Sputnik Light authorizations |
Sputnik Light (Russian: Спутник Лайт, romanized: Sputnik Layt or Lajt[1]) is a single dose COVID-19 vaccine developed by the Gamaleya Research Institute of Epidemiology and Microbiology.[2] It consists of the first dose of the Sputnik V vaccine, which is based on the Ad26 vector, and it can be stored at a normal refrigerator temperature of 2–8 °C (36–46 °F).[3] The institute says this version would be ideally suited for areas with acute outbreaks, allowing more people to be vaccinated quickly.[4] It will also be used as a third (booster) dose for those who received Sputnik V at least 6 months earlier.[5]
Effectiveness[edit]
A vaccine is generally considered effective if the estimate is ≥50% with a >30% lower limit of the 95% confidence interval.[6]
As of September 2021, no study on Sputnik Light reported confidence intervals, so it is not possible to know the accuracy of the estimates. Effectiveness is generally expected to slowly decrease over time.[7]
A real-world study with participants aged 60–79 years in Argentina found that the single-injection vaccine is 79% (95% CI, 75–82%) effective in preventing infections, 88% (95% CI, 80–92%) effective against hospitalization, and 85% (95% CI, 75–91%) against death.[8] A phase III clinical trial in Russia also found an efficacy of 79%.[9][10] According to Nextstrain, lineage B.1.1.317 was the dominant variant in Russia during the study period (5 December 2020 to 15 April 2021),[9] while in Argentina (29 December 2020 to 21 March 2021)[8] lineage N.5 dominated at first, but soon many lineages coexisted in similar proportions.
Preliminary data from a study in Moscow in July 2021 indicate that the vaccine is 70% (95% CI, 64–75%) effective against symptomatic disease from the Delta variant for three months after vaccination.[11]
Composition[edit]
Composition, manufacturing sites and procedures, logistics and concerns about adverse effects and quality control are the same as the first dose of the Sputnik V vaccine. As a result, issues related to the second dose, such as the possible presence of replication-competent particles, do not apply to Sputnik Light.
Clinical trials[edit]
In January 2021, Sputnik Light commenced phase I/II trials.[12]
In February, Sputnik Light commenced phase III trials.[10]
Heterologous prime-boost vaccination[edit]
In August 2021, RDIF announced that preliminary results from a study on heterologous prime-boost vaccination indicate that it is safe to administer Sputnik Light as the first dose, then the Oxford–AstraZeneca, Moderna or Sinopharm BIBP vaccine as the second dose, as well as the homologous course consisting of Sputnik Light as the second dose.[13]
[edit]
Full authorization
Emergency authorization
Allowed for travel
Although Sputnik Light was not authorized by Ukraine or international organizations, tens of thousands of doses were shipped by Russia for use in non-government controlled parts of the eastern Donbas region from January 2021.[14] Ukrainian officials criticized the move.[15]
References[edit]
- ^ Filipenok A, Gubernatorov E (6 May 2021). «В России зарегистрировали вакцину «Спутник Лайт»» [Sputnik Light vaccine registered in Russia]. RBC (in Russian). Retrieved 7 May 2021. Lay summary.
- ^ «Russia Approves Single-Dose Sputnik Light Covid Vaccine For Use». NDTV Coronavirus. Agence France-Presse. 6 May 2021.
- ^ «Single dose vaccine, Sputnik Light, authorized for use in Russia» (Press release). Russian Direct Investment Fund. 6 May 2021. Retrieved 7 May 2021.
- ^ «Russia authorises single-dose Sputnik Light COVID vaccine for use -RDIF». Reuters. Moscow. 6 May 2021. Retrieved 29 June 2021.
- ^ «Russia launches Sputnik Light vaccine into wide circulation». reuters. Moscow. 29 June 2021. Retrieved 25 June 2021.
- ^ Krause P, Fleming TR, Longini I, Henao-Restrepo AM, Peto R (September 2020). «COVID-19 vaccine trials should seek worthwhile efficacy». Lancet. 396 (10253): 741–743. doi:10.1016/S0140-6736(20)31821-3. PMC 7832749. PMID 32861315.
WHO recommends that successful vaccines should show an estimated risk reduction of at least one-half, with sufficient precision to conclude that the true vaccine efficacy is greater than 30%. This means that the 95% CI for the trial result should exclude efficacy less than 30%. Current US Food and Drug Administration guidance includes this lower limit of 30% as a criterion for vaccine licensure.
- ^ Khoury DS, Cromer D, Reynaldi A, Schlub TE, Wheatley AK, Juno JA, et al. (May 2021). «Neutralizing antibody levels are highly predictive of immune protection from symptomatic SARS-CoV-2 infection». Nature Medicine. 27 (7): 1205–1211. doi:10.1038/s41591-021-01377-8. ISSN 1546-170X. PMID 34002089. S2CID 234769053.
- ^ a b González S, Olszevicki S, Salazar M, Calabria A, Regairaz L, Marín L, et al. (1 October 2021). «Effectiveness of the first component of Gam-COVID-Vac (Sputnik V) on reduction of SARS-CoV-2 confirmed infections, hospitalisations and mortality in patients aged 60-79: a retrospective cohort study in Argentina». EClinicalMedicine. 40: 101126. doi:10.1016/j.eclinm.2021.101126. ISSN 2589-5370. PMC 8435263. PMID 34541480.
- ^ a b «Single dose vaccine, Sputnik Light, authorized for use in Russia» (Press release). Russian Direct Investment Fund. 6 May 2021. Retrieved 29 June 2021.
The single dose Sputnik Light vaccine demonstrated 79.4% efficacy according to analyzed data taken from 28 days after the injection was administered as part of Russia’s mass vaccination program between 5 December 2020 and 15 April 2021.
- ^ a b Clinical trial number NCT04741061 for «Study to Evaluate Efficacy, Immunogenicity and Safety of the Sputnik-Light (SPUTNIK-LIGHT)» at ClinicalTrials.gov
- ^ Dolzhikova IV, Gushchin VA, Shcheblyakov DV, Tsybin AN, Shchetinin AM, Pochtovyi AA, et al. (14 October 2021). «One-shot immunization with Sputnik Light (the first component of Sputnik V vaccine) is effective against SARS-CoV-2 Delta variant: efficacy data on the use of the vaccine in civil circulation in Moscow» (Preprint). doi:10.1101/2021.10.08.21264715. S2CID 238747906 – via medRxiv.
- ^ Clinical trial number NCT04713488 for «An Open Study on the Safety, Tolerability, and Immunogenicity of «Sputnik Light» Vaccine» at ClinicalTrials.gov
- ^ «Combination of the first component of Sputnik V vaccine (Sputnik Light vaccine) with vaccines by AstraZeneca, Sinopharm and Moderna demonstrates high safety profile during the study in Argentina’s Buenos-Aires province» (Press release). Moscow: Russian Direct Investment Fund. 4 August 2021. Retrieved 5 August 2021.
- ^ «Moscow Plays Up Donbas As Part Of The Ukraine Conflict». Warsaw Institute. 30 July 2021. Retrieved 4 August 2021.
- ^ «Residents of ORDLO can become ‘guinea pigs’ for Russian pharmacists — Defense Ministry». Interfax Ukraine. Retrieved 4 August 2021.
{{cite web}}: CS1 maint: url-status (link)
Спутник Лайт — инструкция по применению
Синонимы, аналоги
Статьи
Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-СoV-2
▼ Данный лекарственный препарат зарегистрирован по процедуре регистрации препаратов, предназначенных для применения в условиях угрозы возникновения, возникновения и ликвидации чрезвычайных ситуаций. Инструкция подготовлена на основании ограниченного объема клинических данных по применению препарата и будет дополняться по мере поступления новых данных. Применение препарата возможно только в условиях медицинских организаций, имеющих право осуществлять вакцинопрофилактику населения в установленном порядке.
Регистрационный номер:
ЛП-006993
Торговое наименование:
Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
Международное непатентованное или группировочное наименование:
Вакцина для профилактики COVID-19
Лекарственная форма:
раствор для внутримышечного введения
Состав на 1 дозу (0,5 мл):
Действующее вещество: рекомбинантные аденовирусные частицы 26 серотипа, содержащие ген белка S вируса SARS-CoV-2, в количестве (1,0±0,5)×1011 частиц/доза.
Вспомогательные вещества: трис(гидроксиметил)аминометан – 1,21 мг, натрия хлорид – 2,19 мг, сахароза – 25,0 мг, полисорбат 80 – 250 мкг, магния хлорида гексагидрат – 102,0 мкг, ЭДТА динатриевая соль дигидрат – 19,0 мкг, этанол 95 % – 2,5 мкл, вода для инъекций – до 0,5 мл.
Описание
Замороженный препарат.
Раствор замороженный – плотная затвердевшая беловатого цвета масса. После размораживания – однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Жидкий препарат.
Однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Характеристика
Вакцина получена биотехнологическим путем, при котором не используется патогенный для человека вирус SARS-CoV-2. В состав препарата входит рекомбинантный аденовирусный вектор на основе аденовируса человека 26 серотипа, несущий ген белка S вируса SARS-CoV-2.
Фармакотерапевтическая группа:
МИБП-вакцина
Код АТХ:
J07B
Фармакологические свойства
Вакцина индуцирует формирование гуморального и клеточного иммунитета в отношении коронавирусной инфекции, вызываемой вирусом SARS-CoV-2.
Иммунологическая эффективность
Иммунологические свойства и безопасность вакцины изучали в различных клинических исследованиях у взрослых добровольцев обоего пола в возрасте старше 18 лет. Промежуточный анализ иммуногенности показал, что вакцина формирует гуморальный иммунный ответ у добровольцев. На 28 день сероконверсия обнаружена у 96,88% здоровых добровольцев.
У лиц с предсуществующим иммунитетом к коронавирусу отмечен выраженный рост титра антител на 10 день после вакцинации, что может указывать на возможность применения препарата для вакцинации ранее переболевших COVID-19 после снижения титра антител с целью предотвращения повторных случаев заболевания.
В результате однократной иммунизации 100% здоровых добровольцев (все 30 человек у которых изучены показатели клеточного иммунитета) сформировали клеточный иммунный ответ против S белка SARS-Cov2.
Защитный титр антител в настоящее время неизвестен. Продолжительность защиты неизвестна.
Показания к применению
Профилактика новой коронавирусной инфекции (COVID-19) у взрослых от 18 до 60 лет.
Противопоказания
- гиперчувствительность к какому-либо компоненту вакцины или вакцине, содержащей аналогичные компоненты;
- тяжелые аллергические реакции в анамнезе;
- острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний – вакцинацию проводят через 2-4 недели после выздоровления или ремиссии. При нетяжелых ОРВИ, острых инфекционных заболеваниях ЖКТ-вакцинацию проводят после нормализации температуры;
- беременность и период грудного вскармливания;
- возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности).
С осторожностью
Применять вакцину с осторожностью при хронических заболеваниях печени и почек, эндокринных заболеваниях (выраженных нарушениях функции щитовидной железы и сахарном диабете в стадии декомпенсации), тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваниях ЦНС, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах.
Вследствие недостатка информации вакцинация может представлять риск для следующих групп пациентов:
- с аутоиммунными заболеваниями (стимуляция иммунной системы может привести к обострению заболевания, особенно следует с осторожностью относиться к пациентам с аутоиммунной патологией, имеющей тенденцию к развитию тяжёлых и жизнеугрожающих состояний);
- со злокачественными новообразованиями.
Принятие решения о вакцинации должно основываться на оценке соотношения пользы и риска в каждой конкретной ситуации.
Применение при беременности и в период грудного вскармливания
Препарат противопоказан при беременности и в период грудного вскармливания, так как его эффективность и безопасность в этот период не изучались.
Способ применения и дозы
Вакцина предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата. Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча). При невозможности введения в дельтовидную мышцу – препарат вводят в латеральную широкую мышцу бедра.
После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 минут.
Замороженный препарат
Перед вакцинированием флакон, ампулу или шприц с препаратом достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон, ампулу или шприц снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона, ампулы или шприца!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой. Вскрывают ампулу по кольцу и/или точке излома. Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту из ампулы или флакона.
Внимание! Доза, вводимая пациенту, не должна превышать 0,5 мл!
Препарат в шприцах готов к применению без дополнительных манипуляций.
Применение вакцины производства ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России) (флаконы) и АО «Биннофарм» (ампулы, шприцы):
Не допускается хранение размороженного препарата более 30 минут!
Повторное замораживание не допускается!
Применение вакцины производства АО «ГЕНЕРИУМ» (флаконы), ОАО «Фармстандарт-УфаВИТА» (флаконы, ампулы), ЗАО «ЛЕККО» (флаконы):
Внимание! Повторное замораживание флакона или ампулы с раствором не допускается!
Суммарное время хранения размороженного раствора при комнатной температуре не должно превышать 2 часов. Неиспользованная вакцина подлежит уничтожению.
Многодозовые флаконы
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого или невскрытого флакона не более 2 часов при комнатной температуре.
Многодозовые ампулы
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение вакцины при комнатной температуре: вскрытой ампулы, закрытой стерильной салфеткой, не более 1 часа, невскрытой ампулы – не более 2 часов.
ВНИМАНИЕ! Одна ампула содержит две дозы вакцины. Объем одной дозы составляет 0,5 мл. Одному пациенту вводить 1 дозу (0,5 мл).
Однодозовые ампулы
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение невскрытой ампулы при комнатной температуре не более 2 часов.
Применение вакцины производства ЗАО «БИОКАД» (флаконы), АО «Р-Фарм» (флаконы):
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона по 3 мл не более 2 часов при комнатной температуре.
Не допускается хранение размороженного препарата во флаконах по 0,5 мл более 30 минут!
Повторное замораживание не допускается!
Жидкий препарат
Применение вакцины производства ООО «БиоИнтегратор» (флаконы):
Внимание! Замораживание флакона с раствором не допускается!
Флакон достают из холодильника и выдерживают при комнатной температуре, допускается слегка нагреть препарат, например, подержав его в руках. Не следует нагревать препарат выше 37 °С.
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту.
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона или ампулы не более 2 часов при комнатной температуре.
Внимание! К использованию непригоден препарат (жидкий и/или замороженный) с дефектами укупорочной системы и/или нарушенной маркировкой флакона или ампулы,, при изменении физических свойств раствора (мутность, окрашивание), неправильном хранении и/или с истекшим сроком годности.
▼ Информация для медицинских работников, выполняющих вакцинацию лекарственным препаратом: данный лекарственный препарат зарегистрирован по особой процедуре регистрации, в связи с чем необходимо уведомлять Федеральную службу по надзору в сфере здравоохранения о каждом факте применения лекарственного препарата путем внесения информации в соответствующий раздел информационной системы ЕГИСЗ.
Побочное действие
Нежелательные явления, характерные для применения вакцины, выявленные в рамках клинических исследований, а также исследований других вакцин на основе аналогичной технологической платформы, бывают преимущественно легкой или средней степени выраженности, могут развиваться в первые-вторые сутки после вакцинации и разрешаются в течение 3-х последующих дней. Часто и очень часто могут развиться кратковременные общие (непродолжительный гриппоподобный синдром, характеризующийся ознобом, повышением температуры тела, артралгией, миалгией, астенией, общим недомоганием, головной болью) и местные (болезненность в месте инъекции, гиперемия, отечность) реакции. Рекомендуется назначение нестероидных противовоспалительных средств (НПВС) при повышении температуры после вакцинации и антигистаминных средств при выраженной местной реакции.
Нежелательные явления, представленные ниже, перечислены по системам организма и в соответствии с частотой встречаемости. Частота встречаемости определяется следующим образом: очень часто (≥1/10), часто (≥1/100 и < /10), нечасто (≥1/1000 и <1/100), редко (≥1/10000 и <1/1000), очень редко (<1/10000, включая отдельные случаи). Категории частоты были сформированы на основании клинических исследований препарата.
Часто отмечаются: тошнота, диспепсия, снижение аппетита, очень редко – увеличение регионарных лимфоузлов. У некоторых пациентов возможно развитие аллергических реакций, кратковременное повышение уровня печеночных трансаминаз, креатинина и креатинфосфокиназы в сыворотке крови.
В рамках проведенных клинических исследований безопасности, переносимости и иммуногенности препарата «Спутник-Лайт» после вакцинации были зарегистрированы следующие НЯ:
«Общие нарушения и реакции в месте введения»: гипертермия, боль, отек, зуд в месте вакцинации, астения, боль, недомогание, пирексия, повышение температуры кожи в месте вакцинации, снижение аппетита. Частота развития – очень часто и часто.
«Нарушения со стороны дыхательной системы, органов грудной клетки и средостения»: боль в ротоглотке, заложенность носа, першение в горле, ринорея. Частота развития – часто.
«Нарушения со стороны нервной системы»: головная боль, астения – часто; головокружения, обмороки – редко.
«Желудочно-кишечные нарушения»: тошнота, рвота, диспепсия – часто.
«Лабораторные и инструментальные данные»: разнонаправленные отклонения показателей иммунологического статуса: повышение числа Т-лимфоцитов, увеличение процентного содержания лимфоцитов, снижение числа естественных клеток-киллеров, увеличение количества CD4-лимфоцитов, снижение количества CD4-лимфоцитов, повышение числа B-лимфоцитов, снижение числа B-лимфоцитов, повышение числа естественных клеток-киллеров, повышение количества CD8-лимфоцитов, повышение уровня иммуноглобулина Е (IgE) в крови, увеличение соотношения CD4/CD8, уменьшение соотношения CD4/CD8, повышение уровня иммуноглобулина A (IgA) в крови, уменьшение процентного содержания лимфоцитов CD8. Отклонения в общем анализе крови: увеличение процентного содержания лимфоцитов, снижение показателя гематокрита, увеличение числа лимфоцитов, повышение скорости оседания эритроцитов, повышение числа лейкоцитов, повышение числа моноцитов, повышение числа тромбоцитов, снижение числа нейтрофилов, снижение числа тромбоцитов. Отклонения в общем анализе мочи: эритроциты в моче.
Большинство НЯ завершились выздоровлением без последствий. Лабораторные отклонения не имели клинического значения (не нуждались в проведении дополнительных диагностических процедур и назначении терапии).
Передозировка
О случаях передозировки не сообщалось.
Учитывая, что отпуск лекарственного препарата допускается только для лечебно-профилактических учреждений, а сама вакцинация проводится только квалифицированным медицинским персоналом, риск передозировки крайне низок.
Однако можно предположить, что при случайной передозировке возможно развитие указанных выше токсических и токсико-аллергических реакций в более тяжелой степени.
Специфических антидотов к препарату не существует.
Терапевтические мероприятия в данном случае будут включать симптоматическую терапию в соответствии с показаниями (кортикостероиды, жаропонижающие/ НПВС и десенсибилизирующие средства). Режим назначения препаратов должен быть выбран согласно рекомендациям по применению и дозировкам данного лекарственного средства.
Взаимодействие с другими лекарственными средствами
Не изучалось.
Особые указания
У пациентов, получающих иммуносупрессивную терапию, и пациентов с иммунодефицитом может не развиться достаточный иммунный ответ. Поэтому прием препаратов, угнетающих функцию иммунной системы, противопоказан в течение, как минимум, 1 месяца до и после вакцинации из-за риска снижения иммуногенности. Принять решение о возможности отмены иммуносупрессивной терапии может только лечащий врач!
Подобно остальным вакцинам, защитный иммунный ответ может возникать не у всех вакцинируемых лиц.
Влияние на способность управлять транспортными средствами, механизмами
Исследования по изучению влияния вакцины на способность управлять транспортными средствами и потенциально опасными механизмами не проводились.
Форма выпуска
Раствор для внутримышечного введения, 0,5 мл/доза.
Замороженный препарат
При производстве ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России):
по 0,5 мл (1 доза) препарата – во флаконы, укупоренные пробками из резины, обжатые алюминиевыми или алюмопластиковыми колпачками.
1 флакон препарата с инструкцией по применению в пачку картонную или в пачку из картона коробочного.
При производстве АО «Биннофарм»:
по 0,5 мл (1 доза) препарата – в ампулы из бесцветного стекла с точкой излома или в стерильном одноразовом шприце.
По 5 ампул препарата в контурную ячейковую упаковку из пленки поливинилхлоридной, или по 1 или 3 шприца с препаратом помещают в контурную ячейковую упаковку из пленки поливинилхлоридной, покрытую пленкой полиэтиленовой, или без покрытия.
По 1 контурной ячейковой упаковке вместе с инструкцией по применению в пачку из картона.
При производстве на АО «ГЕНЕРИУМ»:
по 3,0 мл (5 доз) препарата – во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
1 флакон препарата вместе с инструкцией по медицинскому применению – в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ЗАО «ЛЕККО»:
по 3 мл (5 доз) препарата – во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
По 1 флакону вместе с инструкцией по применению – в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ОАО «Фармстандарт-УфаВИТА»:
по 0,5 мл (1 доза) или по 1,0 мл (2 дозы) препарата в ампулы из бесцветного стекла.
По 5 ампул помещают в контурную ячейковую упаковку из пленки поливинилхлоридной.
По 1 или 2 контурные ячейковые упаковки вместе с инструкцией по применению – в пачку из картона.
По 3 мл (5 доз) препарата – во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
По 1 флакону вместе с инструкцией по применению в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ЗАО «БИОКАД»:
по 0,5 мл (1 доза) или по 3,0 мл (5 доз) препарата во флаконы из нейтрального стекла I гидролитического класса (типа 2R, 6R), герметично укупоренные резиновыми пробками, с обкаткой алюминиевыми колпачками с пластиковой крышкой типа «flip-off».
На флаконы препарата наклеивают этикетку самоклеящуюся.
1 флакон 6R препарата с инструкцией по применению в пачку картонную.
1 флакон 2R препарата в контурной ячейковой упаковке из ПВХ пленки с инструкцией по применению в пачку картонную.
При производстве на АО «Р-Фарм»:
по 0,5 мл (1 доза) препарата во флаконы, герметично укупоренные пробками из резины и обжатые алюмопластиковыми колпачками.
По 1, 2, 5 или 10 флаконов вместе с инструкцией по применению в пачку из картона.
Жидкий препарат
При производстве на ООО «БиоИнтегратор»:
по 0,5 мл (1 доза) препарата – во флаконы, укупоренные пробками из резины, обжатые алюминиевыми или алюмопластиковыми колпачками.
1 флакон препарата с инструкцией по применению в пачку картонную или в пачку из картона коробочного.
Условия хранения
Замороженный препарат
Хранить в защищенном от света месте, при температуре не выше минус 18 °С. Повторное замораживание не допускается.
Хранить в недоступном для детей месте.
Жидкий препарат
Хранить в защищенном от света месте, при температуре от 2 до 8 °С. Не замораживать.
Хранить в недоступном для детей месте.
Условия транспортирования
Замороженный препарат
Транспортирование препарата при температуре не выше минус 18 °С.
Жидкий препарат
Транспортирование препарата при температуре от 2 до 8 °С. Не замораживать.
Срок годности
Замороженный препарат
6 месяцев. Не применять по истечении срока годности.
Жидкий препарат
1 месяц. Не применять по истечении срока годности.
Условия отпуска:
для лечебно-профилактических учреждений.
Производитель
Наименования и адреса производственных площадок производителя лекарственного препарата:
1) ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия, 123098, г. Москва, улица Гамалеи, д. 18 (все стадии производства).
2) АО «Р-Фарм», Россия, 150061, Ярославская обл., г.о. г. Ярославль, г. Ярославль, ул. Громова, д. 15 (производство готовой формы, первичная и вторичная (потребительская) упаковка).
3) АО «Биннофарм», Россия, 124460, г. Москва, г. Зеленоград, ул. Конструктора Гуськова, д. 3, стр. 1 (производство готовой формы, первичная и вторичная (потребительская) упаковка).
4) ЗАО «БИОКАД», Россия, 198515, г. Санкт-Петербург, п. Стрельна, ул. Связи, д. 38, стр. 1 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
5) АО «ГЕНЕРИУМ», Россия, 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 263 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
6) ЗАО «ЛЕККО», Россия, 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 277; 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 279 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
7) ОАО «Фармстандарт-УфаВИТА», Россия, Республика Башкортостан, г. Уфа, ул. Худайбердина, д. 28 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).

Выпускающий контроль качества
ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России). Россия, 123098, г. Москва, улица Гамалеи, д. 18.
Владелец регистрационного удостоверения/организация, принимающая претензии потребителя:
ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия
Россия, 123098, г. Москва, улица Гамалеи, д. 18.
Спутник Лайт — цена, наличие в аптеках
Указана цена, по которой можно купить Спутник Лайт в Москве. Точную цену в Вашем городе Вы получите после перехода в службу онлайн заказа лекарств:
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
| Вакцина | Цена |
|---|---|
|
|
2500 ₽ |
Вакцина «Спутник Лайт» защищает от инфекций:
Стоимость прививки Спутник Лайт в Москве составляет 2500 руб. В цену включён осмотр врача перед вакцинацией.
Похожие вакцины (аналоги Спутник Лайт):
Торговое наименование:
Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
Лекарственная форма:
раствор для внутримышечного введения
Состав на 1 дозу (0,5 мл):
Действующее вещество: рекомбинантные аденовирусные частицы 26 серотипа, содержащие ген белка S вируса SARS-CoV-2, в количестве (1,0±0,5)×1011 частиц/доза.
Вспомогательные вещества: трис(гидроксиметил)аминометан – 1,21 мг, натрия хлорид – 2,19 мг, сахароза – 25,0 мг, полисорбат 80 – 250 мкг, магния хлорида гексагидрат – 102,0 мкг, ЭДТА динатриевая соль дигидрат – 19,0 мкг, этанол 95 % – 2,5 мкл, вода для инъекций – до 0,5 мл.
Описание
Замороженный препарат.
Раствор замороженный – плотная затвердевшая беловатого цвета масса. После размораживания – однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Жидкий препарат.
Однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Характеристика
Вакцина получена биотехнологическим путем, при котором не используется патогенный для человека вирус SARS-CoV-2. В состав препарата входит рекомбинантный аденовирусный вектор на основе аденовируса человека 26 серотипа, несущий ген белка S вируса SARS-CoV-2.
Фармакотерапевтическая группа:
МИБП-вакцина
Код АТХ:
J07B
Фармакологические свойства
Новая редакция от 19 августа 2021 года.
Вакцина индуцирует формирование гуморального и клеточного иммунитета в отношении коронавирусной инфекции, вызываемой вирусом SARS-CoV-2.
Иммунологическая эффективность
Иммунологические свойства и безопасность вакцины изучали в различных клинических исследованиях у взрослых добровольцев обоего пола в возрасте старше 18 лет. Промежуточный анализ иммуногенности показал, что вакцина формирует гуморальный иммунный ответ у добровольцев. На 28 день сероконверсия обнаружена у 96,88% здоровых добровольцев.
У лиц с предсуществующим иммунитетом к коронавирусу отмечен выраженный рост титра антител на 10 день после вакцинации, что может указывать на возможность применения препарата для вакцинации ранее переболевших COVID-19 после снижения титра антител с целью предотвращения повторных случаев заболевания.
С учетом рекомендаций Всемирной организации здравоохранения для достижения уровня коллектннного иммунитета населения, следует проводить вакцинацию против новой коронавирусной инфекции COVID- 19 по эпидемическим показаниям спустя 6 месяцев после перенесенного заболевания (в том числе у ранее вакцинированных лиц) или спустя 6 месяцев после предыдущей первичной вакцинации.
В результате однократной иммунизации 100% здоровых добровольцев (все 30 человек у которых изучены показатели клеточного иммунитета) сформировали клеточный иммунный ответ против S белка SARS-Cov2.
Защитный титр антител в настоящее время неизвестен. Продолжительность защиты неизвестна.
Показания к применению
Новая редакция от 19 августа 2021 года.
Профилактика новой коронавирусной инфекции (COVID-19) у взрослых старше 18 лет.
Противопоказания
- гиперчувствительность к какому-либо компоненту вакцины или вакцине, содержащей аналогичные компоненты;
- тяжелые аллергические реакции в анамнезе;
- острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний – вакцинацию проводят через 2-4 недели после выздоровления или ремиссии. При нетяжелых ОРВИ, острых инфекционных заболеваниях ЖКТ-вакцинацию проводят после нормализации температуры;
- беременность и период грудного вскармливания;
- возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности).
С осторожностью
Новая редакция от 19 августа 2021 года.
Применять вакцину с осторожностью при хронических заболеваниях печени и почек, эндокринных заболеваниях (выраженных нарушениях функции щитовидной железы и сахарном диабете в стадии декомпенсации), тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваниях ЦНС, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах.
Вследствие недостатка информации вакцинация может представлять риск для следующих групп пациентов:
- с аутоиммунными заболеваниями (стимуляция иммунной системы может привести к обострению заболевания, особенно следует с осторожностью относиться к пациентам с аутоиммунной патологией, имеющей тенденцию к развитию тяжёлых и жизнеугрожающих состояний);
- со злокачественными новообразованиями.
Категориям населения старше 60 лет, ранее не прошедшим иммунизацию от COVID-19, и не болевшим COVID-19, иммунокомпрометированным лицам независимо от возраста, для формирования иммунитета не рекомендовано применение препарата Спутник Лайт в связи со снижением функции иммунной системы, для формирования иммунного ответа показана вакцинация двухкомпонентной вакциной Гам-Ковид-Вак.
Принятие решения о вакцинации должно основываться на оценке соотношения пользы и риска в каждой конкретной ситуации.
Применение при беременности и в период грудного вскармливания
Препарат противопоказан при беременности и в период грудного вскармливания, так как его эффективность и безопасность в этот период не изучались.
Способ применения и дозы
Вакцина предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата. Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча). При невозможности введения в дельтовидную мышцу – препарат вводят в латеральную широкую мышцу бедра.
После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 минут.
Замороженный препарат
Перед вакцинированием флакон, ампулу или шприц с препаратом достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон, ампулу или шприц снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона, ампулы или шприца!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой. Вскрывают ампулу по кольцу и/или точке излома. Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту из ампулы или флакона.
Внимание! Доза, вводимая пациенту, не должна превышать 0,5 мл!
Препарат в шприцах готов к применению без дополнительных манипуляций.
Применение вакцины производства ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России) (флаконы) и АО «Биннофарм» (ампулы, шприцы):
Не допускается хранение размороженного препарата более 30 минут!
Повторное замораживание не допускается!
Применение вакцины производства АО «ГЕНЕРИУМ» (флаконы), ОАО «Фармстандарт-УфаВИТА» (флаконы, ампулы), ЗАО «ЛЕККО» (флаконы):
Внимание! Повторное замораживание флакона или ампулы с раствором не допускается!
Суммарное время хранения размороженного раствора при комнатной температуре не должно превышать 2 часов. Неиспользованная вакцина подлежит уничтожению.
Многодозовые флаконы
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого или невскрытого флакона не более 2 часов при комнатной температуре.
Многодозовые ампулы
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение вакцины при комнатной температуре: вскрытой ампулы, закрытой стерильной салфеткой, не более 1 часа, невскрытой ампулы – не более 2 часов.
ВНИМАНИЕ! Одна ампула содержит две дозы вакцины. Объем одной дозы составляет 0,5 мл. Одному пациенту вводить 1 дозу (0,5 мл).
Однодозовые ампулы
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение невскрытой ампулы при комнатной температуре не более 2 часов.
Применение вакцины производства ЗАО «БИОКАД» (флаконы), АО «Р-Фарм» (флаконы):
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона по 3 мл не более 2 часов при комнатной температуре.
Не допускается хранение размороженного препарата во флаконах по 0,5 мл более 30 минут!
Повторное замораживание не допускается!
Жидкий препарат
Применение вакцины производства ООО «БиоИнтегратор» (флаконы):
Внимание! Замораживание флакона с раствором не допускается!
Флакон достают из холодильника и выдерживают при комнатной температуре, допускается слегка нагреть препарат, например, подержав его в руках. Не следует нагревать препарат выше 37 °С.
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту.
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона или ампулы не более 2 часов при комнатной температуре.
Внимание! К использованию непригоден препарат (жидкий и/или замороженный) с дефектами укупорочной системы и/или нарушенной маркировкой флакона или ампулы,, при изменении физических свойств раствора (мутность, окрашивание), неправильном хранении и/или с истекшим сроком годности.
Информация для медицинских работников, выполняющих вакцинацию лекарственным препаратом: данный лекарственный препарат зарегистрирован по особой процедуре регистрации, в связи с чем необходимо уведомлять Федеральную службу по надзору в сфере здравоохранения о каждом факте применения лекарственного препарата путем внесения информации в соответствующий раздел информационной системы ЕГИСЗ.
Побочное действие
Нежелательные явления, характерные для применения вакцины, выявленные в рамках клинических исследований, а также исследований других вакцин на основе аналогичной технологической платформы, бывают преимущественно легкой или средней степени выраженности, могут развиваться в первые-вторые сутки после вакцинации и разрешаются в течение 3-х последующих дней. Часто и очень часто могут развиться кратковременные общие (непродолжительный гриппоподобный синдром, характеризующийся ознобом, повышением температуры тела, артралгией, миалгией, астенией, общим недомоганием, головной болью) и местные (болезненность в месте инъекции, гиперемия, отечность) реакции. Рекомендуется назначение нестероидных противовоспалительных средств (НПВС) при повышении температуры после вакцинации и антигистаминных средств при выраженной местной реакции.
Нежелательные явления, представленные ниже, перечислены по системам организма и в соответствии с частотой встречаемости. Частота встречаемости определяется следующим образом: очень часто (≥1/10), часто (≥1/100 и < /10), нечасто (≥1/1000 и <1/100), редко (≥1/10000 и <1/1000), очень редко (<1/10000, включая отдельные случаи). Категории частоты были сформированы на основании клинических исследований препарата.
Часто отмечаются: тошнота, диспепсия, снижение аппетита, очень редко – увеличение регионарных лимфоузлов. У некоторых пациентов возможно развитие аллергических реакций, кратковременное повышение уровня печеночных трансаминаз, креатинина и креатинфосфокиназы в сыворотке крови.
В рамках проведенных клинических исследований безопасности, переносимости и иммуногенности препарата «Спутник-Лайт» после вакцинации были зарегистрированы следующие НЯ:
«Общие нарушения и реакции в месте введения»: гипертермия, боль, отек, зуд в месте вакцинации, астения, боль, недомогание, пирексия, повышение температуры кожи в месте вакцинации, снижение аппетита. Частота развития – очень часто и часто.
«Нарушения со стороны дыхательной системы, органов грудной клетки и средостения»: боль в ротоглотке, заложенность носа, першение в горле, ринорея. Частота развития – часто.
«Нарушения со стороны нервной системы»: головная боль, астения – часто; головокружения, обмороки – редко.
«Желудочно-кишечные нарушения»: тошнота, рвота, диспепсия – часто.
«Лабораторные и инструментальные данные»: разнонаправленные отклонения показателей иммунологического статуса: повышение числа Т-лимфоцитов, увеличение процентного содержания лимфоцитов, снижение числа естественных клеток-киллеров, увеличение количества CD4-лимфоцитов, снижение количества CD4-лимфоцитов, повышение числа B-лимфоцитов, снижение числа B-лимфоцитов, повышение числа естественных клеток-киллеров, повышение количества CD8-лимфоцитов, повышение уровня иммуноглобулина Е (IgE) в крови, увеличение соотношения CD4/CD8, уменьшение соотношения CD4/CD8, повышение уровня иммуноглобулина A (IgA) в крови, уменьшение процентного содержания лимфоцитов CD8. Отклонения в общем анализе крови: увеличение процентного содержания лимфоцитов, снижение показателя гематокрита, увеличение числа лимфоцитов, повышение скорости оседания эритроцитов, повышение числа лейкоцитов, повышение числа моноцитов, повышение числа тромбоцитов, снижение числа нейтрофилов, снижение числа тромбоцитов. Отклонения в общем анализе мочи: эритроциты в моче.
Большинство НЯ завершились выздоровлением без последствий. Лабораторные отклонения не имели клинического значения (не нуждались в проведении дополнительных диагностических процедур и назначении терапии).
Передозировка
О случаях передозировки не сообщалось.
Учитывая, что отпуск лекарственного препарата допускается только для лечебно-профилактических учреждений, а сама вакцинация проводится только квалифицированным медицинским персоналом, риск передозировки крайне низок.
Однако можно предположить, что при случайной передозировке возможно развитие указанных выше токсических и токсико-аллергических реакций в более тяжелой степени.
Специфических антидотов к препарату не существует.
Терапевтические мероприятия в данном случае будут включать симптоматическую терапию в соответствии с показаниями (кортикостероиды, жаропонижающие/ НПВС и десенсибилизирующие средства). Режим назначения препаратов должен быть выбран согласно рекомендациям по применению и дозировкам данного лекарственного средства.
Взаимодействие с другими лекарственными средствами
Не изучалось.
Особые указания
У пациентов, получающих иммуносупрессивную терапию, и пациентов с иммунодефицитом может не развиться достаточный иммунный ответ. Поэтому прием препаратов, угнетающих функцию иммунной системы, противопоказан в течение, как минимум, 1 месяца до и после вакцинации из-за риска снижения иммуногенности. Принять решение о возможности отмены иммуносупрессивной терапии может только лечащий врач!
Подобно остальным вакцинам, защитный иммунный ответ может возникать не у всех вакцинируемых лиц.
Влияние на способность управлять транспортными средствами, механизмами
Исследования по изучению влияния вакцины на способность управлять транспортными средствами и потенциально опасными механизмами не проводились.
Форма выпуска
Раствор для внутримышечного введения, 0,5 мл/доза.
Замороженный препарат
При производстве ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России):
по 0,5 мл (1 доза) препарата – во флаконы, укупоренные пробками из резины, обжатые алюминиевыми или алюмопластиковыми колпачками.
1 флакон препарата с инструкцией по применению в пачку картонную или в пачку из картона коробочного.
При производстве АО «Биннофарм»:
по 0,5 мл (1 доза) препарата – в ампулы из бесцветного стекла с точкой излома или в стерильном одноразовом шприце.
По 5 ампул препарата в контурную ячейковую упаковку из пленки поливинилхлоридной, или по 1 или 3 шприца с препаратом помещают в контурную ячейковую упаковку из пленки поливинилхлоридной, покрытую пленкой полиэтиленовой, или без покрытия.
По 1 контурной ячейковой упаковке вместе с инструкцией по применению в пачку из картона.
При производстве на АО «ГЕНЕРИУМ»:
по 3,0 мл (5 доз) препарата – во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
1 флакон препарата вместе с инструкцией по медицинскому применению – в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ЗАО «ЛЕККО»:
по 3 мл (5 доз) препарата – во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
По 1 флакону вместе с инструкцией по применению – в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ОАО «Фармстандарт-УфаВИТА»:
по 0,5 мл (1 доза) или по 1,0 мл (2 дозы) препарата в ампулы из бесцветного стекла.
По 5 ампул помещают в контурную ячейковую упаковку из пленки поливинилхлоридной.
По 1 или 2 контурные ячейковые упаковки вместе с инструкцией по применению – в пачку из картона.
По 3 мл (5 доз) препарата – во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
По 1 флакону вместе с инструкцией по применению в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ЗАО «БИОКАД»:
по 0,5 мл (1 доза) или по 3,0 мл (5 доз) препарата во флаконы из нейтрального стекла I гидролитического класса (типа 2R, 6R), герметично укупоренные резиновыми пробками, с обкаткой алюминиевыми колпачками с пластиковой крышкой типа «flip-off».
На флаконы препарата наклеивают этикетку самоклеящуюся.
1 флакон 6R препарата с инструкцией по применению в пачку картонную.
1 флакон 2R препарата в контурной ячейковой упаковке из ПВХ пленки с инструкцией по применению в пачку картонную.
При производстве на АО «Р-Фарм»:
по 0,5 мл (1 доза) препарата во флаконы, герметично укупоренные пробками из резины и обжатые алюмопластиковыми колпачками.
По 1, 2, 5 или 10 флаконов вместе с инструкцией по применению в пачку из картона.
Жидкий препарат
При производстве на ООО «БиоИнтегратор»:
по 0,5 мл (1 доза) препарата – во флаконы, укупоренные пробками из резины, обжатые алюминиевыми или алюмопластиковыми колпачками.
1 флакон препарата с инструкцией по применению в пачку картонную или в пачку из картона коробочного.
Условия хранения
Замороженный препарат
Хранить в защищенном от света месте, при температуре не выше минус 18 °С. Повторное замораживание не допускается.
Хранить в недоступном для детей месте.
Жидкий препарат
Хранить в защищенном от света месте, при температуре от 2 до 8 °С. Не замораживать.
Хранить в недоступном для детей месте.
Условия транспортирования
Замороженный препарат
Транспортирование препарата при температуре не выше минус 18 °С.
Жидкий препарат
Транспортирование препарата при температуре от 2 до 8 °С. Не замораживать.
Срок годности
Замороженный препарат
6 месяцев. Не применять по истечении срока годности.
Жидкий препарат
1 месяц. Не применять по истечении срока годности.
Условия отпуска:
для лечебно-профилактических учреждений.
Производитель
Наименования и адреса производственных площадок производителя лекарственного препарата:
1) ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия, 123098, г. Москва, улица Гамалеи, д. 18 (все стадии производства).
2) АО «Р-Фарм», Россия, 150061, Ярославская обл., г.о. г. Ярославль, г. Ярославль, ул. Громова, д. 15 (производство готовой формы, первичная и вторичная (потребительская) упаковка).
3) АО «Биннофарм», Россия, 124460, г. Москва, г. Зеленоград, ул. Конструктора Гуськова, д. 3, стр. 1 (производство готовой формы, первичная и вторичная (потребительская) упаковка).
4) ЗАО «БИОКАД», Россия, 198515, г. Санкт-Петербург, п. Стрельна, ул. Связи, д. 38, стр. 1 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
5) АО «ГЕНЕРИУМ», Россия, 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 263 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
6) ЗАО «ЛЕККО», Россия, 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 277; 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 279 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
7) ОАО «Фармстандарт-УфаВИТА», Россия, Республика Башкортостан, г. Уфа, ул. Худайбердина, д. 28 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).

Выпускающий контроль качества
ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России). Россия, 123098, г. Москва, улица Гамалеи, д. 18.
Владелец регистрационного удостоверения/организация, принимающая претензии потребителя:
ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия
Россия, 123098, г. Москва, улица Гамалеи, д. 18.
Внимание руководителям организаций! Специалисты нашего центра выезжают для проведения коллективной вакцинации сотрудников вашей организации по Москве вакцинами от гриппа в сезон 2022/23.
Узнать наличие вакцины Спутник Лайт и записаться на прививку можно по телефонам центра:
«Диавакс» на Таганке
+7 (495) 988-47-76
+7 (916) 550-53-03
«Диавакс» на ВДНХ
+7 (495) 616-29-59
+7 (915) 351-92-53
Если хотите пригласить определённого специалиста, оставьте заявку и мы вам перезвоним!
Возможен выезд врача на дом и на предприятия для вакцинации сотрудников. Стоимость выезда врача – договорная. Услуги по проведению вакцинации оплачиваются отдельно в соответствии с действующим прейскурантом.
11 ноября 2021 года
Составить индивидуальный график вакцинации или получить грамотную консультацию специалиста теперь можно не выходя из дома, потому что мы заботимся о Вас, снижая количество контактов и экономя Ваше время!
Онлайн-консультация по вопросам вакцинопрофилактики
Специалистом центра «Диавакс» будет составлен Индивидуальный график вакцинации, прописаны последовательность и сроки вакцинации с перечнем всех необходимых вакцин, исходя из Вашей конкретной ситуации.
Онлайн-консультация по лечению и реабилитации после COVID-19
Врач центра «Диавакс» удалённо проконсультирует Вас или Вашего ребёнка по вопросам диагностики и лечения новой коронавирусной инфекции, помогут разобраться с анализами и обследованиями, расскажет о профилактике возможных осложнений, определит план реабилитации и ответит на вопросы о вакцинации против COVID-19.
А еще мы отвечаем на интересующие вас вопросы в специальном разделе! Чаще всего это вопросы индивидуального характера в отношении вакцинации, иммунитета и тому подобного.
На вопросы отвечают:
- Специалисты в области иммунопрофилактики
- Сотрудники Кафедры инфекционных болезней у детей РНИМУ им. Н.И. Пирогова
Автор:
30 марта 2021 13:29
«Основную свою функцию данный препарат может выполнить». Прививка «Спутник Лайт» — вакцина от коронавируса. Как она создавалась, какие исследования проходили. Можно ли привиться? «Спутник Лайт»: отличие от «Спутника V». Состав, принцип работы препарата. Иммунитет после «Спутника Лайт», сколько длится.

Вакцина «Спутник Лайт» — это «облегченная» версия первой российской вакцины от коронавируса «Спутник V». «Спутник Лайт» Минздрав России зарегистрировал 6 мая 2021 года. Fishki рассказывает о ее отличительных особенностях, создании, иммунитете и противопоказаниях.
Содержание
-
Что такое «Спутник Лайт»?
-
Состав и принцип работы
-
Иммунитет и его продолжительность
-
Можно ли привиться «Спутником Лайт»
-
Противопоказания
Что такое «Спутник Лайт»?
«Спутник Лайт» представляет собой первый из двух компонентов «Спутника V» — рекомбинантный аденовирусный вектор человека 26-го серотипа (rAd26).
Впервые о намерении ученых из Центра имени Гамалеи создать облегченный вариант вакцины сообщил в декабре прошлого года президент России Владимир Путин в ходе пресс-конференции. Глава государства тогда отметил, что вакцина будет отличаться не только количеством необходимых уколов, но и быстрой выработкой антител.
12 февраля 2021 года директор Центра имени Гамалеи и руководитель научной группы, создавшей «Спутник V», Александр Гинцбург заявил, что подходит к завершению вторая фаза клинических испытаний нового препарата, в которых приняли участие 150 добровольцев.

Пресс-служба НИИ эпидемиологии и микробиологии имени Гамалеи
Третья фаза испытаний с участием семи тысяч человек проходит в России, ОАЭ, Гане и других странах. Промежуточные данные ожидают в мае. Однако вакцину уже зарегистрировали.
Состав и принцип работы
Поскольку «Спутник Лайт» — это часть «Спутника V», он является векторной вакциной.
«Векторная вакцина — это вакцина, направленная на доставку. Например, на доставку нужного вам фрагмента белка, нуклеиновой кислоты, — рассказывает Александр Гинцбург, — Доставку же мы осуществляем с помощью своеобразного “контейнера”. Контейнером служит аденовирус.
Как это работает? Мы берем аденовирус — очень хорошо известный вирус, который с нами с самого рождения человечества, а возможно, еще с наших обезьяньих предков, и очень хорошо научился проникать в наши клетки. Потом из этого вируса удаляются все гены, ответственные за размножение.
Вместо этих генов вставляется любой другой ген. В данном случае нас интересует ген Spike-белка коронавируса».
Данная операция решает сразу две задачи. Во-первых, лишенный возможности размножаться вирус не несет угрозы организму. И во-вторых, добавленный в него материал позволяет организму выработать нужную реакцию — иммунитет.
Гинцбург отмечает, что сотрудники института Гамалеи абсолютно уверены в этой методике, потому что многократно испытывали ее раньше, «подсаживая» к аденовирусу фрагменты других заболеваний: эболы, MERS и т.д.
Иммунитет и его продолжительность
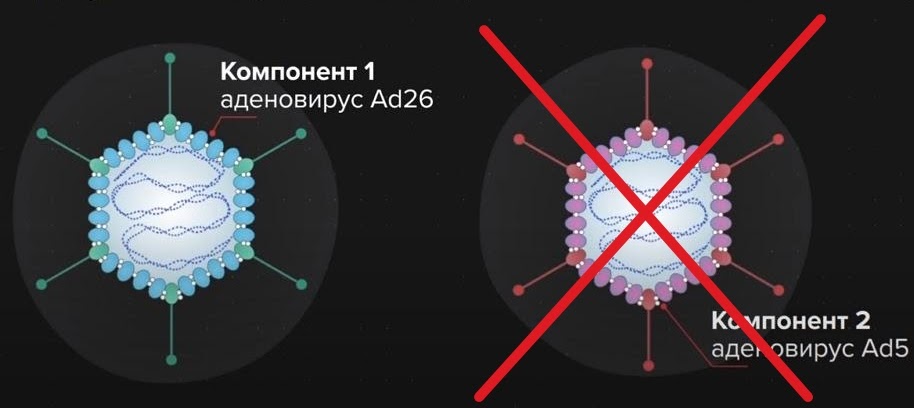
Главным отличием «облегченного» варианта от «Спутника V» является то, что «Спутник Лайт» комбинируется только с одним видом аденовируса — аденовирусом человека 26 типа, входящим в первый компонент «Спутника V». Аденовирус человека 5 типа, входящий во второй компонент, соответственно, не используется.
Соответственно, вакцина принимается организмом легче, так как содержит меньше чужеродного биологического материала. Она не требует двух инъекций, максимальный иммунитет образует через 3–4 недели, а не через 42 дня. Но так как отсутствует дополнительная нагрузка на организм в виде второго компонента, сам иммунитет также получается слабее.
«Эффективность <…> составила 79,4% с 28-го дня после получения иммунизации. Показатель эффективности на уровне около 80% превышает показатели эффективности многих вакцин, требующих двух уколов», — сообщил Российский фонд прямых инвестиций (РФПИ).
У «Спутника V» эффективность оценивается в 91,6%.
Кроме того, по итогам лабораторных исследований вакцина «Спутник Лайт» эффективна против всех новых штаммов коронавируса, серьезных нежелательных явлений после применения препарата не зарегистрировано, отметили в РФПИ.
Особенно ярка разница в продолжительности иммунитета. Гинцбург говорит, что «Спутник Лайт» дает защиту организму на 3–4 месяца, в то время как прогнозируемое время действия «Спутника V» — порядка двух лет.

Александр Гинцбург. Кадр RT
Нужно отметить, что иммунитет после вакцины отличается от иммунитета после болезни. Грубо говоря, у перенесших коронавирус иммунитет возникает ко всему ковиду. У вакцинированных же — иммунитет конкретно к Spike-белку, что не дает коронавирусу проникать в клетки.
Не нужно думать, что в данном случае «частичный» иммунитет хуже «общего». Все применяемые в мире вакцины формируют иммунитет именно к Spike-белку — эта схема доказала свою работоспособность.
Однако проблема была в том, что вакцинированные порой хотели самостоятельно проверить, сработала ли прививка, и сдавали стандартные тесты на антитела. Но стандартные тесты определяют иммунитет, образующийся после болезни, иммунитет же конкретно к Spike-белку ковида они не показывают, из-за чего среди людей начало распространяться ложное опасение о неэффективности вакцинации.
Можно ли привиться «Спутником Лайт»
Основным инструментом для вакцинации в России по-прежнему остается «Спутник V». «Спутник Лайт» будет производиться на экспорт, поскольку вакцина не требует специальных условий для хранения и логистики и обладает доступной ценой менее 10 долларов.
По словам Александра Гинцбурга, «Спутник Лайт» будет поставляться в небогатые страны с высокой плотностью населения и острой эпидемиологической ситуацией:
«Его использование дает возможность сбить пик заболеваемости, тем самым снизить нагрузку на местное здравоохранение, растянув эпидемический процесс во времени. Основную свою функцию, а именно — уменьшение количества тяжелых случаев и госпитализаций, данный препарат может выполнить».
С мая 2021 года препарат все же решили применять и на территории России.
Противопоказания
Поскольку «Спутник Лайт» структурно очень близок к «Спутнику V, противопоказания у этих вакцин также близки. К ним относятся:
- гиперчувствительность к какому-либо компоненту этой вакцины или вакцины, содержащей аналогичные компоненты;
- тяжелые аллергические реакции в анамнезе;
- острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний — вакцинацию проводят через 2–4 недели после выздоровления или ремиссии. При нетяжелых ОРВИ, острых инфекционных заболеваниях ЖКТ вакцинацию проводят после нормализации температуры;
- беременность и период грудного вскармливания;
- возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности).
Также противопоказаниями для введения компонента 2 являются тяжелые поствакцинальные осложнения (анафилактический шок, тяжелые генерализованные аллергические реакции, судорожный синдром, температура выше 40°C и т.д.) на введение компонента 1.
Кроме того, проходить вакцинацию с осторожностью рекомендуется при:
- хронических заболеваниях печени и почек, эндокринных заболеваниях;
- эпилепсии и других заболеваниях центральной нервной системы;
- тяжелых заболеваниях системы кроветворения;
- остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах;
- аутоимунных заболеваниях;
- злокачественных новообразованиях.
Новости партнёров
реклама
Вакцина «Спутник Лайт» появилась позже «Спутника V» и является его облегченной версией, не требует вторичного введения и обладает более мягким действием. В связи с этим вакцинацией препаратом «Спутник Лайт» заинтересовались многие граждане. Особенно те, кто хочет получить QR-код, но не желает долго ждать.
Однако всем ли подходит данная вакцина? Эффективнее ли она «Спутника V»? Нет ли дефицита этого препарата? Ответы на эти и другие вопросы читайте в нашей статье.
Для кого подходит «Спутник Лайт»?
Вакцина «Спутник Лайт» была зарегистрирована в мае 2021 года и поступила в гражданский оборот уже в июне. При выходе было анонсировано, что новая вакцина является первым компонентом »Спутника V» (данная вакцина, как известно, является двухфазной и состоит из двух компонентов, вводимых в организм с определенным временным промежутком). Она также создана на платформе аденовирусных векторов человека, и в принципе действия тоже лежит механизм транспортировки генетической информации коронавируса SARS-CoV-2.
Тогда же министр здравоохранения Михаил Мурашко заявил, что «Спутник Лайт» не является альтернативой «Спутнику V». Было отмечено, что «Спутник Лайт» предназначен для вакцинации уже переболевших пациентов и ревакцинации вакцинированных граждан от 18 до 60 лет.
В то же время глава Центра имени Гамалеи Александр Гинцбург отметил, что новый препарат — «хороший инструмент как для первоначальной вакцинации, так и для повышения эффективности действия ранее сделанных вакцин».
На сегодняшний день после успешного применения «Спутника Лайт» в течение почти полугода специалисты Минздрава и Роспотребнадзора утверждают, что данная вакцина с успехом может применяться в отношении переболевших пациентов, которые с течением времени уже утратили высокий титр антител, а также тех, кто уже прошел двухкомпонентную вакцинацию »Спутником V». Также изменен и верхний возрастной порог вакцинируемых пациентов.
Министр здравоохранения РФ Михаил Мурашко:
«Эксперты дали разрешение на использование вакцины „Спутник Лайт“ у пожилых лиц старше 60 лет. Она преимущественно используется для повторной вакцинации у тех, кто уже прошел вакцинацию».
Эффективна ли вакцина «Спутник Лайт»?
Что касается эффективности, то в ее высоких показателях разработчики вакцины не сомневаются. Вот какие данные приводит Российский фонд прямых инвестиций: «Эффективность однокомпонентной вакцины от коронавируса „Спутник Лайт“, которую разработал Центр имени Гамалеи, составила 70% против заболевания дельта-штаммом SARS-CoV-2 в течение трех месяцев после вакцинации».
При этом эксперты отмечают, что препарат хорошо зарекомендовал себя и в качестве бустера, то есть средства, усиливающего действия других вакцин. В этом случае «Спутник Лайт» демонстрирует показатель эффективности почти 83 процента.
«Спутник Лайт» и QR-код
Сегодня, когда актуальность QR-кодов резко возросла и их использование планируется закрепить на законодательном уровне, многие всерьез заинтересовались вопросом: можно ли сделать однокомпонентную вакцину «Спутник Лайт» и получить заветный QR-код?
Как выясняется, первичную вакцинацию «Спутником Лайт» пройти можно. Но QR-код при этом придет не сразу.
«Сертификат о первичной вакцинации однокомпонентным препаратом „Спутник Лайт“ начинает действовать через 21 день после прививки. Так как только через три недели после введения препарата формируется необходимая иммунная защита, проходит инкубационный период, — пояснил помощник министра здравоохранения Алексей Кузнецов. — При этом если говорить про повторную вакцинацию или вакцинацию ранее переболевших „Спутником Лайт“, то в этих случаях сертификат о вакцинации начинает действовать непосредственно в день прививки».
Безопасна ли вакцина «Спутник Лайт»?
С февраля 2021 года было запущено масштабное исследование эффективности и безопасности вакцины против коронавируса «Спутник Лайт», в котором принимают участие более семи тысяч человек по всему миру. В мае были получены промежуточные результаты исследования, которые показали, что препарат абсолютно безопасен даже для людей с хроническими заболеваниями. Отмечается, что вакцина не вызывает тромбозов, сокращает риск тяжелого развития болезни и последующей госпитализации.
Данная вакцина создана на базе аденовирусов человека — а этот принцип уже доказал свою безопасность на основании более чем 250 клинических испытаний во всем мире.
Результаты исследования, опубликованные в The Lancet
Авторитетный европейский медицинский журнал The Lancet опубликовал результаты масштабного исследования в отношении вакцины «Спутник Лайт», которое проводилось в Санкт-Петербурге с участием 110 здоровых добровольцев в возрасте от 18 до 59 лет.
«Результаты показывают, что вакцина хорошо переносилась и вызывала как гуморальный, так и клеточный иммунный ответ как у пациентов, не имеющих ранее антител, так и у взрослых с антителами», — говорится в статье.
В исследовании отмечается, что вакцинация «Спутником Лайт» очень быстро вызывает иммунный ответ. «Клеточный иммунный ответ сформировался у 96% тех, кто не имел иммунитета до вакцинации, уже к 10-му дню после укола», — пишут ученые в своем докладе.
Также сообщается, что в ходе эксперимента ни у кого из пациентов не обнаружено тяжелых побочных эффектов, а несерьезные осложнения были отмечены только у 5,5 процента испытуемых.
Безопасна ли вакцина «Спутник Лайт»
Важен ли уровень антител перед вакцинацией?
Многие граждане задаются вопросом: а нужно ли мне идти вакцинироваться? Может быть, у меня все еще держится высокий титр антител после ранее сделанной прививки или перенесенного заболевания коронавирусом?
Недавно Министерство здравоохранения РФ выпустило обновленные рекомендации в отношении порядка вакцинации от коронавирусной инфекции Covid-19. В них сказано, что уровень антител в вопросах постковидной вакцинации или ревакцинации совершенно неважен. Антитела, согласно исследованиям, присутствуют в крови пациентов от трех до девяти месяцев. Но специалисты рекомендуют делать прививку через полгода, чтобы избежать повторного или нового заражения. И вот почему.
Штаммы коронавируса постоянно мутируют, и гарантии того, что имеющиеся антитела защитят от нового вида вируса, нет. А вовремя сделанная прививка обладает профилактическим эффектом и способствует выработке коллективного иммунитета, который существенно усиливает защиту даже от новых штаммов Covid-19.
Отличие от вакцины «Спутник V»
Как уже было сказано, «Спутник Лайт» — это первый компонент вакцины «Спутник V». Иными словами, это не принципиально новая вакцина, а лишь облегченный вариант оригинального препарата. Он действует не столь длительное время, как «Спутник V», и защищает не на 90%, а всего на 70%. Однако препарат имеет свои плюсы.
К примеру, он быстрее вызывает иммунный ответ. К тому же отсутствие необходимости делать второй компонент чисто психологически действует на пациента более позитивно.
Что касается противопоказаний и побочных эффектов, то их количество минимально, так же как и у «Спутника V». Среди первых — тяжелые формы аллергии и индивидуальная непереносимость компонентов препарата. Среди вторых — обычные признаки ОРВИ или гриппа: слабость, небольшая температура, насморк, редко потеря обоняния. Вакцина показана беременным и кормящим женщинам. В отношении детей пока не применяется.
Когда появятся антитела?
Согласно информации Министерства здравоохранения РФ, рост антител у людей с иммунитетом к коронавирусу отмечается уже к 10-му дню после вакцинации. Тем не менее специалисты Роспотребнадзора рекомендуют соблюдать меры безопасности в течение всех 42 дней, то есть полного цикла выработки антител, так как в этот период все еще велик риск заразиться Covid-19.
Противопоказания
В инструкции препарата перечислены случаи противопоказаний в отношении данной вакцины. Их немного: это гиперчувствительность к какому-либо компоненту вакцины, тяжелые формы аллергии и острые фазы инфекционных заболеваний, обострение хронических заболеваний (в этом случае вакцинацию, как правило, переносят на период выздоровления или ремиссии).
С какими рисками и заболеваниями рекомендуется использовать «Спутник Лайт»?
При каких же заболеваниях можно и даже нужно прививаться «Спутником Лайт»? Отмечается, что с осторожностью и только после консультации с лечащим врачом и точной диагностики следует принимать вакцину пациентам с ВИЧ, онкологией, аутоиммунными патологиями, заболеваниями крови, эпилепсией и другими болезнями ЦНС, нарушением мозгового кровообращения, при расстройствах функции щитовидной железы и пр.
Также обнародованы условия, при которых людям показана только вакцинация «Спутником Лайт». К ним относятся:
- Возраст прививающихся — от 18 до 60 лет.
- Факт перенесенного пациентом ковида. В качестве доказательства нужно предъявить тест на антитела (бумажный или электронный вариант).
- Необходимость ревакцинации для пациентов, привившихся «Спутником V» (1-й и 2-й дозой) полгода назад.
- Рекомендация ревакцинации «Спутником Лайт» для тех, кто полгода назад был привит другой вакциной от ковида («КовиВак» или «ЭпиВакКорона»).
Побочные действия
Говоря о побочных действиях препарата, следует опять же вспомнить «Спутник V». Список побочек у обеих вакцин примерно одинаковый. Как правило, пациент, получивший прививку, чувствует легкое недомогание. Оно может напомнить самые распространенные симптомы как при гриппе или при коронавирусе: слабость с температурой или без температуры, боль в горле, кашель, боль в месте введения укола.
Если у пациента, впервые сделавшего вакцину «Спутник Лайт», отмечаются признаки аллергии: кожная сыпь или астматический кашель, следует немедленно обратиться к врачу. Возможно, это станет основанием для дальнейшего медотвода от прививки.
Принцип действия
По сути, данная вакцина, как и «Спутник V», вводит в организм пациента не сам коронавирус, а всего лишь часть внешней оболочки его генетического кода. Это абсолютно безопасно, так как не вызывает заражения ковидом, а лишь провоцирует ответную реакцию иммунной системы на «непрошеного гостя».
В течение следующих трех недель у вакцинированного пациента вырабатывается устойчивый иммунитет к Covid-19. В течение этого периода возможны проявления побочных эффектов, как при любой острой респираторной инфекции. Пациент может ощущать гриппозное состояние в легкой форме: озноб, невысокую температуру, слабость, боли в мышцах.
Врачи не советуют в это время пить противовирусные и антибиотики, так как они могут токсично влиять на иммунные клетки. Также не рекомендуется пить разжижающие средства, которые многие начинают принимать, опасаясь тромбоза. А вот обезболивающее, жаропонижающее и витамины принимать можно. Впрочем, болезненное состояние не является продолжительным. И вскоре даже без лекарств и интенсивного домашнего лечения пациент считается полностью вакцинированным.
Комбинации с другими вакцинами
«Что делать, если я ранее привился „КовиВаком“? Можно ли мне ревакцинироваться „Спутником Лайт“?» — такие вопросы очень часто задают медработникам. Действительно, каковы схемы взаимодействия разных вакцин? Не скажется ли оно негативно на организме человека?
По рекомендациям Минздрава РФ повторную вакцинацию можно сделать любой зарегистрированной в России вакциной. Но, конечно, в идеале ревакцинироваться «Спутником Лайт» нужно при первичной прививке «Спутником V».
Состав «Спутника Лайт»
Основное действующее вещество вакцины — это частички аденовируса, которые несут в себе генетический код S-белка коронавируса. Среди вспомогательных веществ: вода, сахароза, аминометан, полисорбат и пр.
Уточните наличие вакцины
Несмотря на то что сегодня не наблюдается дефицита «Спутника Лайт», медики советуют перед прививкой уточнить наличие вакцины, так как при высоких темпах вакцинации препараты быстро заканчиваются. В некоторых учреждениях вакцину необходимо заказывать заранее.
Жидкая или замороженная? Зависит от места производства
Вакцину производят в двух формах: замороженной и жидкой. Первый вариант можно хранить до 6 месяцев при температуре не выше минус 18 градусов. Таким образом, этот вид вакцины удобно транспортировать в дальние регионы, и она прекрасно сохранит свои свойства.
Жидкая вакцина представляет собой бесцветный или слегка желтоватый раствор. Такой препарат можно хранить 1 месяц при температуре 2 — 8 градусов.
Как делают прививку «Спутник Лайт»?
Прививку «Спутник Лайт» получают в виде однокомпонентной инъекции в область предплечья. Впоследствии место укола не рекомендуется мочить и нагревать (исключить походы в баню и сауну).
Ревакцинация «Спутником Лайт»: как подготовиться и нужно ли?
Необходимо ли особое питание перед прививкой, а может, ее вообще делают натощак? Такие вопросы тоже часто задают врачам пациенты. Медики утверждают, что особой подготовки не нужно. Лучше не приходить натощак, но накануне лучше не принимать алкоголь, исключить курение. Если пациент подозревает у себя начинающийся грипп или ОРВИ, то следует отложить поход в прививочный кабинет.
Особой реабилитации после прививки также не требуется.
Как делают прививку «Спутник Лайт»?
Кто выпускает «Спутник Лайт»?
Данный препарат разработан НИЦЭМ имени Гамалеи. А вот производство вакцины на сегодняшний день осуществляют по специальной лицензии восемь фармкомпаний. Среди них компании «Биннофарм», «Генериум», «Р-Фарм», «Биокад», «Фармстандарт — Уфимский витаминный завод», Центр им. Гамалеи.
Отзывы о вакцинации «Спутником Лайт»
На сегодняшний день уже тысячи россиян привились «Спутником Лайт». И вопреки слухам многие из них отмечают, что не почувствовали вообще никаких специфических симптомов после вакцинации. Кто-то говорит, что ощущения такие же, как после прививки от гриппа.
Так, Наталья из Нижнего Новгорода признается, что чувствовала ломоту, озноб, боль в горле, заложенность носа и температуру. Другая пациентка, которая ранее перенесла ковид, но без пневмонии, отмечает, что ощущала сильную боль в месте инъекции, начался кашель.
Где привиться «Спутником Лайт»?
На сегодняшний день прививка и ревакцинация «Спутником Лайт» доступна в любой поликлинике по месту жительства, в лечебных стационарах, в частных клиниках. Кстати, многие из них предлагают вакцинацию на дому.