Кетамин
Ketamine
Аналоги (дженерики, синонимы)
Действующее вещество
Кетамин (Ketaminum )
Фармакологическая группа
Наркозные средства
Рецепт
Международный:
Rр.: Sol. Ketamini 0,1 % — 2 ml
D.t.d. № 10 in ampull.
S. В дозе 1–4 мг/кг.
Rр.: Sol. Ketamini hydrochloridi 50 mg/ml — 10 ml
D.t.d. № 5 in flac.
S. В/в по 1 флакону
Россия:
Препарат не отпускается из аптек
Фармакологическое действие
Наркозное, анальгезирующее, снотворное. Угнетает ассоциативную зону и подкорковые образования таламуса (диссоциативная анестезия). Легко проходит гистогематические барьеры, включая ГЭБ. В печени деметилируется, теряя активность. Основная часть продуктов биотрансформации выделяется в течение 2 ч с мочой, незначительное количество метаболитов остается в организме несколько дней. Кумуляции при многократном введении не отмечено. Особенностью наркотизирующего эффекта является быстрота наступления, малая длительность, сохранение в наркотической фазе самостоятельной адекватной вентиляции легких. Вызывает выраженную анальгезию. Плохо расслабляет скелетную мускулатуру; в фазе наркоза сохраняются глоточный, гортанный и кашлевой рефлексы. Не угнетает и даже стимулирует сердечно-сосудистую систему.
Малотоксичен. Не обладает холино- и адреноблокирующими свойствами, а также антигистаминной активностью. При в/в введении 0,5 мг/кг сознание выключается через 1–2 мин на 2 мин, а анальгезия развивается в течение 10 мин и продолжается 2–3 ч. При в/м введении эффект наступает позже, но имеет большую длительность.
Фармакодинамика
Данных по этому разделу нет. В текущий момент мы обрабатываем информацию, пожалуйста вернитесь позже.
Фармакокинетика
Данных по этому разделу нет. В текущий момент мы обрабатываем информацию, пожалуйста вернитесь позже.
Способ применения
Для взрослых:
В/в, взрослым — в дозе 1–4 мг/кг, детям — 0,5–4,5 мг/кг.
Начальная доза для получения наркозного эффекта — 0,7–2 мг/кг, вводится медленно в течение 60 с, средняя доза для анестезии продолжительностью 5–10 мин — 2 мг/кг, при повторном введении применяют 1/2–1/3 первоначальной дозы или используют капельное введение 0,1% раствора (на физиологическом растворе или растворе глюкозы) со скоростью 20–60 капель в минуту; ослабленным больным, пожилым и больным в шоковом состоянии вводят в дозе 0,5 мг/кг, общая вводимая доза для взрослых составляет 2–6 мг/кг/ч.
В/м, доза 6,5–13 мг/кг (для детей — 2–5 мг/кг) вызывает наркоз продолжительностью 12–25 мин.
Показания
— для вводного и базисного наркоза, при кратковременных хирургических вмешательствах, требующих и не требующих мышечной релаксации.
— при болезненных инструментальных и диагностических манипуляциях
— при транспортировке больных
— обработке ожоговой поверхности.
Противопоказания
— нарушения мозгового кровообращения
— артериальная гипертензия
— стенокардия и сердечная недостаточность в фазе декомпенсации
— преэклампсия и эклампсия, эпилепсия в детском возрасте.
Особые указания
Данных по этому разделу нет. В текущий момент мы обрабатываем информацию, пожалуйста вернитесь позже.
Побочные действия
— Со стороны сердечно-сосудистой системы: повышение АД, тахикардия.
— Со стороны пищеварительной системы: гиперсаливация.
— Со стороны ЦНС: психомоторное возбуждение и галлюцинации в периоде выхода из наркоза.
— Со стороны дыхательной системы: одышка, угнетение дыхания.
— Местные реакции: крайне редко в месте введения возможна болезненность и гиперемия по ходу вены.
Передозировка
Данных по этому разделу нет. В текущий момент мы обрабатываем информацию, пожалуйста вернитесь позже.
Лекарственное взаимодействие
Данных по этому разделу нет. В текущий момент мы обрабатываем информацию, пожалуйста вернитесь позже.
Форма выпуска
Р-р д/инъекц. 100 мг/2 мл: амп. 10 шт.
Раствор для инъекций прозрачный, бесцветный или слегка окрашенный.
1 мл
1 амп. кетамин (в форме гидрохлорида) 50 мг 100 мг
Вспомогательные вещества: бензетония хлорид, натрия хлорид, вода д/и.
2 мл — ампулы (10) — пачки картонные.
Эта информация оказалась полезной?
Содержание
- Структурная формула
- Русское название
- Английское название
- Латинское название вещества Кетамин
- Химическое название
- Брутто формула
- Фармакологическая группа вещества Кетамин
- Нозологическая классификация
- Код CAS
- Фармакологическое действие
- Характеристика
- Фармакология
- Применение вещества Кетамин
- Противопоказания
- Ограничения к применению
- Побочные действия вещества Кетамин
- Взаимодействие
- Способ применения и дозы
- Торговые названия с действующим веществом Кетамин
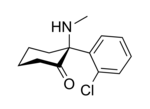
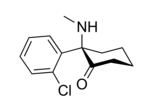
Структурная формула
Английское название
Ketamine
Латинское название вещества Кетамин
Ketaminum (род. Ketamini)
Химическое название
(±)-2-(2-Хлорфенил)-2-(метиламино)циклогексанон (в виде гидрохлорида)
Брутто формула
C13H16ClNO
Фармакологическая группа вещества Кетамин
Фармакологическое действие
—
анальгезирующее, наркозное, снотворное.
Характеристика
Белый или почти белый кристаллический порошок со слабым характерным запахом. Легко растворим в воде и спирте, pH водных растворов 3,5–4,5.
Фармакология
Угнетает ассоциативную зону и подкорковые образования таламуса (диссоциативная анестезия). Легко проходит гистогематические барьеры, включая ГЭБ. В печени деметилируется, теряя активность. Основная часть продуктов биотрансформации выделяется в течение 2 ч с мочой, незначительное количество метаболитов остается в организме несколько дней. Кумуляции при многократном введении не отмечено. Особенностью наркотизирующего эффекта является быстрота наступления, малая длительность, сохранение в наркотической фазе самостоятельной адекватной вентиляции легких. Вызывает выраженную анальгезию. Плохо расслабляет скелетную мускулатуру; в фазе наркоза сохраняются глоточный, гортанный и кашлевой рефлексы. Не угнетает и даже стимулирует сердечно-сосудистую систему. Малотоксичен. Не обладает холино- и адреноблокирующими свойствами, а также антигистаминной активностью. При в/в введении 0,5 мг/кг сознание выключается через 1–2 мин на 2 мин, а анальгезия развивается в течение 10 мин и продолжается 2–3 ч. При в/м введении эффект наступает позже, но имеет большую длительность.
Применение вещества Кетамин
Вводный наркоз, базисный наркоз для обезболивания кратковременных операций и болезненных инструментальных вмешательств (в т.ч. в стоматологической, офтальмологической, оториноларингологической, гинекологической и акушерской практике, и диагностических процедур — эндоскопия, катетеризация сердца и др.), при проведении экстренных хирургических операций у больных с травматическим шоком и кровопотерей, обезболивание при транспортировке больных, при обработке ожоговой поверхности.
Противопоказания
Гиперчувствительность, нарушение мозгового кровообращения (в т.ч. в анамнезе), артериальная гипертензия, преэклампсия, эклампсия, алкоголизм, эпилепсия у детей.
Ограничения к применению
Заболевания почек, декомпенсированная хроническая сердечная недостаточность, операции на гортани и глотке.
Побочные действия вещества Кетамин
Повышение АД, тахикардия, слюнотечение, тошнота, одышка, угнетение дыхательного центра, мышечная ригидность и повышение мышечной активности, обтурация верхних дыхательных путей из-за спазма жевательной мускулатуры и западения языка. В период выхода из состояния наркоза — галлюцинации, психомоторное возбуждение и длительная дезориентация, психоз. Болезненность и гиперемия по ходу вены в месте введения.
Взаимодействие
Усиливает эффект ингаляционных наркозных средств. Углубляет миорелаксацию, вызываемую тубокурарина хлоридом и суксаметония йодидом, не изменяет — панкурония бромидом. Во время наркоза у пациентов, принимающих йодсодержащие препараты и гормоны щитовидной железы, высока вероятность развития артериальной гипертензии и тахикардии (устраняются бета-адреноблокаторами). Дроперидол и бензодиазепины, в т.ч. диазепам, ослабляют риск проявления психотомиметической и моторной активности, а также возникновения тахикардии и и повышения АД. Фармацевтически несовместим с барбитуратами.
Способ применения и дозы
В/в, взрослым — в дозе 1–4 мг/кг, детям — 0,5–4,5 мг/кг. Начальная доза для получения наркозного эффекта — 0,7–2 мг/кг, вводится медленно в течение 60 с, средняя доза для анестезии продолжительностью 5–10 мин — 2 мг/кг, при повторном введении применяют 1/2–1/3 первоначальной дозы или используют капельное введение 0,1% раствора (на физиологическом растворе или растворе глюкозы) со скоростью 20–60 капель в минуту; ослабленным больным, пожилым и больным в шоковом состоянии вводят в дозе 0,5 мг/кг, общая вводимая доза для взрослых составляет 2–6 мг/кг/ч.
В/м, доза 6,5–13 мг/кг (для детей — 2–5 мг/кг) вызывает наркоз продолжительностью 12–25 мин.
Торговые названия с действующим веществом Кетамин
Состав
1 мл раствора 5% содержит 50 мг активного компонента кетамина гидрохлорида.
Форма выпуска
Кетамин выпускается в ампулах по 2 и 10 мл. В каждой пачке из картона содержится по 10 ампул.
Фармакологическое действие
Что такое Кетамин? Это средство, которое при внутримышечном либо внутривенном вливании способно оказывать наркотизирующее (анестезирующее) и анальгезирующее воздействия. Фармакологическая группа – «Наркозные средства». Действующее вещество обладает непродолжительным эффектом, и в наркотических дозах позволяет сохранять адекватное самостоятельное дыхание. ЛС обладает диссоциативной общей анестезией, что объясняется угнетающим воздействием в отношении подкорковых образований таламуса и ассоциативной зоны.
Механизм действия Кетамина основан на избирательном подавлении нейрональной передачи в структуре коры головного мозга, как в таламусе, так и в ассоциативных зонах. В тоже время наблюдается стимуляция лимбической системы и гиппокампа. В результате развивается функциональное разобщение неспецифических связей в структуре таламуса и среднего мозга, блокируются поступающие ноцицептивные афферентные стимулы в высшие мозговые центры из спинного мозга, угнетается импульсная передача в продолговатый мозг (ретикулярную формацию). Считается, что обезболивающий и гипнотический эффекты Кетамина связаны с влиянием активного вещества на различные типы рецепторов. Эффекты медикамента не связаны с блокирование натриевых каналов в нервной системе и воздействием на ГАМК-рецепторы. Википедия содержит информацию по истории синтезирования Кетамина.
Фармакодинамика и фармакокинетика
Кетамин это липофильное соединение, которое достаточно быстро способно распределяться сначала в хорошо кровоснабжаемых органах, а затем и в тканях со сниженной перфузией. Метаболизируется в печёночной системе. Через почки выводится в форме конъюгированных веществ-метаболитов.
Показания к применению
Кетамин что это? Медикамент применяется как для мононаркоза (1 компонент), так и для комбинированного наркоза преимущественно у лиц с низким уровнем кровяного давления, либо при необходимости сохранения у пациента самостоятельного дыхания. Чаще всего Кетамин применяется во время эвакуации при массивных кровопотерях и травматическом шоке, при краткосрочных кардиохирургических операциях, в экстренной хирургии. Кетамин назначают при:
- катетеризации сердца;
- эндоскопических манипуляциях;
- перевязках в оториноларингологии, офтальмологии и стоматологии.
Медикамент может применяться при кесаревом сечении в акушерской практике.
Противопоказания
- эпилепсия;
- нарушение мозгового кровообращения;
- эклампсия при тяжелой форме декомпенсации кровообращения;
- выраженная гипертония.
При необходимости применения миорелаксантов во время операций на гортани Кетамин назначают с осторожностью. Недопустимо смешивание с растворами барбитуратов из-за риска выпадения осадка.
Побочные действия
Медикамент оказывает общее воздействие на организм человека. При введении раствора регистрируется подъём кровяного давления на 20-30%, учащение сердцебиения, повышение минутного объёма крови, снижение периферического сопротивления сосудов. Применение Сибазона (Диазепама) помогает уменьшить стимулирующее влияние Кетамина на сердечную деятельность. В большинстве случаев активный компонент не угнетает рефлексы верхнего отдела дыхательного тракта, не вызывает бронхоспазма, ларингоспазма, рвоты и тошноты. Угнетение дыхания регистрируется при быстром внутривенно вливании раствора. Атропин и Метацин позволяют снизить саливацию. При введении медикамента могут регистрироваться галлюцинации, гипертонус, непроизвольные движения (купируется при введении Дроперидола и транквилизаторов). Возможно покраснение кожных покровов по ходу вены в месте инъекции; при пробуждении от наркоза – длительная дезориентация и психомоторное возбуждение.
Инструкция по применению Кетамина (Способ и дозировка)
Раствор вводят внутривенно (фракционно/струйно) либо внутримышечно. Внутривенно взрослым вводят 2-3 мг, внутримышечно – 4-8 мг на 1 кг веса. Повторное введение Кетамина позволяет продлить наркоз (скорость 2 мг/кг/час). Такой способ введения возможен при наличии инфузоматов либо достигается капельным введением раствора Кетамина 1% в растворе хлорида натрия или изотоническом растворе (30-60 капель в минуту).
В педиатрической практике раствор применяется для комбинированной анестезии. Расчет производится по схеме: 4-5 мг/кг в виде раствора 5%. Требуется обязательная премедикация.
Лекарственное средство может применяться совместно с анальгетиками (Промедол, Фентанил, депидолор и т.д.) и нейролептиками (например, Дроперидол), однако для этого требуется снижение дозы.
Передозировка
Регистрируется угнетение дыхания, что требует проведение своевременной искусственной вентиляции легких.
Взаимодействие
Кетамин несовместим с барбитуратами на химическом уровне (образуется преципитат). Медикамент способен потенцировать действие всех средств, применяемых для ингаляционного наркоза. Лекарственный препарат усиливает действие тубокурарина, но не влияет на эффективность сукцинилхолина и панкурония.
Условия продажи
Продаётся только для стационаров и лечебных учреждений, не предназначен для свободной продажи.
Условия хранения
Производителем рекомендуется соблюдать стандартный температурный режим 15-25 градусов. Ограничить допуск детей к раствору.
Срок годности
5 лет.
Особые указания
При патологии почечной системы применяется с осторожностью. При оперативных вмешательствах на глотке и гортани обязательно введение миорелаксантов. В течение суток после введения Кетамина нельзя управлять автотранспортом из-за заторможенности реакции и снижения внимания.
Аналоги
Совпадения по коду АТХ 4-го уровня:
- Калипсол;
- Кетанест;
- Кеталар.
При беременности и лактации
Активный компонент проходит сквозь плацентарный барьер. На данный момент безопасность применения Кетамина у беременных женщин не установлена. Не рекомендуется к назначению беременным и в период лактации.
Отзывы о Кетамине
От анестезиологов, которые постоянно используют Кетамин в своей практике, можно услышать только положительные отзывы о медикаменте.
Цена Кетамина, где купить
Закупкой занимаются только лечебные учреждения. Купить Кетамин самостоятельно невозможно. Цена для ЛПУ зависит от региона, объёма закупки (в среднем стоимость одной упаковки 1200 рублей).
МНН: Кетамин
Производитель: Фармак ПАО
Анатомо-терапевтическо-химическая классификация: Ketamine
Номер регистрации в РК:
№ РК-ЛС-5№003486
Информация о регистрации в РК:
31.03.2016 — 31.03.2021
Номер регистрации в РБ:
8825/08/14/19
Информация о регистрации в РБ:
05.04.2019 — бессрочно
Информация о реестрах и регистрах
Информация по ценам и ограничения
Предельная цена закупа в РК:
54.51 KZT
- Скачать инструкцию медикамента
Торговое название
Кетамин
Международное непатентованное название
Кетамин
Лекарственная форма
Раствор для инъекций 50 мг/мл
Состав
1 мл препарата содержит
активное вещество — кетамина гидрохлорид 57,6 мг (в пересчете на кетамин 50 мг),
вспомогательные вещества: бензетония хлорид, натрия хлорид, вода для инъекций.
Описание
Прозрачная бесцветная или слегка окрашенная жидкость
Фармакотерапевтическая группа
Анестетики. Анестетики общие. Анестетики общие другие. Кетамин
Код АТХ N01AX03
Фармакологические свойства
Фармакокинетика
Кетамин быстро распределяется в хорошо снабженных сосудами тканях, включая мозг и плаценту. Исследования на животных показали, что кетамин в значительной мере концентрируется в жировой ткани, печени и легких. Прекращение анестезирующего эффекта возникает частично вследствие перераспределения из ЦНС в периферические ткани, частично путем биотрансформации в печени в активные метаболиты. Время полувыведения составляет приблизительно 2-3 часа. Выводится почками, большей частью в виде конъюгированных метаболитов.
Фармакодинамика
Кетамин – быстродействующий общий анестетик для внутривенного и внутримышечного использования с выраженным фармакологическим действием. Препарат вызывает так называемую диссоциативную анестезию, характеризующуюся каталепсией, амнезией и выраженным обезболиванием, которые могут сохраняться в период выхода из наркоза. При применении Кетамина глоточно-гортанные рефлексы остаются в норме; тонус скелетных мышц может быть в норме или в разной степени повышаться.
Происходит незначительная стимуляция сердечной и дыхательной систем, а иногда возникает угнетение дыхания.
Кетамин вызывает седативный и гипнотический эффекты, амнезию и выраженную аналгезию. Состояние анестезии, которое вызывает Кетамин, называется “диссоциативная анестезия” в связи с тем, что он выборочно прерывает ассоциативные связи в головном мозге до того, как блокирует проприоцептивную глубокую чувствительность. Он может селективно угнетать таламо-неокортикальную систему перед тем, как существенно притупить центры и связи мозга (активируя ретикулярную формацию и лимбическую систему). Многочисленные теории пытаются объяснить эффект Кетамина, включая связывание с рецепторами N-метил-D-аспартата (NMDA) в центральной нервной системе, взаимодействием с опиатными рецепторами и взаимодействием с норадреналином, серотонином и мускариновыми холинергическими рецепторами. Активность рецепторов NMDA может быть ответственной за аналгетический так же, как и психиатрический эффекты Кетамина. Кетамин имеет симпатомиметическую активность, что приводит к тахикардии, гипертонии, повышенному потреблению кислорода миокардом и мозгом, усилению мозгового кровообращения и повышению внутричерепного и внутриглазного давления. Кетамин также является мощным бронходилататором. Клинические эффекты, которые наблюдались после введения Кетамина, включают: повышенное кровяное давление, повышенный тонус мышц (может напоминать кататонию), открытие глаз (как правило, в сопровождении нистагма) и увеличение потребления кислорода миокардом.
Показания к применению
— в качестве анестетика при проведении диагностических и хирургических процедур. Внутривенные и внутримышечные инъекции лучше всего подходят для коротких процедур. При введении дополнительных доз или путем применения в виде внутривенной инфузии Кетамин может использоваться для более длительных процедур. Если необходимо расслабление мышц, следует использовать мышечный релаксант и обеспечить поддержку дыхания.
— для индукции наркоза до введения других общих анестетиков.
Специальные показания для применения кетамина или типы процедур:
— проведение наркоза больным, у которых предпочтение отдается внутримышечному введению препарата;
— обработка ран, болезненные процедуры (смена повязки) и пересадка кожи у пациентов с ожогами, а также другие поверхностные хирургические процедуры;
— нейродиагностические процедуры, такие как пневмоэнцефалография, вентрикулография, миелография, люмбальные пункции;
— диагностические и хирургические вмешательства в области глаз, ушей, носа и ротовой полости, включая удаление зубов (примечание: движения глаз могут сохраняться во время офтальмологической процедуры);
— анестезия больным со значительным риском ухудшения или необходимостью избежать ухудшения жизненно важных функций;
— ортопедические процедуры (закрытая репозиция, манипуляции, установка штифта в бедро, ампутация, биопсия);
— ректороманоскопия и незначительные хирургические процедуры на анусе, прямой кишке, обрезание и пилонидальный синус;
— процедуры катетеризации сердца;
— введение в наркоз для операции кесарева сечения при отсутствии повышенного артериального давления;
— при анестезии у больных с астмой для минимизации риска развития бронхоспазма или при наличии бронхоспазма, если анестезия не может быть отложена.
Способ применения и дозы
Кетамин вводят внутривенно (струйно или капельно) или внутримышечно.
Примечание: все дозы указаны в пересчете на действующее вещество кетамин.
Нижеприведенные дозы касаются взрослых, пациентов пожилого возраста (старше 65 лет) и детей. При хирургических вмешательствах у пожилых пациентов Кетамин может использоваться в виде монотерапии или в комбинации с другими анестетиками.
Предоперационная подготовка
В экстренных случаях допускается применение Кетамина в качестве единственного анестетика не на пустой желудок. Однако, так как нельзя спрогнозировать необходимость использования других препаратов и мышечных релаксантов, при подготовке к плановой операции желательно не принимать пищу и жидкость за 6 часов до анестезии.
Премедикация антихолинергическими препаратами (например, атропином, гиосцином и др.) должна быть проведена с определенным интервалом до введения Кетамина, чтобы уменьшить кетамин-индуцированное повышенное слюноотделение.
Мидазолам, диазепам, лоразепам или флунитразепам, при использовании для премедикации или как дополнение к Кетамину, снижают частоту возникновения побочных реакций.
Начало анестезии и продолжительность
Индивидуальная реакция на Кетамин может варьировать в зависимости от дозы, пути введения и возраста пациента, а также совместного использования других средств. Поэтому подбор дозы должен проводиться индивидуально. Кетамин является быстродействующим препаратом, поэтому пациент должен находиться в оптимальном для проведения процедуры положении.
Внутривенная доза 2 мг/кг массы тела обеспечивает хирургическую анестезию через 30 секунд после инъекции продолжительностью 5-10 минут. Внутримышечная доза 10 мг/кг массы тела обеспечивает хирургическую анестезию через 3-4 минуты после инъекции продолжительностью 12-25 минут.
Кетамин в качестве единственного анестетика
Внутривенная инфузия
Применение Кетамина путем непрерывного введения позволяет подобрать более точную дозу по сравнению с прерывистым введением. Это обуславливает более короткое время выхода из наркоза.
Проводится из расчета 1 мг/мл Кетамина, разведенного в 0,9 % растворе натрия хлорида или 5 % декстрозе.
Общий вводный наркоз
Вводить в виде инфузии в дозе 0,5-2 мг/кг.
Поддержание анестезии
Анестезия может поддерживаться с использованием инфузомата со скоростью 10-45 мкг/кг/мин (приблизительно 1-3 мг/мин).
Скорость инфузии зависит от реакции пациента на анестезию. Доза может быть уменьшена при использовании миорелаксанта длительного действия.
Прерывистое введение
Внутривенное введение
Начальная доза Кетамина при внутривенном введении может находиться в диапазоне от 1 мг/кг до 4,5 мг/кг (из расчета на действующее вещество кетамин). Средняя доза, необходимая для обеспечения хирургической анестезии длительностью 5-10 минут, составляет 2,0 мг/кг. Рекомендуется медленное внутривенное введение (в течение 60 секунд). Более быстрое введение может привести к угнетению дыхания и повышению артериального давления.
Внутримышечное введение
Начальная доза Кетамина для внутримышечного введения составляет от 6,5 мг/кг до 13 мг/кг (в расчете на действующее вещество кетамин). Низкая начальная внутримышечная доза (4 мг/кг) используется при проведении диагностических манипуляций и процедур, не связанных с сильными болевыми ощущениями. Доза 10 мг/кг, как правило, обеспечивает анестезию в течение 12-25 минут.
Дозирование при печеночной недостаточности
Необходимость снижения дозы следует рассматривать у пациентов с циррозом печени или другими видами печеночной недостаточности (см. раздел «Особые указания»).
Поддержание общего наркоза
Нистагм, двигательные реакции на раздражение и голос свидетельствуют об ослаблении анестезии. Для поддержания анестезии вводятся внутривенно или внутримышечно дополнительные дозы Кетамина.
Каждая дополнительная доза должна составлять от половины до полной первоначальной дозы введения, независимо от способа введения.
Однако, непроизвольные движения конечностей могут возникать независимо от глубины наркоза!
Кетамин в качестве индуцирующего агента перед использованием других общих анестетиков
Индукция достигается путем внутривенного или внутримышечного введения полной дозы Кетамина. Если Кетамин вводили внутривенно, а основной анестетик замедленного действия, повторная доза Кетамина должна быть введена через 5-8 минут после первоначальной дозы. Если Кетамин вводили внутримышечно, а основной анестетик быстрого действия, введение основного анестетика должно быть проведено через 15 минут после инъекции Кетамина.
Кетамин как дополнение к анестетикам
Кетамин клинически совместим с широко используемыми общими и местными анестетиками при надлежащей поддержке дыхания. Доза Кетамина для использования в сочетании с другими анестетиками, как правило, находится в том же диапазоне, однако использование другого анестетика может позволить снизить дозу Кетамина.
Наблюдение за пациентами в период восстановления
После процедуры за пациентом следует наблюдать, но не беспокоить. Это не исключает мониторинг жизненно важных функций. При появлении делирия можно использовать диазепам (от 5 до 10 мг внутривенно у взрослых). Гипнотическая доза тиобарбитурата (от 50 до 100 мг внутривенно) может использоваться для уменьшения серьезных реакций при восстановлении. При использовании этих препаратов время восстановления после анестезии может увеличиться.
Побочные действия
Нежелательные эффекты по частоте возникновения классифицируют по таким категориям: очень часто (>1/10); часто (>1/100, <1/10); нечасто (>1/1000, <1/100), редко (>1/10000, <1/1000), очень редко (<1/10000, включая единичные случаи).
Со стороны иммунной системы
Редко: анафилактические реакции.
Нарушения обмена веществ
Нечасто: анорексия.
Психические расстройства
Часто: галлюцинации, аномальные или кошмарные сновидения, спутанность сознания, психомоторное возбуждение, неадекватное поведение.
Нечасто: ощущение страха, тревоги.
Редко: делирий, симптом «обратного кадра», дисфория, бессонница, дезориентация.
Со стороны нервной системы
Часто: нистагм, повышение тонуса скелетных мышц и тонико-клонические судороги.
Со стороны органов зрения
Часто: диплопия.
Неизвестна: повышение внутриглазного давления.
Кардиальные нарушения
Часто: повышение артериального давления и частоты сердечных сокращений.
Нечасто: брадикардия, аритмия.
Сосудистые нарушения
Нечасто: гипотензия.
Со стороны дыхательной системы
Часто: увеличение частоты дыхания.
Нечасто: угнетение дыхания, ларингоспазм.
Редко: обструкция дыхательных путей или остановка дыхания.
Со стороны гепатобилиарной системы
Неизвестна: изменения лабораторных показателей функции печени.
Со стороны желудочно-кишечного тракта
Часто: тошнота, рвота.
Редко: слюнотечение.
Со стороны кожи и подкожных тканей
Часто: эритема и/или кореподобная сыпь.
Неизвестна: крапивница.
Со стороны почек и мочевыделения
Редко: цистит, геморрагический цистит.
Общие нарушения и реакции в месте введения
Нечасто: реакции в месте введения, включая боль и/или высыпания в месте введения препарата.
Противопоказания
-
повышенная чувствительность к действующему веществу или к другим компонентам препарата
-
эклампсия, преэклампсия
-
кетамин противопоказан пациентам, у которых повышение артериального давления может представлять серьезную угрозу для жизни; больным с черепно-мозговой травмой, внутричерепным кровоизлиянием, инсультом, тяжелыми сердечно-сосудистыми заболеваниями, нарушениями мозгового кровообращения.
Лекарственные взаимодействия
Одновременное использование барбитуратов и/или других средств для наркоза с Кетамином вызывает удлинение времени пробуждения после наркоза.
Кетамин в комбинации с атракурием и тубокурарином может усиливать блокаду нервно-мышечной передачи, включая угнетение дыхания и апноэ.
Использование галогенированных анестетиков одновременно с Кетамином может удлинить период полувыведения Кетамина и увеличить время пробуждения после наркоза. Совместное использование Кетамина (особенно в высоких дозах или при быстром введении) с галогенированными анестетиками может повысить риск развития брадикардии, гипотензии или снижения сердечного выброса.
Применение Кетамина с другими лекарственными средствами, которые снижают активность центральной нервной системы (например, этанол, фенотиазины, антигистаминные препараты или миорелаксанты) может усиливать угнетение ЦНС и/или увеличивать риск развития дыхательной недостаточности. Возможна необходимость в уменьшении дозы препарата при одновременном применении снотворных, седативных и транквилизаторов. Сообщалось, что Кетамин является антагонистом снотворного эффекта тиопентала.
У пациентов, получающих терапию тиреоидными гормонами, увеличивается риск повышения артериального давления и тахикардии при применении Кетамина.
Одновременное применение антигипертензивных препаратов и Кетамина увеличивает риск развития гипотензии.
При комбинации с аминофилином (теофилином) может снижаться судорожный порог. Имеются данные о непредсказуемых судорогах мышц разгибателей, которые сопровождались одновременным приемом этих лекарственных средств.
Особые указания
Можно комбинировать с любым видом местной анестезии.
Препарат должен назначать специалист – анестезиолог.
Как и при применении других средств для общей анестезии, при применении Кетамина необходимо подготовить инструменты и оборудование для реанимации.
Поскольку при применении лекарственного средства возможно угнетение дыхания, необходимо наличие аппарата для искусственной вентиляции легких. Применение аппарата должно комбинироваться с применением аналептиков.
Внутривенно Кетамин необходимо вводить медленно (в течение 1 минуты). Быстрое введение препарата может привести к угнетению дыхания или его остановке и резкому повышению артериального давления.
Поскольку при терапии Кетамином фарингеальные рефлексы, как правило, сохранены, следует избегать механического раздражения глотки. При вмешательстве на гортани, глотке или трахее необходима комбинация Кетамина с миорелаксантами и тщательный контроль дыхания.
При хирургических вмешательствах с вовлечением висцеральных путей болевой чувствительности может оказаться необходимым введение других аналгетиков.
При применении Кетамина в амбулаторных условиях пациента можно отпустить только после полного восстановления сознания и в сопровождении взрослого человека.
Кетамин следует применять с особой осторожностью при следующих состояниях:
-
хроническом алкоголизме и острой алкогольной интоксикации;
Кетамин метаболизируется в печени и полное высвобождение его через печень приводит к прекращению клинических эффектов. Удлинение действия может возникнуть у больных с циррозом печени или при других видах печеночной недостаточности. Поэтому дозу Кетамина следует снижать у таких пациентов. Также сообщалось об отклонениях печеночных проб от нормальных показателей, которые были связаны с длительным применением препарата, в частности, эти отклонения наблюдались у пациентов, которые применяли лекарственное средство более 3 дней или у лиц с наркотической зависимостью.
-
при повышенном давлении в спинномозговом канале;
-
у пациентов с проникающей травмой глаза и/или повышением внутриглазного давления (например, глаукома), потому, что давление может значительно повыситься даже после одноразового применения Кетамина;
-
пациентам с невротическими нарушениями или психическими заболеваниями (например: шизофрения, острый психоз);
-
пациентам с острой интермиттирующей порфирией;
-
пациентам с эпилептическими припадками;
-
пациентам с гипертиреозом или пациентам, которые получают заместительную терапию препаратами щитовидной железы (увеличивается риск повышения артериального давления и частоты сердечных сокращений);
-
пациентам с инфекционными заболеваниям верхних дыхательных путей или легких (так как Кетамин повышает чувствительность глоточного рефлекса, который в свою очередь может вызвать ларингоспазм).
-
пациентам с внутричерепными объемными образованиями, травмой головы или гидроцефалией.
Реакции и особенности, которые могут наблюдаться после выхода пациента из наркоза.
Психические расстройства могут варьировать от самых легких до более тяжелых, таких как фантастические переживания, подобные тем, которые представляются во сне, яркие видения, галлюцинации, ночные кошмары, постнаркозный делирий (который часто проявлялся диссоциативными ощущениями и ощущением свободного полета), в некоторых случаях эти состояния сопровождаются спутанностью сознания, психомоторным возбуждением иррациональным поведением. Вышеперечисленные проявления наблюдались только у некоторых пациентов.
В период выхода из наркоза может наблюдаться острый делирий. Эту реакцию можно предупредить путем введения бензодиазепинов или снижением вербальных, тактильных и визуальных раздражений. Однако это не исключает наблюдения за жизненно важными параметрами.
Поскольку Кетамин повышает потребление миокардом кислорода, его следует с осторожностью использовать у пациентов с гиповолемией, дегидратацией или болезнями сердца, особенно при ишемической болезни сердца (например, застойная сердечная недостаточность, состояние ишемии и инфаркт миокарда). Также с осторожностью используют Кетамин у пациентов с артериальной гипертензией легкой и умеренной степени и при тахиаритмиях.
Больным с артериальной гипертензией или сердечной недостаточностью необходим постоянный мониторинг сердечной функции во время наркоза. Премедикация диазепамом уменьшает гипертензивную реакцию. Максимум повышения артериального давления (20-25 %) наблюдается через несколько минут после внутривенного введения препарата, но через 15 минут артериальное давление возвращается к начальным значениям. В зависимости от состояния пациента, повышение артериального давления может рассматриваться как позитивный эффект, или в других случаях, как побочная реакция.
Имеются данные о зарегистрированных случаях цистита, включая геморрагический цистит у пациентов, которые получали Кетамин в течение длительного периода (от 1 месяца до нескольких лет). Кетамин не назначается и не рекомендуется для использования в течение длительного периода.
Также сообщалось о случаях злоупотребления кетамином. Имеются данные, которые показывают, что кетамин способствует возникновению проявлений: дисфории, галлюцинаций, симптома «обратного кадра», ощущения страха и тревоги, бессонницы или дезориентации, также случаев цистита или геморрагического цистита. Использование Кетамина ежедневно в течение нескольких недель может вызвать зависимость, особенно у лиц, имеющих или имевших наркотическую зависимость в анамнезе. Поэтому использовать препарат необходимо под тщательным наблюдением медперсонала и с осторожностью при вышеупомянутых состояниях и заболеваниях.
Несовместимость.
Ввиду химической несовместимости барбитураты нельзя вводить в одном шприце вместе с Кетамином.
В случае необходимости одновременного применения Кетамина с диазепамом препараты следует вводить отдельно и нельзя смешивать в одном шприце или инфузии.
Не применять растворители не указанные в разделе «Способ применения и дозы».
Применение в педиатрии
Препарат применяют в педиатрической практике.
Применение в период беременности и лактации
Кетамин проникает через плаценту. На это следует обратить внимание во время оперативных акушерских манипуляций во время беременности. За исключением введения препарата во время операции кесарево сечения или родов через естественные родовые пути, безопасное использование во время беременности и в период лактации не было установлено, и такое использование не рекомендуется.
Особенности влияния препарата на способность управлять транспортом и потенциально опасными механизмами
Пациенты должны быть предупреждены, что управлять автомобилем или работать с другими механизмами и принимать участие в любых других опасных видах деятельности запрещено в течение не менее 24 часов после анестезии.
Кетамин может ухудшать когнитивную функцию, что может повлиять на способность управлять транспортным средством.
Передозировка
При использовании Кетамина возможно угнетение дыхания, поэтому необходимо наличие аппарата искусственной вентиляции легких. Предпочтение отдается механической поддержке дыхания вместо введения аналептиков.
Кетамин имеет большой коэффициент безопасности; несколько случаев непреднамеренной передозировки Кетамина (превышение необходимой дозы до 10 раз) сопровождалось длительным, но полным выходом из наркоза.
Форма выпуска и упаковка
По 2 мл в ампулы из стекла 1 гидролитического класса с кольцом или точкой излома.
По 10 мл во флаконы из прозрачного стекла для инъекций, укупоренные крышками комбинированными (с алюминиевым колпачком с резиновой прокладкой и пластиковым вкладышем) или с пробкой резиновой для инъекционных флаконов и алюминиевой крышкой комбинированной с пластиковым колпачком.
На ампулы и флаконы наклеивают этикетки-самоклейки.
По 10 ампул вместе с инструкцией по медицинскому применению на государственном и русском языках помещают в пачку из картона с гофрированными вкладышами.
По 5 флаконов вместе с инструкцией по медицинскому применению на государственном и русском языках помещают в пачку из картона с вкладышем.
Или по 5 ампул или 5 флаконов вкладывают в контурную ячейковую упаковку из полимерного материала. По 1 контурной ячейковой упаковке (с флаконами) или по 2 контурные ячейковые упаковки (с ампулами) вместе с инструкцией по медицинскому применению на государственном и русском языках помещают в пачку из картона.
Допускается на пачку с гофрированными вкладками для упаковки ампул и флаконов наклеивать этикетку-самоклейку для контроля вскрытия пачки.
Условия хранения
Хранить в оригинальной упаковке при температуре не выше 25 ºС.
Хранить в недоступном для детей месте!
Срок хранения
3 года
Не применять препарат по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек
По рецепту
Производитель
ПАО «Фармак», Украина, 04080, г. Киев, ул. Фрунзе, 74.
Владелец регистрационного удостоверения
ПАО «Фармак», Украина
Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству продукции (товара)
Республика Казахстан, г. Алматы, индекс 050012, ул. Амангельды 59 «А» Бизнес центр «Шартас», 9 этаж.
Тел +7 (727) 267 64 63, факс +7 (727) 267 63 73, электронный адрес: a.liadobruk@gmail.com
| 405915931477976263_ru.doc | 118 кб |
| 986759211477977466_kz.doc | 112 кб |
| 8825_08_14_19_p.pdf | 0.66 кб |
| 8825_08_14_19_s.pdf | 0.66 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники. «Центр экспертиз и испытаний в здравоохранении» МЗ РБ
Кетамин
- Кетамин
- Кетамин
Действующее вещество
›› Кетамин* (Ketamine*)
Латинское название
Ketaminum
АТХ:
›› N01AX03 Кетамин
Фармакологическая группа: Наркозные средства
Состав и форма выпуска
1 ампула с 2 мл раствора для инъекций содержит кетамина 100 мг; в картонной пачке 10 шт.
Способ применения и дозы
В/в (струйно или капельно) — 2–3 мг/кг; в/м — 4–8 мг/кг. Для поддержания наркоза капельно вводят Кетамин в изотоническом растворе глюкозы или хлорида натрия со скоростью 30–60 капель/мин.
Срок годности
2 года
Условия хранения
Список А.: В защищенном от света месте.
Словарь медицинских препаратов.
2005.
Синонимы:
Смотреть что такое «Кетамин» в других словарях:
-
Кетамин — … Википедия
-
кетамин — сущ., кол во синонимов: 4 • калипсол (2) • кеталар (1) • кетанест (2) • … Словарь синонимов
-
КЕТАМИН — (ketamine) лекарственное вещество; применяется для анестезии (особенно у детей). Назначается в инъекциях. Торговое название: кеталар (Ketalar) … Толковый словарь по медицине
-
Кетамин (Ketamine) — лекарственное вещество; применяется для анестезии (особенно у детей). Назначается в инъекциях. Торговое название: кеталар (Ketalar). Источник: Медицинский словарь … Медицинские термины
-
Кетамина гидрохлорид — Кетамин (Ketamine) Химическое соединение … Википедия
-
NMDA-антагонист — Кетамин, распространённый NMDA антагонист Антагонисты NMDA рецептора, или NMDA антагонисты (иногда «НМДА антагонисты») класс анестетиков, ингибирующих д … Википедия
-
канемит — кетамин маетник митенка … Краткий словарь анаграмм
-
КЕТАМИНА ГИДРОХЛОРИД — ( Кеtamini hydrоchloridum ). 2 ( Метиламино) 2 (2 хлорфенил) циклокегсанона гидрохлорид. Синонимы: Калипсол, Кетажест, Кеталар, Kalipsol, Кеtаject, Кеtаlаr, Кеtaminе, Кеtапеst, Кеtо1аr, Vеtаlаr. Белый или почти белый кристаллический порошок со… … Словарь медицинских препаратов
-
Ketamini hydrochloridum — КЕТАМИНА ГИДРОХЛОРИД ( Кеtamini hydrоchloridum ). 2 ( Метиламино) 2 (2 хлорфенил) циклокегсанона гидрохлорид. Синонимы: Калипсол, Кетажест, Кеталар, Kalipsol, Кеtаject, Кеtаlаr, Кеtaminе, Кеtапеst, Кеtо1аr, Vеtаlаr. Белый или почти белый… … Словарь медицинских препаратов
-
Нейротоксичность NMDA-антагонистов — Термин Нейротоксичность NMDA антагонистов (англ. NMDA receptor antagonist neurotoxicity, NAN) описывает повреждения мозга, вызванные диссоциативными анестетиками, в особенности неконкурентными блокаторами канала NMDA рецептора. В их число… … Википедия
Кетамин (Ketamine)
💊 Состав препарата Кетамин
✅ Применение препарата Кетамин
Описание активных компонентов препарата
Кетамин
(Ketamine)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2020.11.24
Владелец регистрационного удостоверения:
Лекарственная форма
|
|
Кетамин |
Р-р д/в/в и в/м введения 100 мг/2 мл: амп. 5 шт. рег. №: Р N000298/01 |
Форма выпуска, упаковка и состав
препарата Кетамин
| Раствор для в/в и в/м введения | 1 мл | 1 амп. |
| кетамин (в форме гидрохлорида) | 50 мг | 100 мг |
2 мл — ампулы (5) — пачки картонные.
Фармакологическое действие
Средство для неингаляционного наркоза. Кетамин вызывает диссоциативную анестезию — состояние, при котором одни участки головного мозга возбуждаются, а другие — угнетаются, что объясняет проявление анальгезирующего эффекта при неполном угнетении сознания и сохранении спонтанного дыхания, глоточного, гортанного и кашлевого рефлексов (доза кетамина, вызывающая апноэ, в 8 раз выше гипнотической). Хирургическая стадия общей анестезии при использовании кетамина не развивается (висцеральная анальгезирующая активность кетамина недостаточна, что следует учитывать при полостных операциях).
Вызывает специфический комплекс симптомов: соматическую анальгезию, состояние, напоминающее нейролептанальгезию, повышает АД, сократимость миокарда, минутный объем крови и потребность миокарда в кислороде, расслабляет гладкую мускулатуру бронхов. Практически не снижает тонус скелетной мускулатуры, может вызывать непроизвольные мышечные подергивания.
У взрослых минимальная доза, вызывающая гипнотический эффект при однократном в/в введении, составляет 0.5 мг/кг массы тела (угнетение сознания длится 1.5 мин). В дозе 1 мг/кг угнетает сознание на 6 мин, в дозе 1.5 мг/кг — на 9 мин, в дозе 2 мг/кг — на 10-15 мин. При в/м введении 4-8 мг/кг эффект наступает через 2-4 мин (6-8 мин) и продолжается в среднем 12-25 мин (до 30-40 мин).
У детей при в/м введении общая анестезия наступает через 2-6 мин, при в/в — через 15-60 с, продолжительность действия — 15-30 мин и 5-15 мин соответственно.
Анальгезирующий эффект кетамина при соматической боли проявляется при назначении субнаркотических доз. Максимум анальгезирующего действия наступает через 10 мин после в/в введения и сохраняется в течение 2-3 ч, при в/м введении эффект более продолжительный.
Фармакокинетика
Кетамин является липофильным соединением и в связи с этим быстро распределяется в хорошо снабжаемые кровью органы, в т.ч. в мозг, а затем перераспределяется в ткани с пониженной перфузией, легко проникает через гистогематические барьеры, включая ГЭБ. Связь с белками плазмы достигает 12%.
Vd — 1.8-2 л/кг, T1/2 — 2-3 ч. Основная часть продуктов метаболизма выделяется в течение 2 ч с мочой. Основной причиной прекращения центрального действия кетамина является быстрое перераспределение препарата из мозга в другие ткани.
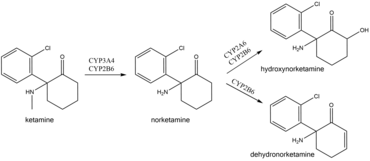
Биотрансформация кетамина осуществляется путем деметилирования печеночными микросомальными ферментами с образованием нескольких метаболитов, некоторые из них сохраняют 1/5-1/3 анестетической активности кетамина. Элиминация кетамина зависит от системы оксидаз гладкого эндоплазматического ретикулума. Главный метаболит, норкетамин, обладает некоторой гипнотической активностью, которая слабее, чем у кетамина. В процессе дальнейшего метаболизма кетамин и норкетамин превращаются в гидроксилированные производные, которые образуют конъюгаты с глюкуроновой кислотой и элиминируются из организма.
Незначительное количество метаболитов может оставаться в организме в течение нескольких дней, кумуляции при многократном введении не наблюдается. При многократных анестезиях кетамином может возникнуть толерантность к кетамину, что частично объясняют индукцией печеночных ферментов.
Показания активных веществ препарата
Кетамин
Вводная и базисная общая анестезия (особенно у больных с низким АД или при необходимости сохранения самостоятельного дыхания, либо при проведении искусственной вентиляции легких дыхательными смесями, не содержащими динитрогена оксид (закись азота)); экстренные хирургические вмешательства (в т.ч. на этапах эвакуации, в частности, у больных с травматическим шоком и кровопотерей); различные хирургические операции при многокомпонентной в/в анестезии; болезненные диагностические процедуры (эндоскопия, катетеризация камер сердца), небольшие хирургические манипуляции при ожогах, перевязках и тому подобных процедурах.
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Применяют в/м и в/в. Дозу, способ и схему применения устанавливают индивидуально, в зависимости от показаний, возраста и массы тела пациента, клинической ситуации, препаратов, применяемых для премедикации.
Побочное действие
Со стороны нервной системы: угнетение дыхательного центра, мышечная ригидность, непроизвольная мышечная активность (для профилактики следует предварительно ввести диазепам); в период выхода из общей анестезии — психомоторное возбуждение, галлюцинации, длительная дезориентация, психоз.
Со стороны органа зрения: диплопия, нистагм, повышение внутриглазного давления.
Со стороны дыхательной системы: одышка, обтурация верхних дыхательных путей из-за спазма жевательной мускулатуры и западания языка, повышенной бронхиальной секреции и саливации.
Со стороны сердечно-сосудистой системы: повышение АД, тахикардия.
Со стороны пищеварительной системы: гиперсаливация, тошнота.
Местные реакции: болезненность и гиперемия по ходу вены в месте введения.
Противопоказания к применению
Повышенная чувствительность к кетамину; артериальная гипертензия и состояния, сопровождающиеся повышенным АД; стенокардия, инфаркт миокарда (в т.ч. в последние 6 мес); хроническая почечная недостаточность; нарушение мозгового кровообращения (в т.ч. в анамнезе); преэклампсия; эпилепсия, в т.ч. в детском возрасте, эклампсия и другие судорожные состояния; алкоголизм.
С осторожностью: заболевания почек, декомпенсированная хроническая сердечная недостаточность, операции на гортани и глотке.
Применение при беременности и кормлении грудью
Кетамин проникает через плацентарный барьер. Безопасность применения кетамина при беременности не установлена. Применение у данной категории пациентов не рекомендуется.
При необходимости применения в период лактации следует решить вопрос о прекращении грудного вскармливания.
Применение при нарушениях функции почек
Противопоказано применение при хронической почечной недостаточности. С осторожностью применяют у пациентов с заболеваниями почек.
Применение у детей
Противопоказан при эпилепсии в детском возрасте. Дозы для детей устанавливают в соответствии с показаниями, из расчета на массу тела
Особые указания
Кетамин применяют только в условиях стационара или скорой помощи.
Для предупреждения усиления секреции слизистых оболочек и слюнных желез в состав средств премедикации следует включать атропин или метоциния йодид, а также медленно вводить основную дозу кетамина (не превышающую 3 мг/кг). Во время кетаминовой анестезии проводить ингаляцию смесью кислорода с воздухом в соотношении 1:2.
При использовании кетамина необходимо следить за функцией внешнего дыхания, особенно за проходимостью верхних дыхательных путей (возможны спазм жевательной мускулатуры и западение языка).
Следует соблюдать осторожность при операциях на гортани и глотке (применяют миорелаксанты).
Для профилактики мышечной ригидности и непроизвольных подергиваний при проведении премедикации в/м или в/в вводят диазепам.
Для предупреждения развития психотомиметического действия в состав средств премедикации следует включать дроперидол, диазепам.
После применения кетамина возможно повышение внутричерепного давления.
Применение кетамина может спровоцировать развитие острых психических нарушений при выведении из анестезии. Необходимо соблюдать осторожность пациентам с острыми нарушениями психики (также при наличии таких указаний в анамнезе), пациентам с алкогольной интоксикацией.
Возможно развитие кетаминовой зависимости у пациентов с наркотической зависимостью или ранее злоупотреблявших наркотическими веществами.
Влияние на способность к управлению транспортными средствами и механизмами
После применения кетамина по крайней мере в течение 24 ч пациентам следует воздерживаться от вождения автотранспорта и других потенциально опасных видов деятельности.
Лекарственное взаимодействие
Кетамин усиливает действие лекарственных средств для общей анестезии, наркотических анальгетиков, антипсихотических средств (нейролептиков), анксиолитиков (транквилизаторов) и других лекарственных средств, оказывающих угнетающее действие на ЦНС.
Перед применением кетамина необходимо отменить линкомицин, препараты лития (за 1-2 дня), ингибиторы МАО (за 15 дней). Нельзя смешивать в одном шприце с барбитуратами (фармацевтически несовместим — образование осадка).
Дроперидол и бензодиазепины, в т.ч. диазепам, ослабляют риск проявления психотомиметической и моторной активности, а также возникновения тахикардии и повышения артериального давления.
Не рекомендуется назначать кетамин одновременно с симпатомиметиками и лекарственными средствами, обладающими стимулирующим воздействием на сердечно-сосудистую систему (усиление гипертензивного и аритмогенного действия, повышение потребности миокарда в кислороде).
Кардиостимулирующий эффект кетамина ослабляется при комбинации с антипсихотическими средствами, анксиолитиками.
Кетамин усиливает миорелаксирующий эффект тубокурарина хлорида и суксаметония йодида, не изменяет — панкурония бромида.
Во время общей анестезии у пациентов, принимающих йодсодержащие препараты и гормоны щитовидной железы, высока вероятность повышения АД и тахикардии (устраняются бета-адреноблокаторами).
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Все действующие вещества
Содержание
- 1 Латинское название
- 2 Фармакологическая группа
- 3 Характеристика вещества
- 4 Фармакология
- 5 Применение
- 6 Кетамин: Противопоказания
- 7 Применение при беременности и кормлении грудью
- 8 Кетамин: Побочные действия
- 9 Взаимодействие
- 10 Кетамин: Способ применения и дозы
- 11 Меры предосторожности
- 12 Условия хранения
- 13 Торговые наименования
- 14 МКБ-10
Латинское название[править]
ketamine
Фармакологическая группа[править]
средство для в/в анестезии
Характеристика вещества[править]
Фармакология[править]
Фармакологическое действие — наркозное, анальгезирующее, снотворное.
Угнетает ассоциативную зону и подкорковые образования таламуса (диссоциативная анестезия). Легко проходит гистогематические барьеры, включая ГЭБ. В печени деметилируется, теряя активность. Основная часть продуктов биотрансформации выделяется в течение 2 ч с мочой, незначительное количество метаболитов остается в организме несколько дней. Кумуляции при многократном введении не отмечено. Особенностью наркотизирующего эффекта является быстрота наступления, малая длительность, сохранение в наркотической фазе самостоятельной адекватной вентиляции легких. Вызывает выраженную анальгезию. Плохо расслабляет скелетную мускулатуру; в фазе наркоза сохраняются глоточный, гортанный и кашлевой рефлексы. Не угнетает и даже стимулирует сердечно-сосудистую систему. Малотоксичен. Не обладает холино- и адреноблокирующими свойствами, а также антигистаминной активностью. При в/в введении 0,5 мг/кг сознание выключается через 1–2 мин на 2 мин, а анальгезия развивается в течение 10 мин и продолжается 2–3 ч. При в/м введении эффект наступает позже, но имеет большую длительность.
Применение[править]
Общая анестезия, анестезия при кратковременных операциях и перевязках.
Кетамин: Противопоказания[править]
Гиперчувствительность, нарушение мозгового кровообращения (в т.ч. в анамнезе), артериальная гипертензия, преэклампсия, эклампсия, алкоголизм, эпилепсия у детей, стенокардия, инфаркт миокарда (в т.ч. в последние 6 мес), состояния, сопровождающиеся повышенным АД, хроническая почечная недостаточность.
Применение при беременности и кормлении грудью[править]
Кетамин: Побочные действия[править]
Повышение АД, тахикардия, слюнотечение, тошнота, одышка, угнетение дыхательного центра, мышечная ригидность и повышение мышечной активности, обтурация верхних дыхательных путей из-за спазма жевательной мускулатуры и западения языка. В период выхода из состояния наркоза — галлюцинации, психомоторное возбуждение и длительная дезориентация, психоз. Болезненность и гиперемия по ходу вены в месте введения.
Взаимодействие[править]
Усиливает эффект ингаляционных наркозных средств. Углубляет миорелаксацию, вызываемую тубокурарина хлоридом и суксаметония йодидом, не изменяет — панкурония бромидом. Во время наркоза у пациентов, принимающих йодсодержащие препараты и гормоны щитовидной железы, высока вероятность развития артериальной гипертензии и тахикардии (устраняются бета-адреноблокаторами). Дроперидол и бензодиазепины, в т.ч. диазепам, ослабляют риск проявления психотомиметической и моторной активности, а также возникновения тахикардии и и повышения АД. Фармацевтически несовместим с барбитуратами.
Перед применением кетамина необходимо отменить линкомицин и препараты лития (за 1-2 дня).
Перед применением кетамина необходимо отменить ингибиторы МАО (за 15 дней).
Не рекомендуется назначать кетамин с симпатомиметиками и ЛС, обладающими стимулирующим воздействием на ССС (усиление гипертензивного и аритмогенного действия, повышение потребности миокарда в кислороде).
Кардиостимулирующий эффект кетамина ослабляется при комбинации с нейролептиками и анксиолитиками.
Кетамин: Способ применения и дозы[править]
Дети:
В/м: 3—7 мг/кг.
В/в. Вводная анестезия: 1—2 мг/кг. Премедикация: 0,5—1 мг/кг.
Взрослые
В/м: 3—8 мг/кг.
В/в, вводная анестезия: 1—2 мг/кг.
Дети и взрослые, поддержание анестезии: 1/3—1/2 дозы для вводной анестезии по мере необходимости.
Меры предосторожности[править]
Условия хранения[править]
Торговые наименования[править]
Кетамин: инъекционный раствор 100 мг в ампулах 2 мл. «Московский эндокринный завод (Россия)»
МКБ-10[править]
- R52 Боль, не классифицированная в других рубриках
- T30 Термические и химические ожоги неуточненной локализации
- Z100* КЛАСС XXII Хирургическая практика
Кетамин
Инструкция по применению, противопоказания, состав, цена, фото
Русское название
Кетамин
Латинское название вещества Кетамин
Ketaminum (род. Ketamini)
Химическое название
(±)-2-(2-Хлорфенил)-2-(метиламино)циклогексанон (в виде гидрохлорида)
Брутто-формула
C13H16ClNO
Фармакологическая группа вещества Кетамин
Наркозные средства
Нозологическая классификация (МКБ-10)
R52 Боль, не классифицированная в других рубриках
T30 Термические и химические ожоги неуточненной локализации
Z100* КЛАСС XXII Хирургическая практика
Код CAS
6740-88-1
Характеристика вещества Кетамин
Белый или почти белый кристаллический порошок со слабым характерным запахом. Легко растворим в воде и спирте, pH водных растворов 3,5–4,5.
Фармакологическое действие
Наркозное, анальгезирующее, снотворное.
Угнетает ассоциативную зону и подкорковые образования таламуса (диссоциативная анестезия). Легко проходит гистогематические барьеры, включая ГЭБ. В печени деметилируется, теряя активность. Основная часть продуктов биотрансформации выделяется в течение 2 ч с мочой, незначительное количество метаболитов остается в организме несколько дней. Кумуляции при многократном введении не отмечено. Особенностью наркотизирующего эффекта является быстрота наступления, малая длительность, сохранение в наркотической фазе самостоятельной адекватной вентиляции легких. Вызывает выраженную анальгезию. Плохо расслабляет скелетную мускулатуру; в фазе наркоза сохраняются глоточный, гортанный и кашлевой рефлексы. Не угнетает и даже стимулирует сердечно-сосудистую систему. Малотоксичен. Не обладает холино- и адреноблокирующими свойствами, а также антигистаминной активностью. При в/в введении 0,5 мг/кг сознание выключается через 1–2 мин на 2 мин, а анальгезия развивается в течение 10 мин и продолжается 2–3 ч. При в/м введении эффект наступает позже, но имеет большую длительность.
Применение вещества Кетамин
Вводный наркоз, базисный наркоз для обезболивания кратковременных операций и болезненных инструментальных вмешательств (в т.ч. в стоматологической, офтальмологической, оториноларингологической, гинекологической и акушерской практике, и диагностических процедур — эндоскопия, катетеризация сердца и др.), при проведении экстренных хирургических операций у больных с травматическим шоком и кровопотерей, обезболивание при транспортировке больных, при обработке ожоговой поверхности.
Противопоказания
Гиперчувствительность, нарушение мозгового кровообращения (в т.ч. в анамнезе), артериальная гипертензия, преэклампсия, эклампсия, алкоголизм, эпилепсия у детей.
- стенокардия, инфаркт миокарда (в т.ч. в последние 6 мес);
- состояния, сопровождающиеся повышенным АД;
- хроническая почечная недостаточность.
Ограничения к применению
Заболевания почек, декомпенсированная хроническая сердечная недостаточность, операции на гортани и глотке.
Побочные действия вещества Кетамин
Повышение АД, тахикардия, слюнотечение, тошнота, одышка, угнетение дыхательного центра, мышечная ригидность и повышение мышечной активности, обтурация верхних дыхательных путей из-за спазма жевательной мускулатуры и западения языка. В период выхода из состояния наркоза — галлюцинации, психомоторное возбуждение и длительная дезориентация, психоз. Болезненность и гиперемия по ходу вены в месте введения.
Взаимодействие
Усиливает эффект ингаляционных наркозных средств. Углубляет миорелаксацию, вызываемую тубокурарина хлоридом и суксаметония йодидом, не изменяет — панкурония бромидом. Во время наркоза у пациентов, принимающих йодсодержащие препараты и гормоны щитовидной железы, высока вероятность развития артериальной гипертензии и тахикардии (устраняются бета-адреноблокаторами). Дроперидол и бензодиазепины, в т.ч. диазепам, ослабляют риск проявления психотомиметической и моторной активности, а также возникновения тахикардии и и повышения АД. Фармацевтически несовместим с барбитуратами.
Взаимодействие с линкомицином и препаратами лития:
Перед применением кетамина необходимо отменить линкомицин и препараты лития (за 1-2 дня).
Взаимодействие с ингибиторами МАО:
Перед применением кетамина необходимо отменить ингибиторы МАО (за 15 дней).
Другие ЛС:
Не рекомендуется назначать кетамин с симпатомиметиками и ЛС, обладающими стимулирующим воздействием на ССС (усиление гипертензивного и аритмогенного действия, повышение потребности миокарда в кислороде).
Кардиостимулирующий эффект кетамина ослабляется при комбинации с нейролептиками и анксиолитиками.
Взаимодействия с другими действующими веществами
Алпразолам:
Усиливает (взаимно) угнетение ЦНС.
Атракурия безилат:
Кетамин при совместном применении с атракурия безилатом усиливает нервно-мышечную блокаду.
Бупренорфин:
Усиливает (взаимно) угнетение ЦНС.
Вальпроевая кислота:
На фоне вальпроевой кислоты усиливается угнетение ЦНС.
Галоперидол:
Кетамин усиливает (взаимно) угнетение ЦНС.
Галотан:
При совместном с галотаном применении кетамин увеличивает период его полувыведения.
Гидроксизин:
На фоне гидроксизина усиливается депримирующий эффект и требуются меньшие дозы наркозных средств (во избежание тяжелых осложнений).
Гуанфацин:
На фоне гуанфацина усиливаются эффекты.
Дапоксетин:
Пациентам следует рекомендовать не принимать дапоксетин вместе с кетамином. Одновременное применение дапоксетина с кетамином, обладающим серотонинергической активностью, может приводить к потенциально серьезным реакциям, включая в т.ч. аритмию, гипертермию и серотониновый синдром.
Диазепам:
При одновременном применении с кетамином диазепам ослабляет риск проявления психотомиметической и моторной активности, а также возникновения тахикардии и повышения АД.
Дифенгидрамин:
Усиливает (взаимно) угнетение ЦНС.
Дроперидол:
Возможно сочетанное использование кетамина с дроперидолом. При одновременном применении с кетамином дроперидол ослабляет риск проявления психотомиметической и моторной активности, а также возникновения тахикардии и повышения АД.
Клоназепам:
Потенцирование угнетения ЦНС.
Левотироксин натрия:
На фоне левотироксина натрия повышается вероятность гипертензии и тахикардии.
Линкомицин:
Перед применением кетамина необходимо отменить линкомицин (за 1–2 дня).
Лиотиронин:
Кетамин повышает концентрацию в крови и риск развития побочных эффектов.
Мемантин:
Сочетанное применение мемантина и кетамина не рекомендуется (увеличивается риск токсического действия на ЦНС).
Метилдопа:
На фоне метилдопы усиливается эффект: для наркоза может потребоваться меньшая доза.
Метоклопрамид:
Кетамин усиливает седацию, ослабляет стимуляцию двигательной активности ЖКТ.
Мивакурия хлорид:
Кетамин усиливает эффект (нервно-мышечную блокаду).
Мидазолам:
Совместное введение мидазолама с кетамином может привести к усилению седативного и снотворного эффектов.
Морфин:
Кетамин усиливает (взаимно) эффект (в т.ч. угнетение дыхания).
Прометазин:
Кетамин усиливает и пролонгирует (взаимно) седативный эффект. На фоне прометазина используется меньшая доза.
Рисперидон:
При совместном использовании необходима осторожность.
Рокурония бромид:
Действие рокурония бромида усиливается при введении в высоких дозах кетамина.
Суксаметония йодид:
При одновременном применении кетамин усиливает миорелаксирующий эффект суксаметония йодида.
Тиопентал натрий:
Кетамин при сочетанном применении с тиопенталом натрия повышает риск снижения АД и угнетения дыхания. Тиопентал натрия фармацевтически несовместим (нельзя смешивать в одном шприце) с кетамином.
Топирамат:
Усиливает (взаимно) угнетение ЦНС.
Трамадол:
Усиливает (взаимно) эффект; при одновременном или последовательном назначении необходима осторожность.
Тубокурарина хлорид:
При одновременном применении кетамин усиливает миорелаксирующий эффект тубокурарина хлорида.
Ципрогептадин:
При сочетанном применении кетамин усиливает депримирующий эффект ципрогептадина: в постнаркозном периоде снижается скорость психомоторных реакций и ухудшается функционирование ЦНС. На фоне ципрогептадина для наркоза могут потребоваться меньшие дозы.
Цисатракурия безилат:
При сочетанном применении кетамин усиливает эффект цисатракурия безилата.
Способ применения и дозы
В/в, взрослым — в дозе 1–4 мг/кг, детям — 0,5–4,5 мг/кг. Начальная доза для получения наркозного эффекта — 0,7–2 мг/кг, вводится медленно в течение 60 с, средняя доза для анестезии продолжительностью 5–10 мин — 2 мг/кг, при повторном введении применяют 1/2–1/3 первоначальной дозы или используют капельное введение 0,1% раствора (на физиологическом растворе или растворе глюкозы) со скоростью 20–60 капель в минуту; ослабленным больным, пожилым и больным в шоковом состоянии вводят в дозе 0,5 мг/кг, общая вводимая доза для взрослых составляет 2–6 мг/кг/ч.
В/м, доза 6,5–13 мг/кг (для детей — 2–5 мг/кг) вызывает наркоз продолжительностью 12–25 мин.
Внимание: данная информация может не являться актуальной на момент прочтения. Актуальные версии РЛС всегда ищите в упаковке с препаратом.
Запрещено использование материалов сайта без консультации со специалистом.
Комментарии:
For the functional group referred to as ketimine, see Imine.
 |
|
 |
|
| Clinical data | |
|---|---|
| Trade names | Ketalar, others |
| Other names | CI-581; CL-369; CM-52372-2[1] |
| AHFS/Drugs.com | Monograph |
| License data |
|
| Pregnancy category |
|
| Addiction liability |
Low–moderate[3] |
| Routes of administration |
Any[4][5][6][7] |
| Drug class | NMDA receptor antagonists; General anesthetics; Dissociative hallucinogens; Analgesics; Antidepressants |
| ATC code |
|
| Legal status | |
| Legal status |
|
| Pharmacokinetic data | |
| Bioavailability |
|
| Protein binding | 23 to 47%.[12] |
| Metabolism | Liver, intestine (oral):[6][16][17]
|
| Metabolites |
|
| Onset of action |
|
| Elimination half-life |
|
| Duration of action |
|
| Excretion |
|
| Identifiers | |
|
IUPAC name
|
|
| CAS Number |
|
| PubChem CID |
|
| IUPHAR/BPS |
|
| DrugBank |
|
| ChemSpider |
|
| UNII |
|
| KEGG |
|
| ChEBI |
|
| ChEMBL |
|
| CompTox Dashboard (EPA) |
|
| ECHA InfoCard | 100.027.095 |
| Chemical and physical data | |
| Formula | C13H16ClNO |
| Molar mass | 237.73 g·mol−1 |
| 3D model (JSmol) |
|
| Chirality | Racemic mixture:[13]
|
| Melting point | 92[18] °C (198 °F) |
|
SMILES
|
|
|
InChI
|
|
| (verify) |
Ketamine is a dissociative anesthetic used medically for induction and maintenance of anesthesia. It is also used as a recreational drug. Ketamine is also simple to administer and highly tolerable compared to drugs with similar effects which are flammable, irritating, or even explosive. Ketamine is a novel compound, derived from PCP, created in pursuit of a safer anesthetic with similar characteristics. Ketamine is also used for acute pain management.[19][20]
At anesthetic doses, ketamine induces a state of «dissociative anesthesia», a trance-like state providing pain relief, sedation, and amnesia.[21] The distinguishing features of ketamine anesthesia are preserved breathing and airway reflexes, stimulated heart function with increased blood pressure, and moderate bronchodilation.[21] At lower, sub-anesthetic doses, ketamine is a promising agent for pain and treatment-resistant depression.[22] However, the antidepressant action of a single administration of ketamine wanes with time. The long-term effects of repeated use are largely unknown, and are an area of active investigation.[23][24][25]
Liver and urinary toxicity have been reported among regular users of high doses of ketamine for recreational purposes.[26] Ketamine is an NMDA receptor pore blocker and that accounts for most of its actions except the antidepressive effect, the mechanism of which is a matter of much research and debate.
Ketamine was first synthesized in 1962 and approved for use in the United States in 1970. It has been regularly used in veterinary medicine and was extensively used for surgical anaesthesia in the Vietnam War.[27] When used as a recreational drug, it is found both in powder and liquid form, and is often referred to as «Special K» for its hallucinogenic and dissociative effects.[28] Along with other psychotropic drugs, it is on the World Health Organization’s List of Essential Medicines.[29] It is available as a generic medication.[30]
Medical uses[edit]
Anesthesia[edit]
The use of ketamine in anesthesia reflects its characteristics. It is a drug of choice for short-term procedures when muscle relaxation is not required.[31] The effect of ketamine on the respiratory and circulatory systems is different from that of other anesthetics. It suppresses breathing much less than most other available anesthetics.[32] When used at anesthetic doses, ketamine usually stimulates rather than depresses the circulatory system.[33] Protective airway reflexes are preserved[34] and it is sometimes possible to administer ketamine anesthesia without protective measures to the airways.[31] Psychotomimetic effects limit the acceptance of ketamine; however, lamotrigine[35] and nimodipine[36] decrease psychotomimetic effects and can be counteracted also by benzodiazepines administered or propofol.[37]
Ketamine is frequently used in severely injured people and appears to be safe in this group.[38] It has been widely used for emergency surgery in field conditions in war zones,[39] for example, during the Vietnam War.[40] A 2011 clinical practice guideline supports the use of ketamine as a sedative in emergency medicine, including during physically painful procedures.[21] It is the drug of choice for people in traumatic shock who are at risk of hypotension.[41] Low blood pressure is dangerous for people with severe head injury[42] and ketamine is unlikely to lower blood pressure — conversely, often raising blood pressure, making it often the best suited for those with severe head injury.[43][44]
Ketamine is an option in children, as the sole anesthetic for minor procedures or as an induction agent followed by neuromuscular blocker and tracheal intubation[39] In particular, children with cyanotic heart disease and neuromuscular disorders are good candidates for ketamine anesthesia.[37]
Due to the bronchodilating properties of ketamine, it can be used for anesthesia in people with asthma, chronic obstructive airway disease, and with severe reactive airway disease including active bronchospasm.[39][37][45]
Pain[edit]
Ketamine infusions are used for acute pain treatment in emergency departments and in the perioperative period in individuals with refractory pain. The doses are lower than those used for anesthesia; they are usually referred to as sub-anesthetic doses. Adjunctive to morphine or on its own, ketamine reduces morphine use, pain level, nausea, and vomiting after surgery. Ketamine is likely to be most beneficial for surgical patients when severe post-operative pain is expected and for opioid-tolerant patients.[46][47]
Ketamine is especially useful in the prehospital setting, due to its effectiveness and low risk of respiratory depression.[48]
Ketamine has similar efficacy to opioids in a hospital emergency department setting for management of acute pain and for control of procedural pain.[49] It may also prevent opioid-induced hyperalgesia[50][51] and postanesthetic shivering.[52]
For chronic pain, ketamine is used as an intravenous analgesic, particularly, if the pain is neuropathic.[20] It has the added benefit of counteracting spinal sensitization or wind-up phenomena experienced with chronic pain.[53] In multiple clinical trials, ketamine infusions delivered short-term pain relief in neuropathic pain diagnoses, pain after traumatic spine injury, fibromyalgia, and complex regional pain syndrome (CRPS).[20] However, the 2018 consensus guidelines on chronic pain concluded that, overall, there is only weak evidence in favor of ketamine use in spinal injury pain, moderate evidence in favor of ketamine for CRPS, and weak or no evidence for ketamine in mixed neuropathic pain, fibromyalgia, and cancer pain. In particular, only for CRPS there is evidence of medium to longer term pain relief.[20]
Depression[edit]
Ketamine is a robust and rapid-acting[54] antidepressant, although its effect is transient.[55] Intravenous ketamine infusion in treatment resistant depression may result in improved mood within 4 hours reaching the peak at 24 hours.[22][23] A single dose of intravenous ketamine has been shown to result in a response rate greater than 60% as early as 4.5 hours after the dose (with a sustained effect after 24 hours) and greater than 40% after 7 days.[56] Although there are only a few pilot studies studying the optimal dose, increasing evidence suggests that 0.5 mg/kg dose injected over 40 minutes gives an optimal outcome.[57] The antidepressant effect of ketamine is diminished at 7 days, and most people relapse within 10 days, although for a significant minority the improvement may last 30 days and longer.[23][24][56][58] One of the main challenges with ketamine treatment can be the length of time that the antidepressant effects lasts after finishing a course of treatment. A possible option may be maintenance therapy with ketamine which usually runs twice a week to once in two weeks.[23][24][25] Ketamine may decrease suicidal thoughts for up to three days after the injection.[59]
An enantiomer of ketamine – esketamine commercially sold as Spravato – was approved as an antidepressant by the European Medicines Agency in 2019.[60] Esketamine was approved as a nasal spray for treatment-resistant depression in the United States[61] and elsewhere in 2019 (see Esketamine and Depression). The Canadian Network for Mood and Anxiety Treatments (CANMAT) recommends esketamine as a third-line treatment for depression.[24]
A Cochrane review of randomized controlled trials in adults with unipolar major depressive disorder, found that when compared with placebo, people treated with either ketamine or esketamine experienced reduction or remission of symptoms lasting 1 to 7 days.[62] There were 18.7% (4.1 to 40.4%) more people reporting some benefit and 9.6% (0.2 to 39.4%) more who achieved remission within 24-hours of ketamine treatment. Among people receiving esketamine, 2.1% (2.5 to 24.4%) more encountered some relief at 24-hours and 10.3% (4.5 to 18.2%) more had few or no symptoms. These effects did not persist beyond one week, although higher dropout rate in some studies mean that the duration of benefit remains unclear.[62]
Ketamine may partially improve depressive symptoms among people with bipolar depression, at 24 hours after treatment, but not 3 or more days.[63] Potentially, 10 more people with bipolar depression per 1000 may experience brief improvement, but not cessation of symptoms, one day following treatment. These estimates are based on limited available research.[63]
In February 2022, the US Food and Drug Administration issued an alert to health care professionals concerning compounded nasal spray products containing ketamine intended to treat depression: «There is no FDA-approved ketamine nasal spray product. Compounded drugs are not FDA-approved, which means FDA has not evaluated their safety, effectiveness, or quality prior to marketing.»[64]
Near-death experience[edit]
Most people who were able to remember their dreams during ketamine anesthesia report near-death experiences (NDE) when the widest possible definition of an NDE is used.[65] Ketamine can reproduce features that commonly have been associated with NDEs.[66] A 2019 large-scale study found that written reports of ketamine experiences had a high degree of similarity to written reports of NDE in comparison to other written reports of drug experiences.[67]
Seizures[edit]
Ketamine is used to treat status epilepticus that has not responded to standard treatments, but only case studies and no randomized controlled trials support its use.[68][69]
Contraindications[edit]
Main contraindications for ketamine:[20][46]
- Severe cardiovascular disease such as unstable angina or poorly controlled hypertension
- Increased intracranial or intraocular pressure. Both of these contraindications are controversial [46]
- Poorly controlled psychosis
- Severe liver disease such as cirrhosis
- Pregnancy
- Active substance use disorder (for serial ketamine injections)
- Age less than 3 months [10]
Side effects[edit]
At anesthetic doses, 10–20% of adults (1–2% of children)[10] experience adverse psychiatric reactions that occur during emergence from anesthesia, ranging from dreams and dysphoria to hallucinations and emergence delirium.[70] Psychotomimetic effects decrease adding lamotrigine[35] and nimodipine[36] and can be counteracted by pretreatment with a benzodiazepine or propofol.[70][37] Ketamine anesthesia commonly causes tonic-clonic movements (greater than 10% of people) and rarely hypertonia.[14][70] Vomiting can be expected in 5–15% of the patients; pretreatment with propofol mitigates it as well.[10][70] Laryngospasm occurs only rarely with ketamine. Ketamine, generally, stimulates breathing; however, in the first 2–3 minutes of a high-dose rapid intravenous injection it may cause a transient respiratory depression.[70]
At lower sub-anesthetic doses, psychiatric side effects are prominent. Most people feel strange, spacey, woozy, or a sense of floating, or have visual distortions or numbness. Also very frequent (20–50%) are difficulty speaking, confusion, euphoria, drowsiness, and difficulty concentrating. The symptoms of psychosis such as going into a hole, disappearing, feeling as if melting, experiencing colors, and hallucinations are described by 6–10% of people. Dizziness, blurred vision, dry mouth, hypertension, nausea, increased or decreased body temperature, or feeling flushed are the common (>10%) non-psychiatric side effects. All these adverse effects are most pronounced by the end of the injection, dramatically reduced 40 minutes afterward, and completely disappear within 4 hours after the injection.[71]
Urinary and liver toxicity[edit]
Urinary toxicity occurs primarily in people who use large amounts of ketamine routinely, with 20–30% of frequent users having bladder complaints.[20][72] It includes a range of disorders from cystitis to hydronephrosis to kidney failure.[73] The typical symptoms of ketamine-induced cystitis are frequent urination, dysuria, and urinary urgency sometimes accompanied by pain during urination and blood in urine.[74] The damage to the bladder wall has similarities to both interstitial and eosinophilic cystitis. The wall is thickened and the functional bladder capacity is as low as 10–150 mL.[73]
Management of ketamine-induced cystitis involves ketamine cessation as the first step. This is followed by NSAIDs and anticholinergics and, if the response is insufficient, by tramadol. The second line treatments are epithelium-protective agents such as oral pentosan polysulfate or intravesical (intra-bladder) instillation of hyaluronic acid. Intravesical botulinum toxin is also useful.[73]
Liver toxicity of ketamine involves higher doses and repeated administration. In a group of chronic high dose ketamine users, the frequency of liver injury was reported to be about 10%. There are case reports of increased liver enzymes involving ketamine treatment of chronic pain.[73]
Dependence and tolerance[edit]
Although the incidence of ketamine dependence is unknown, some people who regularly use ketamine develop ketamine dependence. Animal experiments also confirm the risk of misuse.[28] Additionally, the rapid onset of effects following insufflation may increase potential use as a recreational drug. The short duration of effects promotes bingeing. Ketamine tolerance rapidly develops, even with repeated medical use, prompting the use of higher doses. Some daily users reported withdrawal symptoms, primarily anxiety, shaking, sweating, and palpitations, following the attempts to stop.[28] Cognitive deficits as well as increased dissociation and delusion symptoms were observed in frequent recreational users of ketamine.[75]
Interactions[edit]
Ketamine potentiates the sedative effects of propofol[76] and midazolam.[77] Naltrexone potentiates psychotomimetic effects of a low dose of ketamine,[78] while lamotrigine[35] and nimodipine[36] decrease them. Clonidine reduces the increase of salivation, heart-rate and blood-pressure during ketamine anesthesia and decreases the incidence of nightmares.[79]
Clinical observations suggest that benzodiazepines may diminish the antidepressant effects of ketamine.[80] It appears most conventional antidepressants can be safely combined with ketamine.[80]
Pharmacology[edit]
Pharmacodynamics[edit]
Mechanism of action[edit]
Pore blocking of the NMDA receptor is responsible for the anesthetic, analgesic, and psychotomimetic effects of ketamine.[81][82] Block of NMDA receptor results in analgesia by preventing central sensitization in dorsal horn neurons; in other words, ketamine’s actions interfere with pain transmission in the spinal cord.[14]
The mechanism of action of ketamine in alleviating depression is not well understood, and is an area of active investigation. Possible mechanisms include direct action on the NMDA receptor, downstream effects on regulators such as BDNF and mTOR, and effects of ketamine’s metabolites such as hydroxynorketamine.[83] It is not clear whether NMDA receptor is solely responsible for this action or interactions with other receptors are also necessary. It is not also not clear whether ketamine alone is sufficient for the antidepressive action or its metabolites also are important.[81][84][85] In any case, it has been elucidated that acute blockade of NMDA receptors in the brain results in an activation of α-amino-3-hydroxy-5-methyl-4-isoxazolepropionic acid receptors (AMPA receptors), which in turn modulate a variety of downstream signaling pathways to influence neurotransmission in the limbic system and mediate antidepressant effects of NMDA receptor antagonists like ketamine.[56][84] Such downstream actions of this activation of AMPA receptors include upregulation of brain-derived neurotrophic factor (BDNF) and activation of its signaling receptor tropomyosin receptor kinase B (TrkB), activation of the mammalian target of rapamycin (mTOR) pathway, deactivation of glycogen synthase kinase 3 (GSK-3), and inhibition of the phosphorylation of the eukaryotic elongation factor 2 (eEF2) kinase.[56][84][86][87] In addition to blockade of the NMDA receptor, the active metabolite of ketamine hydroxynorketamine, which does not interact importantly with the NMDA receptor, but nonetheless indirectly activates AMPA receptors similarly, may also or alternatively be involved in the rapid-onset antidepressant effects of ketamine.[84][85] Recent research has elucidated that an acute inhibition of the lateral habenula, a part of the brain in the limbic system that has been referred to as the «anti-reward center» (projecting to and inhibiting the mesolimbic reward pathway and modulating other limbic areas), may be involved in the antidepressant effects of ketamine.[84][88][89]
Ketamine is a mixture of equal amounts of two enantiomers: esketamine and arketamine. Esketamine is a more potent NMDA receptor pore blocker and dissociative hallucinogen than arketamine.[11] Because of the hypothesis that NMDA receptor antagonism underlies the antidepressant effects of ketamine, esketamine was developed as an antidepressant.[11] However, multiple other NMDA receptor antagonists, including memantine, lanicemine, rislenemdaz, rapastinel, and 4-chlorokynurenine, thus far have failed to demonstrate sufficient effectiveness for depression.[11][90] Furthermore, animal research indicates that arketamine, the enantiomer with a weaker NMDA receptor antagonism, as well as (2R,6R)-hydroxynorketamine, the metabolite with negligible affinity for the NMDA receptor, but a potent alpha-7 nicotinic receptor antagonist may have antidepressive action.[11][91] It is now argued that NMDA receptor antagonism may not be primarily responsible for the antidepressant effects of ketamine.[11][92][90]
Molecular targets[edit]
| Site | Value (μM) | Type | Action | Species | Ref |
|---|---|---|---|---|---|
| NMDA | 0.25–0.66 | Ki | Antagonist | Human | [93][94] |
| MOR | 42 | Ki | Antagonist | Human | [95] |
| MOR2 | 12.1 | Ki | Antagonist | Human | [96] |
| KOR | 28 25 |
Ki Ki |
Antagonist Agonist |
Human | [95] [97] |
| σ2 | 26 | Ki | ND | Rat | [98] |
| D2 | 0.5 >10 |
Ki Ki |
Agonist ND |
Human | [99] [94][100][101] |
| M1 | 45 | Ki | ND | Human | [102] |
| α2β2 | 92 | IC50 | Antagonist | Human | [103] |
| α2β4 | 29 | IC50 | Antagonist | Human | [103] |
| α3β2 | 50 | IC50 | Antagonist | Human | [103] |
| α3β4 | 9.5 | IC50 | Antagonist | Human | [103] |
| α4β2 | 72 | IC50 | Antagonist | Human | [103] |
| α4β4 | 18 | IC50 | Antagonist | Human | [103] |
| α7 | 3.1 | IC50 | Antagonist | Rat | [91] |
| ERα | 0.34 | Ki | ND | Human | [104] |
| NET | 82–291 | IC50 | Inhibitor | Human | [105][106] |
| DAT | 63 | Ki | Inhibitor | Rat | [105] |
| HCN1 | 8–16 | EC50 | Inhibitor | Mouse | [107] |
| TRPV1 | 1-100 | Ki | Agonist | Rat | [108] |
| The smaller the value, the stronger the interaction with the site. |
Ketamine principally acts as a pore blocker of the NMDA receptor, an ionotropic glutamate receptor.[109] The S(+) and R(–) stereoisomers of ketamine bind to the dizocilpine site of the NMDA receptor with different affinities, the former showing approximately 3- to 4- fold greater affinity for the receptor than the latter. As a result, the S isomer is a more potent anesthetic and analgesic than its R counterpart.[110]
Ketamine may interact with and inhibit the NMDAR via another allosteric site on the receptor.[111]
With a couple of exceptions, ketamine actions at other receptors are far weaker than ketamine’s antagonism of the NMDA receptor (see the activity table to the right).[6][112]
Although ketamine is a very weak ligand of the monoamine transporters (Ki > 60 μM), it has been suggested that it may interact with allosteric sites on the monoamine transporters to produce monoamine reuptake inhibition.[94] However, no functional inhibition (IC50) of the human monoamine transporters has been observed with ketamine or its metabolites at concentrations of up to 10,000 nM.[100][109] Moreover, animal studies and at least three human case reports have found no interaction between ketamine and the monoamine oxidase inhibitor (MAOI) tranylcypromine, which is of importance as the combination of a monoamine reuptake inhibitor with an MAOI can produce severe toxicity such as serotonin syndrome or hypertensive crisis.[113][114] Collectively, these findings shed doubt on the involvement of monoamine reuptake inhibition in the effects of ketamine in humans.[113][109][100][114] Ketamine has been found to increase dopaminergic neurotransmission in the brain, but instead of being due to dopamine reuptake inhibition, this may be via indirect/downstream mechanisms, namely through antagonism of the NMDA receptor.[109][100]
Whether ketamine is an agonist of D2 receptors is controversial. Early research by the Philip Seeman group found ketamine to be a D2 partial agonist with the potency similar to that of its NMDA receptor antagonism.[99][115][116] However, later studies by different researchers found the affinity of ketamine of >10 μM for the regular human and rat D2 receptors,[94][100][101] Moreover, whereas D2 receptor agonists such as bromocriptine are able to rapidly and powerfully suppress prolactin secretion,[117] subanesthetic doses of ketamine have not been found to do this in humans and in fact, have been found to dose-dependently increase prolactin levels.[118][119] Imaging studies have shown mixed results on inhibition of striatal [11C] raclopride binding by ketamine in humans, with some studies finding a significant decrease and others finding no such effect.[120] However, changes in [11C] raclopride binding may be due to changes in dopamine concentrations induced by ketamine rather than binding of ketamine to the D2 receptor.[120]
Relationships between levels and effects[edit]
Dissociation and psychotomimetic effects are reported in people treated with ketamine at plasma concentrations of approximately 100 to 250 ng/mL (0.42–1.1 μM).[81] The typical intravenous antidepressant dosage of ketamine used to treat depression is low and results in maximal plasma concentrations of 70 to 200 ng/mL (0.29–0.84 μM).[55] At similar plasma concentrations (70 to 160 ng/mL; 0.29–0.67 μM) it also shows analgesic effects.[55] In 1–5 minutes after inducing anesthesia by a rapid intravenous injection of ketamine, its plasma concentration reaches as high as 60–110 μM.[121][122] When the anesthesia was maintained using nitrous oxide together with continuous injection of ketamine, the ketamine concentration stabilized at approximately 9.3 μM.[121] In an experiment with purely ketamine anesthesia, people began to awaken once the plasma level of ketamine decreased to about 2,600 ng/mL (11 μM) and became oriented in place and time when the level was down to 1,000 ng/mL (4 μM).[123] In a single-case study, the concentration of ketamine in cerebrospinal fluid, a proxy for the brain concentration, during anesthesia varied between 2.8 and 6.5 μM and was approximately 40% lower than in plasma.[124]
Pharmacokinetics[edit]
Ketamine can be absorbed by many different routes due to both its water and lipid solubility. Intravenous ketamine bioavailability is 100% by definition, intramuscular injection bioavailability is slightly lower at 93%,[6] and epidural bioavailability is 77%.[9] Subcutaneous bioavailability has never been measured, but is presumed to be high.[8] Among the less invasive routes, the intranasal route has the highest bioavailability (45–50%)[6][10] and oral – the lowest (16–20%).[6][10] Sublingual and rectal bioavailabilities are intermediate at approximately 25–50%.[6][11][10]
After absorption ketamine is rapidly distributed into the brain and other tissues.[82] The plasma protein binding of ketamine is variable at 23 to 47%.[12]
Major routes of ketamine metabolism.[81]
In the body ketamine undergoes extensive metabolism. It is biotransformed by CYP3A4 and CYP2B6 isoenzymes into norketamine, which, in turn, is converted by CYP2A6 and CYP2B6 into hydroxynorketamine and dehydronorketamine.[81] Low oral bioavailability of ketamine is due to the first-pass effect and, possibly, ketamine intestinal metabolism by CYP3A4.[17] As a result, norketamine plasma levels are several-fold higher than ketamine following oral administration, and norketamine may play a role in anesthetic and analgesic action of oral ketamine.[6][17] This also explains why oral ketamine levels are independent of CYP2B6 activity, unlike subcutaneous ketamine levels.[17][125]
After an intravenous injection of tritium-labelled ketamine, 91% of the radioactivity is recovered from urine and 3% from the feces.[15] The medication is excreted mostly in the form of metabolites, with only 2% remaining unchanged. Conjugated hydroxylated derivatives of ketamine (80%) followed by dehydronorketamine (16%) are the most prevalent metabolites detected in urine.[27]
Chemistry[edit]
Synthesis[edit]
2-chlorobenzonitrile is reacted with the Grignard reagent cyclopentylmagnesium bromide to give (2-chlorophenyl)(cyclopentyl)methanone. This is then brominated using bromine to form the corresponding bromoketone, which is then reacted with methylamine in an aqueous solution to form the methylimino derivative, 1-(2-Chloro-N-methylbenzimidoyl)cyclopentanol, with hydrolysis of the tertiary bromine atom. This final intermediate is then heated in decalin or another suitable high-boiling solvent, upon which an Alpha-ketol rearrangement occurs resulting in a ring-expansion, and the formation of racemic ketamine.
Preparation of Ketamine.[126]
Structure[edit]
(S)-ketamine
(R)-ketamine
In chemical structure, ketamine is an arylcyclohexylamine derivative. Ketamine is a chiral compound. The more active enantiomer, esketamine (S-ketamine), is also available for medical use under the brand name Ketanest S,[127] while the less active enantiomer, arketamine (R-ketamine), has never been marketed as an enantiopure drug for clinical use. While S-ketamine is more effective as an analgesic and anesthetic through NMDA receptor antagonism, R-ketamine produces longer-lasting effects as an antidepressant.
The optical rotation of a given enantiomer of ketamine can vary between its salts and free base form. The free base form of (S)‑ketamine exhibits dextrorotation and is therefore labelled (S)‑(+)‑ketamine. However, its hydrochloride salt shows levorotation and is thus labelled (S)‑(−)‑ketamine hydrochloride.[128]
Detection[edit]
Ketamine may be quantitated in blood or plasma to confirm a diagnosis of poisoning in hospitalized people, provide evidence in an impaired driving arrest, or to assist in a medicolegal death investigation. Blood or plasma ketamine concentrations are usually in a range of 0.5–5.0 mg/L in persons receiving the drug therapeutically (during general anesthesia), 1–2 mg/L in those arrested for impaired driving and 3–20 mg/L in victims of acute fatal overdosage. Urine is often the preferred specimen for routine drug use monitoring purposes. The presence of norketamine, a pharmacologically active metabolite, is useful for confirmation of ketamine ingestion.[129][130][131]
History[edit]
Ketamine was first synthesized in 1962 by Calvin L. Stevens, a professor of chemistry at Wayne State University and a Parke-Davis consultant. It was known by the developmental code name CI-581. After promising preclinical research in animals, ketamine was tested in human prisoners in 1964.[27] These investigations demonstrated ketamine’s short duration of action and reduced behavioral toxicity made it a favorable choice over phencyclidine (PCP) as an anesthetic.[132] The researchers wanted to call the state of ketamine anesthesia «dreaming», but Parke-Davis did not approve of the name. Hearing about this problem and about the «disconnected» appearance of treated people, Mrs. Edward F. Domino,[133] the wife of one of the pharmacologists working on ketamine, suggested «dissociative anesthesia».[27] Following FDA approval in 1970, ketamine anesthesia was first given to American soldiers during the Vietnam War.[134]
The discovery of antidepressive action of ketamine in 2000 [135] has been described as the single most important advance in the treatment of depression in more than 50 years.[58][11] It has sparked interest in NMDA receptor antagonists for depression,[136] and has shifted the direction of antidepressant research and development.[137]
Society and culture[edit]
Legal status[edit]
While ketamine is marketed legally in many countries worldwide,[138] it is also a controlled substance in many countries.[6]
- In Australia, ketamine is listed as a schedule 8 controlled drug under the Poisons Standard (October 2015).[139]
- In Canada, ketamine is classified as a Schedule I narcotic, since 2005.[140]
- In December 2013, the government of India, in response to rising recreational use and the use of ketamine as a date rape drug, has added it to Schedule X of the Drug and Cosmetics Act requiring a special license for sale and maintenance of records of all sales for two years.[141][142]
- In the United Kingdom, it became labeled a Class B drug on 12 February 2014.[143][144]
- The increase in recreational use prompted ketamine to be placed in Schedule III of the United States Controlled Substance Act in August 1999.[145]
Recreational use[edit]
At sub-anesthetic doses ketamine produces a dissociative state, characterised by a sense of detachment from one’s physical body and the external world that is known as depersonalization and derealization.[146] At sufficiently high doses, users may experience what is called the «K-hole», a state of dissociation with visual and auditory hallucination.[147] John C. Lilly, Marcia Moore, D. M. Turner, and David Woodard (amongst others) have written extensively about their own entheogenic and psychonautic experiences with ketamine.[148] Turner died prematurely due to drowning during presumed unsupervised ketamine use.[149] In 2006 the Russian edition of Adam Parfrey’s Apocalypse Culture II was banned and destroyed by authorities owing to its inclusion of an essay by Woodard about the entheogenic use of, and psychonautic experiences with, ketamine.[150]: 288–295
Recreational ketamine use has been implicated in deaths globally, with more than 90 deaths in England and Wales in the years of 2005–2013.[151] They include accidental poisonings, drownings, traffic accidents, and suicides.[151] The majority of deaths were among young people.[152] Because of its ability to cause confusion and amnesia, ketamine has been used for date rape.[153][134]
Research[edit]
Ketamine is under investigation for its potential in treating treatment-resistant depression.[154][155][156] Ketamine is a known psychoplastogen, which refers to a compound capable of promoting rapid and sustained neuroplasticity.[157]
A phase 2 clinical study showed that ketamine can safely and effectively reduce levodopa-induced dyskinesia in patients with Parkinson’s disease.[158] A phase II clinical trial is underway to test the use of ketamine as an antidepressant for patients with Parkinson’s disease.[159][160]
Veterinary medicine[edit]
In veterinary anaesthesia, ketamine is often used for its anaesthetic and analgesic effects on cats,[161] dogs,[162] rabbits, rats, and other small animals.[163][164] It is frequently used in induction and anaesthetic maintenance in horses. It is an important part of the «rodent cocktail», a mixture of drugs used for anaesthetising rodents.[165] Veterinarians often use ketamine with sedative drugs to produce balanced anaesthesia and analgesia, and as a constant-rate infusion to help prevent pain wind-up. Ketamine is also used to manage pain among large animals. It is the primary intravenous anaesthetic agent used in equine surgery, often in conjunction with detomidine and thiopental, or sometimes guaifenesin.[166]
Ketamine appears not to produce sedation or anaesthesia in snails. Instead, it appears to have an excitatory effect.[167]
References[edit]
- ^ Morton IK, Hall JM (6 December 2012). Concise Dictionary of Pharmacological Agents: Properties and Synonyms. Springer Science & Business Media. pp. 159–. ISBN 978-94-011-4439-1. Archived from the original on 11 April 2017.
- ^ «Ketamine (Ketalar) Use During Pregnancy». Drugs.com. 22 November 2019. Retrieved 18 May 2020.
- ^ Malenka RC, Nestler EJ, Hyman SE (2009). «Chapter 15: Reinforcement and Addictive Disorders». In Sydor A, Brown RY (eds.). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York: McGraw-Hill Medical. pp. 374–375. ISBN 978-0-07-148127-4.
Phencyclidine (PCP or angel dust) and ketamine (also known as special K) are structurally related drugs… their reinforcing properties and risks related to compulsive abuse
- ^ Bell RF, Eccleston C, Kalso EA (June 2017). «Ketamine as an adjuvant to opioids for cancer pain» (PDF). The Cochrane Database of Systematic Reviews. 6 (9): CD003351. doi:10.1002/14651858.CD003351.pub3. PMC 6481583. PMID 28657160.
- ^ Moyse DW, Kaye AD, Diaz JH, Qadri MY, Lindsay D, Pyati S (March 2017). «Perioperative Ketamine Administration for Thoracotomy Pain». Pain Physician. 20 (3): 173–184. PMID 28339431.
- ^ a b c d e f g h i j k l m n o Mathew SJ, Zarate Jr CA (25 November 2016). Ketamine for Treatment-Resistant Depression: The First Decade of Progress. Springer. pp. 8–10, 14–22. ISBN 978-3-319-42925-0. Archived from the original on 8 September 2017.
- ^ Brayfield A, ed. (9 January 2017). «Ketamine Hydrochloride: Martindale: The Complete Drug Reference». MedicinesComplete. London, UK: Pharmaceutical Press. Retrieved 24 August 2017.
- ^ a b Mao J (19 April 2016). Opioid-Induced Hyperalgesia. CRC Press. pp. 127–. ISBN 978-1-4200-8900-4. Archived from the original on 8 September 2017.
- ^ a b Kintz P (22 March 2014). Toxicological Aspects of Drug-Facilitated Crimes. Elsevier Science. pp. 87–. ISBN 978-0-12-416969-2. Archived from the original on 8 September 2017.
- ^ a b c d e f g h i Marland S, Ellerton J, Andolfatto G, Strapazzon G, Thomassen O, Brandner B, Weatherall A, Paal P (June 2013). «Ketamine: use in anesthesia». CNS Neurosci Ther. 19 (6): 381–9. doi:10.1111/cns.12072. PMC 6493613. PMID 23521979.
- ^ a b c d e f g h Hashimoto K (October 2019). «Rapid-acting antidepressant ketamine, its metabolites and other candidates: A historical overview and future perspective». Psychiatry and Clinical Neurosciences. 73 (10): 613–627. doi:10.1111/pcn.12902. PMC 6851782. PMID 31215725.
- ^ a b Dayton PG, Stiller RL, Cook DR, Perel JM (1983). «The binding of ketamine to plasma proteins: emphasis on human plasma». Eur J Clin Pharmacol. 24 (6): 825–31. doi:10.1007/BF00607095. PMID 6884418. S2CID 807011.
- ^ a b c d e f g h Sinner B, Graf BM (2008). «Ketamine». In Schüttler J, Schwilden H (eds.). Modern Anesthetics. Handbook of Experimental Pharmacology. Vol. 182. pp. 313–33. doi:10.1007/978-3-540-74806-9_15. ISBN 978-3-540-72813-9. PMID 18175098.
- ^ a b c d e f g h Quibell R, Prommer EE, Mihalyo M, Twycross R, Wilcock A (March 2011). «Ketamine*». Journal of Pain and Symptom Management (Therapeutic Review). 41 (3): 640–9. doi:10.1016/j.jpainsymman.2011.01.001. PMID 21419322.
- ^ a b c Chang T, Glazko AJ (1974). «Biotransformation and disposition of ketamine». Int Anesthesiol Clin. 12 (2): 157–77. doi:10.1097/00004311-197412020-00018. PMID 4603048. S2CID 30723730.
- ^ Hijazi Y, Boulieu R (July 2002). «Contribution of CYP3A4, CYP2B6, and CYP2C9 isoforms to N-demethylation of ketamine in human liver microsomes». Drug Metabolism and Disposition. 30 (7): 853–8. doi:10.1124/dmd.30.7.853. PMID 12065445. S2CID 15787750.
- ^ a b c d Rao LK, Flaker AM, Friedel CC, Kharasch ED (December 2016). «Role of Cytochrome P4502B6 Polymorphisms in Ketamine Metabolism and Clearance». Anesthesiology. 125 (6): 1103–1112. doi:10.1097/ALN.0000000000001392. PMID 27763887. S2CID 41380105.
- ^ Sass W, Fusari S (1977). «Ketamine». Analytical Profiles of Drug Substances, volume 6. Analytical Profiles of Drug Substances. Vol. 6. Academic Press. pp. 297–322. doi:10.1016/S0099-5428(08)60347-0. ISBN 9780122608063.
- ^ Peltoniemi MA, Hagelberg NM, Olkkola KT, Saari TI (September 2016). «Ketamine: A Review of Clinical Pharmacokinetics and Pharmacodynamics in Anesthesia and Pain Therapy». Clinical Pharmacokinetics. 55 (9): 1059–77. doi:10.1007/s40262-016-0383-6. PMID 27028535. S2CID 5078489.
- ^ a b c d e f Cohen SP, Bhatia A, Buvanendran A, Schwenk ES, Wasan AD, Hurley RW, et al. (July 2018). «Consensus Guidelines on the Use of Intravenous Ketamine Infusions for Chronic Pain From the American Society of Regional Anesthesia and Pain Medicine, the American Academy of Pain Medicine, and the American Society of Anesthesiologists». Reg Anesth Pain Med. 43 (5): 521–546. doi:10.1097/AAP.0000000000000808. PMC 6023575. PMID 29870458.
- ^ a b c Green SM, Roback MG, Kennedy RM, Krauss B (May 2011). «Clinical practice guideline for emergency department ketamine dissociative sedation: 2011 update». Annals of Emergency Medicine. 57 (5): 449–61. doi:10.1016/j.annemergmed.2010.11.030. PMID 21256625.
- ^ a b Zhang K, Hashimoto K (January 2019). «An update on ketamine and its two enantiomers as rapid-acting antidepressants». Expert Review of Neurotherapeutics. 19 (1): 83–92. doi:10.1080/14737175.2019.1554434. PMID 30513009. S2CID 54628949.
- ^ a b c d Marcantoni WS, Akoumba BS, Wassef M, Mayrand J, Lai H, Richard-Devantoy S, Beauchamp S (December 2020). «A systematic review and meta-analysis of the efficacy of intravenous ketamine infusion for treatment resistant depression: January 2009 — January 2019». J Affect Disord. 277: 831–841. doi:10.1016/j.jad.2020.09.007. PMID 33065824. S2CID 223557698.
- ^ a b c d Swainson J, McGirr A, Blier P, et al. (November 2020). «The Canadian Network for Mood and Anxiety Treatments (CANMAT) Task Force Recommendations for the Use of Racemic Ketamine in Adults with Major Depressive Disorder: Recommandations Du Groupe De Travail Du Réseau Canadien Pour Les Traitements De L’humeur Et De L’anxiété (Canmat) Concernant L’utilisation De La Kétamine Racémique Chez Les Adultes Souffrant De Trouble Dépressif Majeur». Can J Psychiatry. 66 (2): 113–125. doi:10.1177/0706743720970860. PMC 7918868. PMID 33174760.
- ^ a b Bobo WV, Riva-Posse P, Goes FS, Parikh SV (April 2020). «Next-Step Treatment Considerations for Patients With Treatment-Resistant Depression That Responds to Low-Dose Intravenous Ketamine». Focus (Am Psychiatr Publ). 18 (2): 181–192. doi:10.1176/appi.focus.20190048. PMC 7587874. PMID 33162856.
- ^ Orhurhu VJ, Vashisht R, Claus LE, Cohen SP (April 2022). «Ketamine toxicity». StatPearls. Treasure Island (FL): StatPearls Publishing. PMID 31082131. Retrieved 18 August 2022.
- ^ a b c d Domino EF (September 2010). «Taming the ketamine tiger. 1965». Anesthesiology. 113 (3): 678–84. doi:10.1097/ALN.0b013e3181ed09a2. PMID 20693870.
- ^ a b c Morgan CJ, Curran HV (January 2012). «Ketamine use: a review». Addiction. 107 (1): 27–38. doi:10.1111/j.1360-0443.2011.03576.x. PMID 21777321. S2CID 11064759.
- ^ World Health Organization (2021). World Health Organization model list of essential medicines: 22nd list (2021). Geneva: World Health Organization. hdl:10665/345533. WHO/MHP/HPS/EML/2021.02.
- ^ «Ketamine Injection». Drugs.com. Archived from the original on 10 December 2014. Retrieved 1 December 2014.
- ^ a b Rosenbaum SB, Gupta V, Palacios JL (2020). «Ketamine». StatPearls. StatPearls Publishing. PMID 29262083. Retrieved 5 March 2020.
- ^ Heshmati F, Zeinali MB, Noroozinia H, Abbacivash R, Mahoori A (December 2003). «Use of ketamine in severe status asthmaticus in intensive care unit». Iranian Journal of Allergy, Asthma, and Immunology. 2 (4): 175–80. PMID 17301376. Archived from the original on 6 October 2014.
- ^ Adams HA (December 1997). «[S-(+)-ketamine. Circulatory interactions during total intravenous anesthesia and analgesia-sedation]» [S-(+)-ketamine. Circulatory interactions during total intravenous anesthesia and analgesia-sedation]. Der Anaesthesist (in German). 46 (12): 1081–7. doi:10.1007/s001010050510. PMID 9451493.
- ^ Wong JJ, Lee JH, Turner DA, Rehder KJ (August 2014). «A review of the use of adjunctive therapies in severe acute asthma exacerbation in critically ill children». Expert Review of Respiratory Medicine. 8 (4): 423–41. doi:10.1586/17476348.2014.915752. PMID 24993063. S2CID 31435021.
- ^ a b c Anand A, Charney DS, Oren DA, Berman RM, Hu XS, Cappiello A, Krystal JH (March 2000). «Attenuation of the neuropsychiatric effects of ketamine with lamotrigine: support for hyperglutamatergic effects of N-methyl-D-aspartate receptor antagonists». Arch Gen Psychiatry. 57 (3): 270–6. doi:10.1001/archpsyc.57.3.270. PMID 10711913.
- ^ a b c Krupitsky EM, Burakov AM, Romanova TN, Grinenko NI, Grinenko AY, Fletcher J, Petrakis IL, Krystal JH (December 2001). «Attenuation of ketamine effects by nimodipine pretreatment in recovering ethanol dependent men: psychopharmacologic implications of the interaction of NMDA and L-type calcium channel antagonists». Neuropsychopharmacology. 25 (6): 936–47. doi:10.1016/S0893-133X(01)00346-3. PMID 11750186.
- ^ a b c d Barrett W, Buxhoeveden M, Dhillon S (October 2020). «Ketamine: a versatile tool for anesthesia and analgesia». Current Opinion in Anesthesiology. 33 (5): 633–638. doi:10.1097/ACO.0000000000000916. PMID 32826629. S2CID 221236545.
- ^ Cohen L, Athaide V, Wickham ME, Doyle-Waters MM, Rose NG, Hohl CM (January 2015). «The effect of ketamine on intracranial and cerebral perfusion pressure and health outcomes: a systematic review». Annals of Emergency Medicine. 65 (1): 43–51.e2. doi:10.1016/j.annemergmed.2014.06.018. PMID 25064742.
- ^ a b c Kurdi MS, Theerth KA, Deva RS (September 2014). «Ketamine: Current applications in anesthesia, pain, and critical care». Anesthesia: Essays and Researches. 8 (3): 283–90. doi:10.4103/0259-1162.143110. PMC 4258981. PMID 25886322.
- ^ Mion G (September 2017). «History of anaesthesia: The ketamine story — past, present and future». Eur J Anaesthesiol. 34 (9): 571–575. doi:10.1097/EJA.0000000000000638. PMID 28731926. S2CID 27536846.
- ^ Nickson C (7 August 2013). «Intubation, Hypotension and Shock». Life in the Fastlane (blog). Critical Care Compendium. Archived from the original on 9 February 2014. Retrieved 10 April 2014.[unreliable medical source?]
- ^ Manley G, Knudson MM, Morabito D, Damron S, Erickson V, Pitts L (October 2001). «Hypotension, hypoxia, and head injury: frequency, duration, and consequences». Archives of Surgery. 136 (10): 1118–23. doi:10.1001/archsurg.136.10.1118. PMID 11585502.
- ^ Hemmingsen C, Nielsen JE (November 1991). «Intravenous ketamine for prevention of severe hypotension during spinal anaesthesia». Acta Anaesthesiologica Scandinavica. 35 (8): 755–7. doi:10.1111/j.1399-6576.1991.tb03385.x. PMID 1763596. S2CID 1324453.
- ^ Wong DH, Jenkins LC (May 1975). «The cardiovascular effects of ketamine in hypotensive states». Canadian Anaesthetists’ Society Journal. 22 (3): 339–48. doi:10.1007/BF03004843. PMID 1139377.
- ^ Goyal S, Agrawal A (May 2013). «Ketamine in status asthmaticus: A review». Indian Journal of Critical Care Medicine. 17 (3): 154–61. doi:10.4103/0972-5229.117048. PMC 3777369. PMID 24082612.
- ^ a b c Schwenk ES, Viscusi ER, Buvanendran A, Hurley RW, Wasan AD, Narouze S, Bhatia A, Davis FN, Hooten WM, Cohen SP (July 2018). «Consensus Guidelines on the Use of Intravenous Ketamine Infusions for Acute Pain Management From the American Society of Regional Anesthesia and Pain Medicine, the American Academy of Pain Medicine, and the American Society of Anesthesiologists». Reg Anesth Pain Med. 43 (5): 456–466. doi:10.1097/AAP.0000000000000806. PMC 6023582. PMID 29870457.
- ^ Sin B, Ternas T, Motov SM (March 2015). «The use of subdissociative-dose ketamine for acute pain in the emergency department». Academic Emergency Medicine. 22 (3): 251–7. doi:10.1111/acem.12604. PMID 25716117. S2CID 24658476.
- ^ Svenson J, Biedermann M (2011). «Ketamine: a unique drug with several potential uses in the prehospital setting». Journal of Paramedic Practice. 3 (10): 552–556. doi:10.12968/jpar.2011.3.10.552.
- ^ Karlow N, Schlaepfer CH, Stoll CR, Doering M, Carpenter CR, Colditz GA, et al. (October 2018). «A Systematic Review and Meta-analysis of Ketamine as an Alternative to Opioids for Acute Pain in the Emergency Department». Academic Emergency Medicine. 25 (10): 1086–1097. doi:10.1111/acem.13502. PMID 30019434.
- ^ Radvansky BM, Shah K, Parikh A, Sifonios AN, Le V, Eloy JD (2015). «Role of ketamine in acute postoperative pain management: a narrative review». BioMed Research International. 2015: 749837. doi:10.1155/2015/749837. PMC 4606413. PMID 26495312.
- ^ Lee M, Silverman SM, Hansen H, Patel VB, Manchikanti L (2011). «A comprehensive review of opioid-induced hyperalgesia». Pain Physician. 14 (2): 145–61. doi:10.36076/ppj.2011/14/145. PMID 21412369.
- ^ Zhou Y, Mannan A, Han Y, Liu H, Guan HL, Gao X, et al. (December 2019). «Efficacy and safety of prophylactic use of ketamine for prevention of postanesthetic shivering: a systematic review and meta analysis». BMC Anesthesiology. 19 (1): 245. doi:10.1186/s12871-019-0910-8. PMC 6937868. PMID 31888509.
- ^ Elia N, Tramèr MR (January 2005). «Ketamine and postoperative pain—a quantitative systematic review of randomised trials». Pain. 113 (1–2): 61–70. doi:10.1016/j.pain.2004.09.036. PMID 15621365. S2CID 25925720.
- ^ «How Does Ketamine Work in The Brain? Does It Help? – Everything You Need to Know». Psychreg. 3 January 2022. Retrieved 19 August 2022.
- ^ a b c Sanacora G, Frye MA, McDonald W, Mathew SJ, Turner MS, Schatzberg AF, et al. (April 2017). «A Consensus Statement on the Use of Ketamine in the Treatment of Mood Disorders». JAMA Psychiatry. 74 (4): 399–405. doi:10.1001/jamapsychiatry.2017.0080. PMID 28249076. S2CID 28320520.
- ^ a b c d Molero P, Ramos-Quiroga JA, Martin-Santos R, Calvo-Sánchez E, Gutiérrez-Rojas L, Meana JJ (May 2018). «Antidepressant Efficacy and Tolerability of Ketamine and Esketamine: A Critical Review». CNS Drugs. 32 (5): 411–420. doi:10.1007/s40263-018-0519-3. PMID 29736744. S2CID 13679905.
- ^ Sanacora G, Katz R (July 2018). «Ketamine: A Review for Clinicians». Focus. American Psychiatric Association Publishing. 16 (3): 243–250. doi:10.1176/appi.focus.20180012. PMC 6493090. PMID 31975918.
- ^ a b Singh I, Morgan C, Curran V, Nutt D, Schlag A, McShane R (May 2017). «Ketamine treatment for depression: opportunities for clinical innovation and ethical foresight». The Lancet. Psychiatry. 4 (5): 419–426. doi:10.1016/S2215-0366(17)30102-5. hdl:10871/30208. PMID 28395988. S2CID 28186580.
- ^ Witt K, Potts J, Hubers A, Grunebaum MF, Murrough JW, Loo C, Cipriani A, Hawton K (January 2020). «Ketamine for suicidal ideation in adults with psychiatric disorders: A systematic review and meta-analysis of treatment trials». Aust N Z J Psychiatry. 54 (1): 29–45. doi:10.1177/0004867419883341. PMID 31729893. S2CID 208035394.
- ^ «Spravato (esketamine)». European Medicines Agency. 8 July 2022. Retrieved 20 July 2022.
- ^ «FDA approves new nasal spray medication for treatment-resistant depression; available only at a certified doctor’s office or clinic». US Food and Drug Administration. 5 March 2019. Retrieved 29 July 2022.
- ^ a b Dean RL, Hurducas C, Hawton K, et al. (September 2021). «Ketamine and other glutamate receptor modulators for depression in adults with unipolar major depressive disorder». The Cochrane Database of Systematic Reviews. 9 (11): CD011612. doi:10.1002/14651858.CD011612.pub3. PMC 8434915. PMID 34510411.
- ^ a b Dean RL, Marquardt T, Hurducas C, Spyridi S, Barnes A, Smith R, et al. (October 2021). «Ketamine and other glutamate receptor modulators for depression in adults with bipolar disorder». The Cochrane Database of Systematic Reviews. 2021 (10): CD011611. doi:10.1002/14651858.CD011611.pub3. PMC 8499740. PMID 34623633.
- ^ «FDA alerts health care professionals of potential risks associated with compounded ketamine nasal spray». US Food and Drug Administration. 16 February 2022. Retrieved 29 July 2022.
- ^ Jansen K (2001). Ketamine: Dreams and Realities. Multidisciplinary Association for Psychedelic Studies. p. 122. ISBN 978-0-9660019-3-8.
- ^ Peinkhofer C, Dreier JP, Kondziella D (July 2019). «Semiology and Mechanisms of Near-Death Experiences». Current Neurology and Neuroscience Reports. 19 (9): 62. doi:10.1007/s11910-019-0983-2. PMID 31352520. S2CID 198965307.
- ^ Martial C, Cassol H, Charland-Verville V, Pallavicini C, Sanz C, Zamberlan F, et al. (March 2019). «Neurochemical models of near-death experiences: A large-scale study based on the semantic similarity of written reports». Consciousness and Cognition. 69: 52–69. doi:10.1016/j.concog.2019.01.011. hdl:2268/231971. PMID 30711788. S2CID 73432875.
- ^ Gomes D, Pimentel J, Bentes C, Aguiar de Sousa D, Antunes AP, Alvarez A, Silva ZC (October 2018). «Consensus Protocol for the Treatment of Super-Refractory Status Epilepticus». Acta Médica Portuguesa. 31 (10): 598–605. doi:10.20344/amp.9679. PMID 30387431.
- ^ Rosati A, De Masi S, Guerrini R (November 2018). «Ketamine for Refractory Status Epilepticus: A Systematic Review». CNS Drugs. 32 (11): 997–1009. doi:10.1007/s40263-018-0569-6. PMID 30232735. S2CID 52302073.
- ^ a b c d e Strayer RJ, Nelson LS (November 2008). «Adverse events associated with ketamine for procedural sedation in adults». The American Journal of Emergency Medicine. 26 (9): 985–1028. doi:10.1016/j.ajem.2007.12.005. PMID 19091264. Archived from the original on 8 September 2017.
- ^ Acevedo-Diaz EE, Cavanaugh GW, Greenstein D, Kraus C, Kadriu B, Zarate CA, Park LT (February 2020). «Comprehensive assessment of side effects associated with a single dose of ketamine in treatment-resistant depression». J Affect Disord. 263: 568–575. doi:10.1016/j.jad.2019.11.028. PMC 8457026. PMID 31791675.
- ^ Smith HS (2010). «Ketamine-induced urologic insult (KIUI)». Pain Physician. 13 (6): E343–6. doi:10.36076/ppj.2010/13/E343. PMID 21102971.
- ^ a b c d Castellani D, Pirola GM, Gubbiotti M, Rubilotta E, Gudaru K, Gregori A, Dellabella M (April 2020). «What urologists need to know about ketamine-induced uropathy: A systematic review». Neurourol Urodyn. 39 (4): 1049–1062. doi:10.1002/nau.24341. PMID 32212278. S2CID 214643776.
- ^ Middela S, Pearce I (January 2011). «Ketamine-induced vesicopathy: a literature review». International Journal of Clinical Practice. 65 (1): 27–30. doi:10.1111/j.1742-1241.2010.02502.x. PMID 21155941. S2CID 25034266.
- ^ Morgan CJ, Muetzelfeldt L, Curran HV (January 2010). «Consequences of chronic ketamine self-administration upon neurocognitive function and psychological wellbeing: a 1-year longitudinal study». Addiction. 105 (1): 121–33. doi:10.1111/j.1360-0443.2009.02761.x. PMID 19919593.
- ^ Hui TW, Short TG, Hong W, Suen T, Gin T, Plummer J (March 1995). «Additive interactions between propofol and ketamine when used for anesthesia induction in female patients». Anesthesiology. 82 (3): 641–8. doi:10.1097/00000542-199503000-00005. PMID 7879932. S2CID 24005549.
- ^ Hong W, Short TG, Hui TW (December 1993). «Hypnotic and anesthetic interactions between ketamine and midazolam in female patients». Anesthesiology. 79 (6): 1227–32. doi:10.1097/00000542-199312000-00013. PMID 8267198. S2CID 12246068.
- ^ Krystal JH, Madonick S, Perry E, Gueorguieva R, Brush L, Wray Y, Belger A, D’Souza DC (August 2006). «Potentiation of low dose ketamine effects by naltrexone: potential implications for the pharmacotherapy of alcoholism». Neuropsychopharmacology. 31 (8): 1793–800. doi:10.1038/sj.npp.1300994. PMID 16395307.
- ^ Handa F, Tanaka M, Nishikawa T, Toyooka H (February 2000). «Effects of oral clonidine premedication on side effects of intravenous ketamine anesthesia: a randomized, double-blind, placebo-controlled study». J Clin Anesth. 12 (1): 19–24. doi:10.1016/s0952-8180(99)00131-2. PMID 10773503.
- ^ a b Andrade C (July 2017). «Ketamine for Depression, 5: Potential Pharmacokinetic and Pharmacodynamic Drug Interactions». The Journal of Clinical Psychiatry. 78 (7): e858–e861. doi:10.4088/JCP.17f11802. PMID 28858450.
- ^ a b c d e Zanos P, Moaddel R, Morris PJ, Riggs LM, Highland JN, Georgiou P, Pereira EF, Albuquerque EX, Thomas CJ, Zarate CA, Gould TD (July 2018). «Ketamine and Ketamine Metabolite Pharmacology: Insights into Therapeutic Mechanisms». Pharmacol Rev. 70 (3): 621–660. doi:10.1124/pr.117.015198. PMC 6020109. PMID 29945898.
- ^ a b Peltoniemi MA, Hagelberg NM, Olkkola KT, Saari TI (September 2016). «Ketamine: A Review of Clinical Pharmacokinetics and Pharmacodynamics in Anesthesia and Pain Therapy». Clin Pharmacokinet. 55 (9): 1059–77. doi:10.1007/s40262-016-0383-6. PMID 27028535. S2CID 5078489.
- ^ Zanos P, Gould TD (April 2018). «Mechanisms of ketamine action as an antidepressant». Molecular Psychiatry. 23 (4): 801–811. doi:10.1038/mp.2017.255. PMC 5999402. PMID 29532791.
- ^ a b c d e Zanos P, Gould TD (April 2018). «Mechanisms of ketamine action as an antidepressant». Molecular Psychiatry. 23 (4): 801–811. doi:10.1038/mp.2017.255. PMC 5999402. PMID 29532791.
- ^ a b Zanos P, Thompson SM, Duman RS, Zarate CA, Gould TD (March 2018). «Convergent Mechanisms Underlying Rapid Antidepressant Action». CNS Drugs. 32 (3): 197–227. doi:10.1007/s40263-018-0492-x. PMC 6005380. PMID 29516301.
- ^ Björkholm C, Monteggia LM (March 2016). «BDNF — a key transducer of antidepressant effects». Neuropharmacology. 102: 72–79. doi:10.1016/j.neuropharm.2015.10.034. PMC 4763983. PMID 26519901.
- ^ Castrén E, Kojima M (January 2017). «Brain-derived neurotrophic factor in mood disorders and antidepressant treatments». Neurobiology of Disease. 97 (Pt B): 119–126. doi:10.1016/j.nbd.2016.07.010. hdl:10138/311483. PMID 27425886. S2CID 644350.
- ^ Kim D, Cheong E, Shin HS (June 2018). «Overcoming Depression by Inhibition of Neural Burst Firing». Neuron. 98 (5): 878–879. doi:10.1016/j.neuron.2018.05.032. PMID 29879390.
- ^ Yang Y, Cui Y, Sang K, Dong Y, Ni Z, Ma S, Hu H (February 2018). «Ketamine blocks bursting in the lateral habenula to rapidly relieve depression». Nature. 554 (7692): 317–322. Bibcode:2018Natur.554..317Y. doi:10.1038/nature25509. PMID 29446381. S2CID 3334820.
- ^ a b Garay R, Zarate CA, Cavero I, Kim YK, Charpeaud T, Skolnick P (October 2018). «The development of glutamate-based antidepressants is taking longer than expected». Drug Discovery Today. 23 (10): 1689–1692. doi:10.1016/j.drudis.2018.02.006. PMC 6211562. PMID 29501913.
- ^ a b Moaddel R, Abdrakhmanova G, Kozak J, Jozwiak K, Toll L, Jimenez L, Rosenberg A, Tran T, Xiao Y, Zarate CA, Wainer IW (January 2013). «Sub-anesthetic concentrations of (R,S)-ketamine metabolites inhibit acetylcholine-evoked currents in α7 nicotinic acetylcholine receptors». Eur J Pharmacol. 698 (1–3): 228–34. doi:10.1016/j.ejphar.2012.11.023. PMC 3534778. PMID 23183107.
- ^ «Arketamine – Jiangsu Hengrui Medicine – AdisInsight».
- ^ Morris PJ, Moaddel R, Zanos P, Moore CE, Gould TD, Zarate CA, Thomas CJ (September 2017). «Synthesis and N-Methyl-d-aspartate (NMDA) Receptor Activity of Ketamine Metabolites». Organic Letters. 19 (17): 4572–4575. doi:10.1021/acs.orglett.7b02177. PMC 5641405. PMID 28829612.
- ^ a b c d Roth BL, Gibbons S, Arunotayanun W, Huang XP, Setola V, Treble R, Iversen L (2013). «The ketamine analogue methoxetamine and 3- and 4-methoxy analogues of phencyclidine are high affinity and selective ligands for the glutamate NMDA receptor». PLOS ONE. 8 (3): e59334. Bibcode:2013PLoSO…859334R. doi:10.1371/journal.pone.0059334. PMC 3602154. PMID 23527166.
- ^ a b Hirota K, Okawa H, Appadu BL, Grandy DK, Devi LA, Lambert DG (January 1999). «Stereoselective interaction of ketamine with recombinant mu, kappa, and delta opioid receptors expressed in Chinese hamster ovary cells». Anesthesiology. 90 (1): 174–82. doi:10.1097/00000542-199901000-00023. PMID 9915326.
- ^ Hirota K, Sikand KS, Lambert DG (1999). «Interaction of ketamine with mu2 opioid receptors in SH-SY5Y human neuroblastoma cells». Journal of Anesthesia. 13 (2): 107–9. doi:10.1007/s005400050035. PMID 14530949. S2CID 9322174.
- ^ Nemeth CL, Paine TA, Rittiner JE, Béguin C, Carroll FI, Roth BL, Cohen BM, Carlezon WA (June 2010). «Role of kappa-opioid receptors in the effects of salvinorin A and ketamine on attention in rats». Psychopharmacology (Berl). 210 (2): 263–74. doi:10.1007/s00213-010-1834-7. PMC 2869248. PMID 20358363.
- ^ Robson MJ, Elliott M, Seminerio MJ, Matsumoto RR (April 2012). «Evaluation of sigma (σ) receptors in the antidepressant-like effects of ketamine in vitro and in vivo». Eur Neuropsychopharmacol. 22 (4): 308–17. doi:10.1016/j.euroneuro.2011.08.002. PMID 21911285. S2CID 24494428.
- ^ a b Kapur S, Seeman P (2002). «NMDA receptor antagonists ketamine and PCP have direct effects on the dopamine D(2) and serotonin 5-HT(2)receptors-implications for models of schizophrenia». Molecular Psychiatry. 7 (8): 837–44. doi:10.1038/sj.mp.4001093. PMID 12232776.
- ^ a b c d e Can A, Zanos P, Moaddel R, Kang HJ, Dossou KS, Wainer IW, et al. (October 2016). «Effects of Ketamine and Ketamine Metabolites on Evoked Striatal Dopamine Release, Dopamine Receptors, and Monoamine Transporters». The Journal of Pharmacology and Experimental Therapeutics. 359 (1): 159–70. doi:10.1124/jpet.116.235838. PMC 5034706. PMID 27469513.
- ^ a b Jordan S, Chen R, Fernalld R, Johnson J, Regardie K, Kambayashi J, et al. (July 2006). «In vitro biochemical evidence that the psychotomimetics phencyclidine, ketamine and dizocilpine (MK-801) are inactive at cloned human and rat dopamine D2 receptors». European Journal of Pharmacology. 540 (1–3): 53–6. doi:10.1016/j.ejphar.2006.04.026. PMID 16730695.
- ^ Hirota K, Hashimoto Y, Lambert DG (December 2002). «Interaction of intravenous anesthetics with recombinant human M1-M3 muscarinic receptors expressed in chinese hamster ovary cells». Anesth Analg. 95 (6): 1607–10, table of contents. doi:10.1097/00000539-200212000-00025. PMID 12456425. S2CID 25643394.
- ^ a b c d e f Yamakura T, Chavez-Noriega LE, Harris RA (April 2000). «Subunit-dependent inhibition of human neuronal nicotinic acetylcholine receptors and other ligand-gated ion channels by dissociative anesthetics ketamine and dizocilpine». Anesthesiology. 92 (4): 1144–53. doi:10.1097/00000542-200004000-00033. PMID 10754635. S2CID 23651917.
- ^ Ho MF, Correia C, Ingle JN, Kaddurah-Daouk R, Wang L, Kaufmann SH, Weinshilboum RM (June 2018). «Ketamine and ketamine metabolites as novel estrogen receptor ligands: Induction of cytochrome P450 and AMPA glutamate receptor gene expression». Biochemical Pharmacology. 152: 279–292. doi:10.1016/j.bcp.2018.03.032. PMC 5960634. PMID 29621538.
- ^ a b Nishimura M, Sato K, Okada T, Yoshiya I, Schloss P, Shimada S, Tohyama M (March 1998). «Ketamine inhibits monoamine transporters expressed in human embryonic kidney 293 cells». Anesthesiology. 88 (3): 768–74. doi:10.1097/00000542-199803000-00029. PMID 9523822. S2CID 30159489.
- ^ Zhao Y, Sun L (November 2008). «Antidepressants modulate the in vitro inhibitory effects of propofol and ketamine on norepinephrine and serotonin transporter function». J Clin Neurosci. 15 (11): 1264–9. doi:10.1016/j.jocn.2007.11.007. PMC 2605271. PMID 18815045.
- ^ Chen X, Shu S, Bayliss DA (January 2009). «HCN1 channel subunits are a molecular substrate for hypnotic actions of ketamine». The Journal of Neuroscience. 29 (3): 600–9. doi:10.1523/JNEUROSCI.3481-08.2009. PMC 2744993. PMID 19158287.
- ^ da Costa FL, Pinto MC, Santos DC, Carobin NV, de Jesus IC, Ferreira LA, et al. (December 2020). «Ketamine potentiates TRPV1 receptor signaling in the peripheral nociceptive pathways». Biochemical Pharmacology. 182: 114210. doi:10.1016/j.bcp.2020.114210. PMID 32882205. S2CID 221497233.
- ^ a b c d Tyler MW, Yourish HB, Ionescu DF, Haggarty SJ (June 2017). «Classics in Chemical Neuroscience: Ketamine». ACS Chemical Neuroscience. 8 (6): 1122–1134. doi:10.1021/acschemneuro.7b00074. PMID 28418641.
- ^ Hirota K, Lambert DG (October 1996). «Ketamine: its mechanism(s) of action and unusual clinical uses». British Journal of Anaesthesia. 77 (4): 441–4. doi:10.1093/bja/77.4.441. PMID 8942324.
- ^ Orser BA, Pennefather PS, MacDonald JF (April 1997). «Multiple mechanisms of ketamine blockade of N-methyl-D-aspartate receptors». Anesthesiology. 86 (4): 903–17. doi:10.1097/00000542-199704000-00021. PMID 9105235. S2CID 2164198.
- ^ Lodge D, Mercier MS (September 2015). «Ketamine and phencyclidine: the good, the bad, and the unexpected». British Journal of Pharmacology. 172 (17): 4254–76. doi:10.1111/bph.13222. PMC 4556466. PMID 26075331.
- ^ a b Kraus C, Rabl U, Vanicek T, Carlberg L, Popovic A, Spies M, et al. (March 2017). «Administration of ketamine for unipolar and bipolar depression». International Journal of Psychiatry in Clinical Practice. 21 (1): 2–12. doi:10.1080/13651501.2016.1254802. PMID 28097909. S2CID 35626369.
- ^ a b Bartova L, Vogl SE, Stamenkovic M, Praschak-Rieder N, Naderi-Heiden A, Kasper S, Willeit M (November 2015). «Combination of intravenous S-ketamine and oral tranylcypromine in treatment-resistant depression: A report of two cases». European Neuropsychopharmacology. 25 (11): 2183–4. doi:10.1016/j.euroneuro.2015.07.021. PMID 26302763. S2CID 39039021.
- ^ Seeman P, Guan HC (November 2008). «Phencyclidine and glutamate agonist LY379268 stimulate dopamine D2High receptors: D2 basis for schizophrenia». Synapse. 62 (11): 819–28. doi:10.1002/syn.20561. PMID 18720422. S2CID 206519749.
- ^ Seeman P, Guan HC, Hirbec H (August 2009). «Dopamine D2High receptors stimulated by phencyclidines, lysergic acid diethylamide, salvinorin A, and modafinil». Synapse. 63 (8): 698–704. doi:10.1002/syn.20647. PMID 19391150. S2CID 17758902.
- ^ The Role of Brain Dopamine. Springer Science & Business Media. 6 December 2012. pp. 23–. ISBN 978-3-642-73897-5.
- ^ Krystal JH, Karper LP, Seibyl JP, Freeman GK, Delaney R, Bremner JD, et al. (March 1994). «Subanesthetic effects of the noncompetitive NMDA antagonist, ketamine, in humans. Psychotomimetic, perceptual, cognitive, and neuroendocrine responses». Archives of General Psychiatry. 51 (3): 199–214. doi:10.1001/archpsyc.1994.03950030035004. PMID 8122957.
- ^ Hergovich N, Singer E, Agneter E, Eichler HG, Graselli U, Simhandl C, Jilma B (May 2001). «Comparison of the effects of ketamine and memantine on prolactin and cortisol release in men. a randomized, double-blind, placebo-controlled trial». Neuropsychopharmacology. 24 (5): 590–3. doi:10.1016/S0893-133X(00)00194-9. PMID 11282259.
- ^ a b Rabiner EA (May 2007). «Imaging of striatal dopamine release elicited with NMDA antagonists: is there anything there to be seen?». Journal of Psychopharmacology. 21 (3): 253–8. doi:10.1177/0269881107077767. PMID 17591653. S2CID 23776189.
- ^ a b Idvall J, Ahlgren I, Aronsen KR, Stenberg P (December 1979). «Ketamine infusions: pharmacokinetics and clinical effects». Br J Anaesth. 51 (12): 1167–73. doi:10.1093/bja/51.12.1167. PMID 526385.
- ^ Domino EF, Zsigmond EK, Domino LE, Domino KE, Kothary SP, Domino SE (February 1982). «Plasma levels of ketamine and two of its metabolites in surgical patients using a gas chromatographic mass fragmentographic assay». Anesth Analg. 61 (2): 87–92. doi:10.1213/00000539-198202000-00004. PMID 7198883. S2CID 27596215.
- ^ White PF, Schüttler J, Shafer A, Stanski DR, Horai Y, Trevor AJ (February 1985). «Comparative pharmacology of the ketamine isomers. Studies in volunteers». Br J Anaesth. 57 (2): 197–203. doi:10.1093/bja/57.2.197. PMID 3970799.
- ^ Stenberg P, Idvall J (July 1981). «Does ketamine metabolite II exist in vivo?». Br J Anaesth. 53 (7): 778. doi:10.1093/bja/53.7.778. PMID 7248132.
- ^ Li Y, Jackson KA, Slon B, Hardy JR, Franco M, William L, Poon P, Coller JK, Hutchinson MR, Currow DC, Somogyi AA (August 2015). «CYP2B6*6 allele and age substantially reduce steady-state ketamine clearance in chronic pain patients: impact on adverse effects». Br J Clin Pharmacol. 80 (2): 276–84. doi:10.1111/bcp.12614. PMC 4541975. PMID 25702819.
- ^ Synthesis of ketamine references:
- Stevens CL, Klundt IL, Munk ME, Pillai MD (1965). «Amino ketone rearrangements. IV. Thermal rearrangements of α-amino methyl ketones». Journal of Organic Chemistry. 30 (9): 2967–72. doi:10.1021/jo01020a019.
- US patent 3254124, Stevens, Calvin L., «Aminoketones and methods for their production», issued 1966-05-31, assigned to Parke Davis & Co.
- BE 634208, Stevens, Calvin L., «Procédé de production d’aminocétones», issued 1963-07-15.
- ^ Krüger AD (1998). «[Current aspects of using ketamine in childhood]». Anaesthesiologie und Reanimation (in German). 23 (3): 64–71. PMID 9707751.
- ^ Chankvetadze B, Burjanadze N, Breitkreutz J, Bergander K, Bergenthal D, Kataeva O, Fröhlich R, Luftmann H, Blaschke G (2002). «Mechanistic study on the opposite migration order of the enantiomers of ketamine with α- and β-cyclodextrin in capillary electrophoresis». Journal of Separation Science. 25 (15–17): 1155–1166. doi:10.1002/1615-9314(20021101)25:15/17<1155::AID-JSSC1155>3.0.CO;2-M.
- ^ Feng N, Vollenweider FX, Minder EI, Rentsch K, Grampp T, Vonderschmitt DJ. Development of a gas chromatography-mass spectrometry method for determination of ketamine in plasma and its application to human samples. Ther. Drug Monit. 17: 95–100, 1995.
- ^ Parkin MC, Turfus SC, Smith NW, Halket JM, Braithwaite RA, Elliott SP, Osselton MD, Cowan DA, Kicman AT. Detection of ketamine and its metabolites in urine by ultra high pressure liquid chromatography-tandem mass spectrometry. J. Chrom. B 876: 137–142, 2008.
- ^ R. Baselt, Disposition of Toxic Drugs and Chemicals in Man, 8th edition, Biomedical Publications, Foster City, CA, 2008, pp. 806–808.
- ^
- ^ Li L, Vlisides PE (2016). «Ketamine: 50 Years of Modulating the Mind». Frontiers in Human Neuroscience. 10: 612. doi:10.3389/fnhum.2016.00612. PMC 5126726. PMID 27965560.
- ^ a b «Ketamine». Center for Substance Abuse Research (CESAR); University of Maryland, College Park. 29 October 2013. Archived from the original on 12 November 2013. Retrieved 27 July 2014.
- ^ Berman RM, Cappiello A, Anand A, Oren DA, Heninger GR, Charney DS, Krystal JH (February 2000). «Antidepressant effects of ketamine in depressed patients». Biol Psychiatry. 47 (4): 351–4. doi:10.1016/s0006-3223(99)00230-9. PMID 10686270. S2CID 43438286.
- ^ Chaffrey J (16 March 2022). «Yale Researchers Study Potential Treatment for Depression in Patients With Parkinson’s Disease». NBC Connecticut.
- ^ Dhir A (January 2017). «Investigational drugs for treating major depressive disorder». Expert Opinion on Investigational Drugs. 26 (1): 9–24. doi:10.1080/13543784.2017.1267727. PMID 27960559. S2CID 45232796.
- ^ Index Nominum 2000: International Drug Directory. Taylor & Francis. 2000. pp. 584–585. ISBN 978-3-88763-075-1.
- ^ Poisons Standard October 2015 «Poisons Standard». Australian Government. October 2015. Archived from the original on 19 January 2016. Retrieved 6 January 2016.
- ^ Legal status of ketamine in Canada references:
- «Statutes of Canada (S.C.) Controlled Drugs and Substances Act (S.C. 1996 c.19) Schedule I § 14». Justice Laws Website. Government of Canada. 12 June 2014. Archived from the original on 22 November 2013.
- «Order Amending Schedule I to the Controlled Drugs and Substances Act» (PDF). Canada Gazette Part II. Vol. 139, no. 19. 21 September 2005. p. 2130. Archived from the original (PDF) on 8 August 2014. Retrieved 2 August 2014.
- «Status of ketamine under CDSA». Canadian Society of Customs Brokers. 2 May 2005. Archived from the original on 10 August 2014. Retrieved 2 August 2014.
- ^ «Ketamine drug brought under ‘Schedule X’ to curb abuse». The Times of India. 7 January 2014. Archived from the original on 14 April 2014. Retrieved 2 August 2014.
- ^ Sumitra DR (30 December 2013). «Govt makes notorious ‘date rape’ drug ketamine harder to buy or sell». The Times of India. Archived from the original on 30 December 2013.
- ^ Baker N (12 February 2014), Response to ACMD recommendation on ketamine (PDF) (Correspondence to Les Iverson [chair of]; Advisory Council on the Misuse of Drugs), Crown copyright; Open Government Licence, archived (PDF) from the original on 28 February 2014, retrieved 21 February 2014.
- ^ Dixon H (12 February 2014). «Party drug ketamine to be upgraded to Class B». The Daily Telegraph. Archived from the original on 9 June 2014. Retrieved 2 August 2014.
- ^ Marshall DR (13 July 1999). «Schedules of Controlled Substances: Placement of Ketamine into Schedule III [21 CFR Part 1308. Final Rule 99-17803]» (PDF). Rules and Regulations. Federal Register. 64 (133): 37673–5. Archived (PDF) from the original on 5 May 2015.
- ^ Giannini AJ, Underwood NA, Condon M (November 2000). «Acute ketamine intoxication treated by haloperidol: a preliminary study». American Journal of Therapeutics. 7 (6): 389–91. doi:10.1097/00045391-200007060-00008. PMID 11304647.
- ^ Giannini AJ (1999). Drug Abuse. Los Angeles: Health Information Press. p. 104. ISBN 978-1-885987-11-2.
- ^ References for recreational use in literature:
- Lilly JC (1997). The Scientist: A Metaphysical Autobiography. Berkeley, CA: Ronin. pp. 144–. ISBN 978-0-914171-72-0.
- Kelly K (2001). The Little Book of Ketamine. Ronin. pp. 23, 40–45, 46–51, ibid. ISBN 978-1-57951-121-0.
- Alltounian HS, Moore M (1978). Journeys Into the Bright World. Rockport, MA: Para Research. ISBN 978-0-914918-12-7.
- Palmer C, Horowitz M (2000). Sisters of the Extreme: Women Writing on the Drug Experience. Inner Traditions. pp. 254–258, ibid. ISBN 978-0-89281-757-3.
- Turner DM (1994). The Essential Psychedelic Guide. San Francisco: Panther Press. ISBN 978-0-9642636-1-1.
- ^ Jansen K (2001). Ketamine: Dreams and Realities. Multidisciplinary Association for Psychedelic Studies. pp. 50, 89. ISBN 978-0-9660019-3-8.
- ^ Woodard D (2000). «The Ketamine Necromance». In Parfrey A (ed.). Apocalypse Culture II. Los Angeles: Feral House. pp. 288–295.
- ^ a b See Max Daly, 2014, «The Sad Demise of Nancy Lee, One of Britain’s Ketamine Casualties,» at Vice (online), 23 July 2014, see «The Sad Demise of Nancy Lee, One of Britain’s Ketamine Casualties». 23 July 2014. Archived from the original on 7 June 2015. Retrieved 7 June 2015., accessed 7 June 2015.
- ^ «Drug related deaths involving ketamine in England and Wales». A report of the Mortality team, Life Events and Population Sources Division, Office for National Statistics. Government of the United Kingdom. 2013. Archived from the original on 7 June 2015. Retrieved 7 June 2015. and «Deaths Related to Drug Poisoning in England and Wales – Office for National Statistics». Archived from the original on 19 June 2015. Retrieved 7 June 2015., accessed 7 June 2015.
- ^ «Do you know… Ketamine». Knowledge Exchange. Toronto: Centre for Addiction and Mental Health. 2003. Archived from the original on 7 April 2014. Retrieved 27 July 2014.
- ^ Grinspoon P (9 August 2022). «Ketamine for treatment-resistant depression: When and where is it safe?». Harvard Health. Retrieved 6 September 2022.
- ^ «New Hope for Treatment-Resistant Depression: Guessing Right on Ketamine». National Institute of Mental Health (NIMH). Retrieved 6 September 2022.
- ^ Pérez-Esparza R (2018). «Ketamine for Treatment-Resistant Depression: a New Advocate». Revista de Investigacion Clinica. 70 (2): 65–67. doi:10.24875/RIC.18002501. PMID 29718013.
- ^ Li N, Lee B, Liu RJ, Banasr M, Dwyer JM, Iwata M, et al. (August 2010). «mTOR-dependent synapse formation underlies the rapid antidepressant effects of NMDA antagonists». Science. 329 (5994): 959–964. Bibcode:2010Sci…329..959L. doi:10.1126/science.1190287. PMC 3116441. PMID 20724638.
- ^ Maia M (29 March 2022). «Ketamine Eases Parkinson’s Patients’ Levodopa-induced Dyskinesia». Retrieved 11 September 2022.
- ^ Nalbantoglu S (4 March 2022). «Yale researchers study ketamine as a potential treatment for depression in patients with Parkinson’s disease». Yale Daily News. Retrieved 11 September 2022.
- ^ «Using Ketamine to Treat Depression in Parkinson’s Disease». www.michaeljfox.org. Retrieved 11 September 2022.
- ^ Robertson SA, Taylor PM (October 2004). «Pain management in cats—past, present and future. Part 2. Treatment of pain—clinical pharmacology». Journal of Feline Medicine and Surgery. 6 (5): 321–33. doi:10.1016/j.jfms.2003.10.002. PMID 15363764. S2CID 25572412.
- ^ Lamont LA (November 2008). «Adjunctive analgesic therapy in veterinary medicine». The Veterinary Clinics of North America. Small Animal Practice. 38 (6): 1187–203, v. doi:10.1016/j.cvsm.2008.06.002. PMID 18954680.
- ^ Stunkard JA, Miller JC (September 1974). «An outline guide to general anesthesia in exotic species». Veterinary Medicine, Small Animal Clinician. 69 (9): 1181–6. PMID 4604091.
- ^ Riviere JE, Papich MG (2009). Veterinary Pharmacology and Therapeutics. John Wiley & Sons. p. 200. ISBN 978-1-118-68590-7.
- ^ Standard Operating Procedure No. 1 Anesthesia and Analgesia in Rodents, Washington College, 2012, pp. 1–2, archived from the original on 4 August 2013, retrieved 27 November 2015
- ^ Hubbell JA, Muir WW, Sams RA (November 1980). «Guaifenesin: cardiopulmonary effects and plasma concentrations in horses». American Journal of Veterinary Research. 41 (11): 1751–5. PMID 7212404.
- ^ Woodall AJ, McCrohan CR (December 2000). «Excitatory actions of propofol and ketamine in the snail Lymnaea stagnalis«. Comparative Biochemistry and Physiology. Toxicology & Pharmacology. 127 (3): 297–305. doi:10.1016/S0742-8413(00)00155-9. PMID 11246501.
External links[edit]
Wikimedia Commons has media related to Ketamine.
- Ketamine — from the U.S. National Library of Medicine (NLM) Drug Information Portal
- Ketamine hydrochloride — from the U.S. National Library of Medicine (NLM)Drug Information Portal
- Ketamine fact sheet — from the United States DEA, via Archive.org