У этого термина существуют и другие значения, см. Оксид серы.
| Оксид серы(IV) | |
 |
|
 |
|
| Общие | |
|---|---|
| Систематическое наименование | Оксид серы (IV) |
| Химическая формула | SO2 |
| Физические свойства | |
| Состояние (ст. усл.) | бесцветный газ |
| Отн. молек. масса | 64.054 а. е. м. |
| Молярная масса | 64.054 г/моль |
| Плотность | 0,002927 г/см³ |
| Термические свойства | |
| Температура плавления | −75,5 °C |
| Температура кипения | −10,01 °C |
| Химические свойства | |
| Растворимость в воде | 11,5 г/100 мл |
| Классификация | |
| Рег. номер CAS | [7446-09-5] |
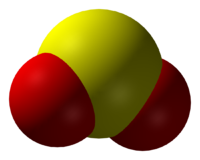
Окси́д се́ры (IV) (диокси́д се́ры, се́рнистый газ, се́рнистый ангидри́д) — SO2. В нормальных условиях представляет собой бесцветный газ с характерным резким запахом (запах загорающейся спички). Под давлением сжижается при комнатной температуре. Растворяется в воде с образованием нестойкой се́рнистой кислоты; растворимость 11,5 г/100 г воды при 20 °C, снижается с ростом температуры. Растворяется также в этаноле, се́рной кислоте. SO2 — один из основных компонентов вулканических газов.
Содержание
- 1 Получение
- 2 Химические свойства
- 3 Применение
- 4 Физиологическое действие
- 5 Воздействие на атмосферу
- 6 Примечания
- 7 Литература
Получение
Промышленный способ получения — сжигание серы или обжиг сульфидов, в основном — пирита:
В лабораторных условиях SO2 получают воздействием сильных кислот на сульфиты и гидросульфиты. Образующаяся сернистая кислота H2SO3 сразу разлагается на SO2 и H2O:
Также диоксид серы можно получить действием концентрированной серной кислоты на малоактивные металлы при нагревании:
Химические свойства
Спектр поглощения SO2 в ультрафиолетовом диапазоне
Относится к кислотным оксидам. Растворяется в воде с образованием сернистой кислоты (при обычных условиях реакция обратима):
Со щелочами образует сульфиты:
Химическая активность SO2 весьма велика. Наиболее ярко выражены восстановительные свойства SO2, степень окисления серы в таких реакциях повышается:
Последняя реакция является качественной реакцией на сульфит-ион SO32− и на SO2 (обесцвечивание фиолетового раствора).
В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства. Например, для извлечения серы из отходящих газов металлургической промышленности используют восстановление SO2 оксидом углерода(II):
Или для получения фосфорноватистой кислоты:
Применение
Большая часть оксида серы (IV) используется для производства серной кислоты. Используется также в слабоалкогольных напитках (вина средней ценовой категории) в качестве консерванта (пищевая добавка E220). Так как этот газ убивает микроорганизмы, им окуривают овощехранилища и склады. Оксид серы (IV) используется для отбеливания соломы, шелка и шерсти, то есть материалов, которые нельзя отбеливать хлором. Применяется он также и в качестве растворителя в лабораториях. При таковом его применении следует помнить о возможном содержании в SO2 примесей в виде SO3, H2O, и как следствие присутствия воды H2SO4 и H2SO3. Их удаляют пропусканием через растворитель концентрированной H2SO4; это лучше делать под вакуумом или в другой закрытой аппаратуре[1]. Оксид серы (IV) применяется также для получения различных солей сернистой кислоты.
Физиологическое действие
SO2 очень токсичен. Симптомы при отравлении сернистым газом — насморк, кашель, охриплость, сильное першение в горле и своеобразный привкус. При вдыхании сернистого газа более высокой концентрации — удушье, расстройство речи, затруднение глотания, рвота, возможен острый отёк лёгких.
При кратковременном вдыхании оказывает сильное раздражающее действие, вызывает кашель и першение в горле.
- ПДК(предельно допустимая концентрация):
- в атмосферном воздухе максимально-разовая — 0,5 мг/м³, среднесуточная — 0,05 мг/м³;
- в помещении (рабочая зона) — 10 мг/м³
Интересно, что чувствительность по отношению к SO2 весьма различна у отдельных людей, животных и растений. Так, среди растений наиболее устойчивы по отношению к сернистому газу берёза и дуб, наименее — роза, сосна и ель.
Воздействие на атмосферу
Из-за образования в больших количествах в качестве отходов диоксид серы является одним из основных газов, загрязняющих атмосферу.
Наибольшую опасность представляет собой загрязнение соединениями серы, которые выбрасываются в атмосферу при сжигании угольного топлива, нефти и природного газа, а также при выплавке металлов и производстве серной кислоты.
Антропогенное загрязнение серой в два раза превосходит природное[источник не указан 62 дня]. Серный ангидрид образуется при постепенном окислении сернистого ангидрида кислородом воздуха с участием света. Конечным продуктом реакции является аэрозоль серной кислоты в воздухе, раствор в дождевой воде (в облаках). Выпадая с осадками, она подкисляет почву, обостряет заболевания дыхательных путей, скрыто угнетающе воздействует на здоровье человека. Выпадение аэрозоля серной кислоты из дымовых факелов химических предприятий чаще отмечается при низкой облачности и высокой влажности воздуха. Растения около таких предприятий обычно бывают густо усеяны мелкими некротическими пятнами, образовавшимися в местах оседания капель серной кислоты, что доказывает присутствие ее в окружающей среде в существенных количествах. Пирометаллургические предприятия цветной и чёрной металлургии, а также ТЭЦ ежегодно выбрасывают в атмосферу десятки миллионов тонн серного ангидрида.
Наибольших концентраций сернистый газ достигает в северном полушарии, особенно над территорией США, Европы, Китая, европейской части России и Украины. В южном полушарии содержание его значительно ниже.
Примечания
- ↑ Гордон А., Форд Р. Спутник химика / Пер. на русск. Е. Л. Розенберга, С. И. Коппель. — М.: «Мир», 1976. — 544 с.
Литература
- Ахметов Н. С. «Общая и неорганическая химия» М.: Высшая школа, 2001
- Карапетьянц М. Х., Дракин С. И. «Общая и неорганическая химия» М.: Химия 1994
Окси́ды се́ры, окси́ды се́ры — сера образует несколько оксидов (бинарных соединений с кислородом), из которых наибольшей устойчивостью и значением отличаются два высших: диоксид серы и триоксид серы. Вместе с тем, и низшие оксиды представляют серьёзный интерес, в том числе, и научный:
Оксиды серы[править]
- Оксид серы(I) или закись серы, формула S2О — бесцветный газ, неустойчивый при нормальных условиях.
- Оксид серы(II) или моноокись серы, формула SО — бесцветный газ, радикал, крайне неустойчивый при нормальных условиях.
- Оксид серы(IV), диоксид серы, сернистый газ или сернистый ангидрид, формула SO2 — бесцветный газ с резким характерным запахом.
- Оксид серы(VI), триоксид серы, серный ангидрид или серный газ, формула SO3 — высший оксид серы, летучая жидкость с удушливым запахом.
Оксиды серы в разных версиях[править]
|
|
…продуктами этой давно известной реакции является не только SO2 (сернистый газ) и Н2O, но в весьма значительных количествах появляется и такой «экзотический» продукт, как SO. В первых стадиях реакции SO появляется в очень большом количестве, достигая 7% от исходного вещества и до 40% от превращенного к этому моменту H2S, и лишь в конечных стадиях SO исчезает, переходя в SO2.[1] |
|
|
Низший окисел серы получается при пропускании слабого <электрического> разряда в SO2, а также другими способами. Долгое время считали его соединением <с формулой> SO, однако газообразный продукт такого состава представляет собой эквимольную смесь S2O и SO2. Чрезвычайно реакционноспособный бирадикал SO можно обнаружить, однако, как промежуточный продукт в реакциях, а (SO)2 также обнаруживается при помощи масс-спектрометра.[2]:II:397 |
| — Коттон Ф., Уилкинсон Дж. «Современная неорганическая химия» (том второй), 1961 |
|
|
Сера с кислородом образует несколько оксидов: S2O2, S2O3, SO2, SO3, S2O7, SO4 и большое число кислородных кислот. Оксиды — S2O7 и SO4 — являются её пероксидными соединениями. Наибольшее значение имеют SO2 и SO3. Остальные оксиды неустойчивы и образуются в особых условиях.[4]:266 |
| — Сергей Оленин, Герман Фадеев, «Неорганическая химия», 1978 |
Источники[править]
- ↑ Семёнов Н. Н. Теория цепных реакций (из статьи «Теория горения»). — М.: «Наука и жизнь» № 8-9, 1940 г.
- ↑ Коттон Ф., Уилкинсон Дж. Современная неорганическая химия, часть 2 (пер. с англ.: Иванова Е.К., Прохорова Г.В., Чуранов С.С. Под ред.: Астахов К.В.) — М.: Мир, 1969 г.
- ↑ Б. В. Некрасов. Основы общей химии (в двух томах), издание 2-е, стереотипное. Том первый. ― М.: Химия, 1968-1969 г. — стр.325-326
- ↑ С. С. Оленин, Г. Н. Фадеев, Неорганическая химия (для медико-биологических специальностей). — М.: «Высшая школа», 1979 г.
См. также[править]
- Олеум
- Сера
- Серная кислота
- Сернистая кислота
- Купоросное масло
- Сероводород
- Кислотный дождь
- Серный дождь
Поиск химических веществ по названиям или формулам.
Справочник содержит названия веществ и описания химических формул (в т.ч. структурные формулы и скелетные формулы).
Введите часть названия или формулу для поиска:
Общее число найденных записей: 298.
Показано записей: 20.
1. Оксид серы(IV)
Брутто-формула:
O2S
CAS# 7446-09-5
Названия
Русский:
- Оксид серы(IV)(IUPAC) [Wiki]
- двуокись серы
- диоксид серы
- сернистый ангидрид
- сернистый газ
;
;
;
;
;
English:
- Caswell No. 813
- E 220
- EINECS:231-195-2
- Fermenicide liquid
- Fermenicide powder
- Fermenticide liquid
- Schwefeldioxid
- Sulfur dioxide(IUPAC) [Wiki]
- Sulfur dioxide (SO2)
- Sulfur oxide (SO2)
- Sulfur superoxide
- Sulfur(IV) oxide
- Sulfurous acid anhydride
- Sulfurous anhydride
- Sulfurous oxide
- Sulfuroxide
- Sulfursuperoxide (6CI)
- UN 1079
- sulphur dioxide
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
2. Оксид серы(VI)
Брутто-формула:
O3S
CAS# 7446-11-9
Названия
Русский:
- Оксид серы(VI) [Wiki]
- серный ангидрид
- серный газ
- треокись серы
- триоксид серы
;
;
;
;
;
English:
- 227692_ALDRICH
- 425478_ALDRICH
- AC1Q6YFD
- Sulfan
- Sulfite radical anion
- Sulfonylideneoxidane
- Sulfur trioxide(CAS) [Wiki]
- Sulfuric anhydride
- Sulphur trioxide
- UN 1829
- oxosulfane dioxide
;
;
;
;
;
;
;
;
;
;
;
3. Пиросульфурил хлористый
Брутто-формула:
Cl2O5S2
CAS# 7791-27-7
Названия
Русский:
- Пиросульфурил хлористый
- дисеры(VI) пентаоксид-дихлорид
- хлорангидрид пиросерной кислоты
;
;
;
English:
- Chlorosulfonic anhydride
- Disulfur pentoxydichloride
- Disulfuryl chloride
- PYROSULFURYL CHLORIDE
- Sulfur pentoxydichloride
- UN1817
;
;
;
;
;
;
Cl/S<_qq4O><_pp4O>/OS<_qq4O><_pp4O>Cl
4. метиловый спирт
Брутто-формула:
CH4O
CAS# 67-56-1
Названия
Русский:
- Метанол(IUPAC) [Wiki]
- гидроксид метила
- древесный спирт
- карбинол
- метилгидрат
- метиловый спирт
;
;
;
;
;
;
English:
- Colonial Spirit
- EINECS:212-378-6
- Hydroxymethane
- Methanol(IUPAC)(CAS) [Wiki]
- Methyl hydrate
- Methyl hydroxide
- Methylic alcohol
- Methylol
- Pyroxylic spirit
- Wood alcohol
- Wood naphtha
- Wood spirit
- carbinol
- methyl alcohol
;
;
;
;
;
;
;
;
;
;
;
;
;
;
$slope(55)H/C<_(A-160,w+)H><_(A-100,d+)H>-O/H
5. Этиленоксид
Брутто-формула:
C2H4O
CAS# 75-21-8
Названия
Русский:
- 1,2-эпоксиэтан
- Окись этилена(IUPAC) [Wiki]
- Этиленоксид
- оксиран
;
;
;
;
English:
- Ethylene oxide(IUPAC) [Wiki]
- Oxirane(CAS)
- dimethylene oxide
- epoxyethane
- oxacyclopropane
;
;
;
;
;
C_(x1.4)C_q3O_q3; H_(A-15,d-)#1_(A110,w+)H; H_(A-165,d-)#2_(A70,w+)H;
$L(1.4)C_(A0)C_q3O_q3; H_(x1)#1_p3H;H_(x-1)#2_q3H
6. Триметиленоксид
Брутто-формула:
C3H6O
Названия
Русский:
- Оксетан(IUPAC)
- Триметиленоксид
;
;
English:
- 1,3-epoxypropane
- 1,3-propylene oxide
- Oxetane(IUPAC)
- oxacyclobutane
- trimethylene oxide
;
;
;
;
;
H|C|C|H; H|C|$atomColor1(blue)O; H-#2-#6-H; H-#3-#O
7. Гексаметиленоксид
Брутто-формула:
C6H12O
Названия
Русский:
- Гексаметиленоксид
- Оксепан(IUPAC)
;
;
English:
- Oxepane
;
8. Вода
Брутто-формула:
H2O
CAS# 7732-18-5
Названия
Русский:
- Вода [Wiki]
- Оксид водорода(IUPAC)
;
;
English:
- Dihydrogen oxide
- Water(CAS) [Wiki]
- oxidane(IUPAC)
;
;
;
9. Углекислый газ
Брутто-формула:
CO2
Названия
Русский:
- Оксид углерода(IV)(IUPAC)
- Углекислый газ
- двуокись углерода
- диоксид углерода
- угольный ангидрид
;
;
;
;
;
English:
- Carbon dioxide
- Carbon oxide
- Carbon(IV) oxide
- Carbonic acid gas
- Carbonic anhydride
- Carbonic oxide
- Dry ice
;
;
;
;
;
;
;
10. Оксид фосфора(V)
Брутто-формула:
O10P4
Названия
Русский:
- Оксид фосфора(V)
- Пентаоксид фосфора
- пятиокись фосфора
- фосфорный ангидрид
;
;
;
;
English:
- Diphosphorus pentoxide
- Phosphoric anhydride
- Phosphoric oxide
- Phosphoric pentoxide
- Phosphorus oxide
- Phosphorus pentaoxide
- Phosphorus pentoxide
;
;
;
;
;
;
;
$slope(15)$L(1.5)O||P`/O|P:l`/O/O/P:rO«|O`_(A120)O|P<`/O_#l><O_#r>_(A120,N2)O
11. Гидроксид калия
Брутто-формула:
HKO
CAS# 1310-58-3
Названия
Русский:
- Гидроксид калия(IUPAC) [Wiki]
- Кали едкое
- гидроокись калия
- калия гидроксид
- каустический поташ
;
;
;
;
;
English:
- Caustic potash
- E525
- Potash lye
- Potassia
- Potassium hydrate
- Potassium hydroxide(IUPAC) [Wiki]
;
;
;
;
;
;
12. Гидроксид натрия
Брутто-формула:
HNaO
CAS# 1310-73-2
Названия
Русский:
- Гидроксид натрия(IUPAC) [Wiki]
- гидроокись натрия
- едкая щелочь
- едкий натр
- каустик
- каустическая сода
- натрия гидроксид
;
;
;
;
;
;
;
English:
- Ascarite
- Caustic soda
- E524
- Lye
- Sodium hydrate
- Sodium hydroxide(IUPAC) [Wiki]
- Sodium oxidanide
- White caustic
;
;
;
;
;
;
;
;
13. Гидроксид кальция
Брутто-формула:
H2CaO2
CAS# 1305-62-0
Названия
Русский:
- Гидроксид кальция(IUPAC) [Wiki]
- гашёная известь
- гидроокись кальция
- кальция гидроксид
;
;
;
;
English:
- Calcium hydroxide(IUPAC) [Wiki]
- Calcium(II) hydroxide
- E526
- Hydrated lime
- Milk of lime
- Pickling lime
- Slaked lime
;
;
;
;
;
;
;
$L(1.5)HO^-Ca^2+/0`HO^-
14. Оксид кальция
Брутто-формула:
CaO
CAS# 1305-78-8
Названия
Русский:
- Оксид кальция(IUPAC) [Wiki]
- кальция оксид
- окись кальция, негашёная и́звесть
;
;
;
English:
- Calcia
- Calciogreen
- Calcium oxide(IUPAC) [Wiki]
- Calciumoxide (CaO)
- EINECS:215-138-9
- Oxocalcium(IUPAC)
- Quicklime
- burnt lime
- unslaked lime
;
;
;
;
;
;
;
;
;
15. Оксид магния
Брутто-формула:
MgO
Названия
Русский:
- Жжёная магнезия
- Оксид магния(IUPAC)
- магния окись
- магния оксид
- периклаз
;
;
;
;
;
English:
- Magnesia
- Magnesium oxide(IUPAC)
- Periclase
;
;
;
16. Гидроксид магния
Брутто-формула:
H2MgO2
CAS# 1309-42-8
Названия
Русский:
- Гидроксид магния(IUPAC)
- магния гидроксид
;
;
English:
- Magnesium hydroxide(IUPAC)
- Magnesium hydroxide, (Mg(OH)2)(CAS)
- Milk of magnesia
;
;
;
H/O^-$L(1.4)hMg^++/hO^-$L()H
17. Гидроксид аммония
Брутто-формула:
H5NO
CAS# 1336-21-6
Названия
Русский:
- Аммония гидрооксид
- Гидрат аммиака(IUPAC) [Wiki]
- Гидроксид аммония
- аммиачная вода
- едкий аммиак
- едкий аммоний
;
;
;
;
;
;
English:
- Ammonium hydroxide [Wiki]
- E527
- EINECS:215-647-6
- ammonia liquor
- ammonia water
- ammonical liquor
- aqua ammonia
- aqueous ammonia
;
;
;
;
;
;
;
;
H/N^+<`|H><_(A80,w+)H>_(A15,d+)H`|0O`^-# -H
18. Оксид бора
Брутто-формула:
B2O3
CAS# 1303-86-2
Названия
Русский:
- Борный ангидрид
- Оксид бора [Wiki]
- ангидрид борной кислоты
;
;
;
English:
- Boracicanhydride
- Boria (B2O3)
- Boric acid (HBO2), anhydride
- Boric acid anhydride
- Boric acidanhydride
- Boric anhydride
- Boron trioxide [Wiki]
- Boron(III) oxide
- Boronsesquioxide
- EINECS:215-125-8
- Fused boricacid
- boria
- boric oxide
- boron oxide
- boron sesquioxide
- diboron trioxide
- oxo(oxoboranyloxy)borane(IUPAC)
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
;
19. Диоксан
Брутто-формула:
C4H8O2
CAS# 123-91-1
Названия
Русский:
- 1,4-диоксан(IUPAC)
- Диоксан
- диэтилендиоксид
;
;
;
English:
- 1,4-Diethylene dioxide
- 1,4-Diethyleneoxide
- 1,4-Dioxacyclohexane(IUPAC)
- 1,4-Dioxan
- 1,4-Dioxane(IUPAC)
- Dioxane
- [1,4]Dioxane
- [6]-crown-2
- p-Dioxane
;
;
;
;
;
;
;
;
;
$slope(15)O<_(A-120)H><|H>/<`|H><H>_(A60)O_(A-165,W+)<`|H><_(A60,w1)H>_(A165)<|H><`H>_(W-)#1
20. Пероксид водорода
Брутто-формула:
H2O2
CAS# 7722-84-1
Названия
Русский:
- Пероксид водорода
- перекись водорода
;
;
English:
- Albone
- Dioxidane
- Hioxyl
- Hydrogen dioxide
- Hydrogen peroxide(IUPAC)
- Inhibine
- Oxidanyl
- Peroxaan
- Superoxol
- dihydrogen dioxide(IUPAC)
- hydroperoxide
- oxydol
- perhydrol
;
;
;
;
;
;
;
;
;
;
;
;
;
…
Сероводород
Получение
сероводорода
- Получение из простых веществ:
S + Н2 = H2S
- Взаимодействие минеральных кислот и сульфидов металлов, расположенных в ряду напряжений левее железа:
FeS + 2HCI = H2S↑ + FeCl2
- Действие концентрированной H2SO4 (без избытка) на щелочные и щелочно-земельные металлы:
5H2SO4(конц.) + 8Na = H2S↑ + 4Na2SO4 + 4H2О
- Гидролиз некоторых сульфидов:
AI2S3 + 6Н2О = 3H2S↑ + 2Аl(ОН)3↓
- Нагревание парафина с серой:
C40H82
+ 41S = 41Н2S+40С
Видео Получение и обнаружение сероводорода
Физические
свойства и строение сероводорода
Сероводород H2S – это бинарное летучее водородное соединение соединение с серой. H2S
— бесцветный ядовитый газ, с неприятным удушливым
запахом тухлых яиц. При концентрации > 3 г/м3 вызывает смертельное отравление.
Сероводород тяжелее воздуха и легко конденсируется в бесцветную жидкость. Растворимость в воде H2S при обычной температуре составляет 2,5.
В твердом состоянии имеет молекулярную кристаллическую решетку.
Геометрическая форма молекулы сероводорода представляет собой сцепленные между собой атомы H-S-H с валентным углом 92,1о.

Качественная реакция для обнаружения сероводорода
Для
обнаружения анионов S2- и сероводорода используют
реакцию газообразного H2S с Pb(NO3)2:
H2S + Pb(NO3)2 = 2HNO3 + PbS↓ черный
осадок.
Влажная бумага, смоченная в растворе Pb(NO3)2 чернеет в присутствии H2S из-за получения черного осадка PbS.
Химические свойства серы
H2S является сильным восстановителем
При взаимодействии H2S с окислителями образуются различные вещества — S, SО2, H2SO4
- Окисление кислородом воздуха:
2H2S + 3О2(избыток) = 2SО2↑ + 2Н2О
2H2S + О2(недостаток) = 2S↓ + 2Н2О
- Окисление галогенами:
H2S + Br2 = S↓ + 2НВr
H2S + Cl2 → 2HCl + S↓
H2S + 4Cl2 + 4H2O → H2SO4 + 8HCl
- Взаимодействие с кислотами-окислителями:
3H2S + 8HNО3(разб.) = 3H2SO4 + 8NO + 4Н2О
H2S + 8HNО3(конц.) = H2SO4 + 8NО2↑ + 4Н2О
H2S + H2SO4(конц.) = S↓ + SО2↑ + 2Н2О
- Взаимодействие со сложными окислителями:
5H2S + 2KMnO4 + 3H2SO4 = 5S↓ + 2MnSO4 + K2SO4 + 8Н2О
5H2S + 6KMnO4 + 9H2SO4 = 5SО2 + 6MnSO4 + 3K2SO4 + 14Н2О
H2S + 2FeCl3 = S↓ + 2FeCl2 + 2HCl
2H2S + SO2 = 2H2O + 3S
3H2S + K2Cr2O7 + 4H2SO4 → 3S + Cr2(SO4)3 + K2SO4 + 7H2O
- Сероводородная кислота H2S двухосновная кислота и диссоциирует по двум ступеням:
1-я ступень:
H2S → Н+ + HS—
2-я ступень:
HS— → Н+ + S2-
H2S очень слабая
кислота, несмотря на это имеет характерные для кислот химические свойства. Взаимодействует:
- с активными металлами
H2S + Mg = Н2↑ + MgS
- с малоактивными металлами (Аg, Си, Нg) при совместном присутствии окислителей:
2H2S + 4Аg + O2 = 2Ag2S↓ + 2Н2O
- с основными оксидами:
H2S + ВаО = BaS + Н2O
- со щелочами:
H2S + NaOH(недостаток) = NaHS + Н2O
H2S + 2NaOH(избыток) → Na2S + 2H2O
- с аммиаком:
H2S + 2NH3(избыток) = (NH4)2S
- с некоторыми солями сильных кислот, если образующийся сульфид металла нерастворим в воде и в сильных кислотах:
CuSO4 + H2S = CuS↓ + H2SO4
H2S + Pb(NO3)2 → PbS↓ + 2HNO3
Реакция
с нитратом свинца в растворе – это качественная реакция
на сероводород и сульфид-ионы.
Видео Взаимодействие сероводорода с нитратом свинца
Сульфиды
Получение сульфидов
- Непосредственно из простых веществ:
S + Fe → FeS
S + Mg → MgS
S + Ca → CaS
- Взаимодействие H2S с растворами щелочей:
H2S + 2NaOH = 2H2O + Na2S
H2S + NaOH = H2O + NaHS
- Взаимодействие H2S или (NH4)2S с растворами солей:
H2S + CuSO4 = CuS↓ + H2SO4
H2S + 2AgNO3 = Ag2S↓ + 2HNO3
Pb(NO3)2 + Н2S → PbS↓ + 2НNO3
ZnSO4 + Na2S → ZnS↓ + Na2SO4
- Восстановление сульфатов при прокаливании с углем:
Na2SO4 + 4С = Na2S + 4СО
Физические свойства сульфидов
Сульфиды – это бинарные соединения серы с элементами с меньшей электроотрицательностью, в том числе с некоторыми неметаллами (С, Si, Р, As и др.).
По растворимости
в воде и кислотах сульфиды классифицируют
на:
- растворимые в воде — сульфиды щелочных металлов и аммония;
- нерастворимые в воде, но растворимые в минеральных кислотах — сульфиды металлов, расположенных до железа в ряду активности (белые и цветные сульфиды ZnS, MnS, FeS, CdS);
- нерастворимые ни в воде, ни в минеральных кислотах — черные сульфиды (CuS, HgS, PbS, Ag2S, NiS, CoS)
- гидролизуемые водой — сульфиды трехвалентных металлов (алюминия и хрома (III))
По цвету сульфиды можно разделить на:
- Чёрные – HgS, Ag2S, PbS, CuS, FeS,
NiS; - Коричневые – SnS, Bi2S3;
- Оранжевые – Sb2S3, Sb2S5;
- Жёлтые – As2S3, As2S5,
SnS2, CdS; - Розовые — MnS
- Белые – ZnS, Al2S3, BaS,
CaS;
Химические свойства сульфидов
Обратимый гидролиз сульфидов
- Хорошо растворимыми в воде являются сульфиды щелочных металлов и аммония, но в водных растворах они в значительной степени подвергаются гидролизу. Реакция среды — сильнощелочная:
K2S + H2O ⇄ KHS + KOH
S2- + H2O → HS— + ОН—
- Сульфиды щелочно-земельных металлов и Mg, при взаимодействии с водой подвергаются полному гидролизу и переходят в растворимые кислые соли — гидросульфиды:
2CaS + 2НОН
= Ca(HS)2 + Са(ОН)2
При нагревании растворов сульфидов гидролиз протекает и по 2-й ступени:
HS— + H2O → H2S↑ + ОН—
Необратимый
гидролиз сульфидов
- Сульфиды некоторых металлов (Cr2S3, Fe2S3, Al2S3) подвергаются необратимому гидролизу, полностью разлагаясь в водных растворах:
Al2S3 + 6H2O = 3H2S↑ + 2AI(OH)3↓
Нерастворимые
сульфиды гидролизу не подвергаются
NiS + HСl ≠
- Некоторые из сульфидов растворяются в сильных кислотах:
FeS + 2HCI =
FeCl2 + H2S↑
ZnS + 2HCI =
ZnCl2 + H2S↑
CuS + 8HNO3 → CuSO4 + 8NO2 + 4H2O
CuS + 4H2SO4(конц. гор.) → CuSO4 + 4SO2 + 4H2O
MnS + 3HNO3 = MnSO4 + 8NO2 + 4H2O
- Сульфиды Ag2S, HgS, Hg2S, PbS, CuS не pacтворяются не только в воде, но и во многих кислотах.
- Сульфиды обладают восстановительными свойствами и вступают в реакции с окислителями:
PbS + 4H2O2 → PbSO4 + 4H2O
СuS + Cl2 → CuCl2 + S
-
Окислительный обжиг сульфидов является
важной стадией переработки сульфидного сырья в различных производствах
2ZnS + 3O2 = 2ZnO + 2SO2
4FeS2 + 11O2 = 2Fe2O3 + 8SO2↑
2CuS + 3O2 → 2CuO + 2SO2
2Cr2S3 + 9O2 → 2Cr2O3 + 6SO2
Взаимодействия
сульфидов с растворимыми солями свинца, серебра, меди являются качественными на ион S2−:
Na2S + Pb(NO3)2 → PbS↓ + 2NaNO3
Na2S + 2AgNO3 → Ag2S↓ + 2NaNO3
Na2S + Cu(NO3)2 → CuS↓ + 2NaNO3
Оксид серы
(IV), диоксид серы, сернистый газ, сернистый ангидрид (SO2)
Способы получения сернистого газа
- Окисление серы, сероводорода и сульфидов кислородом воздуха:
S + O2 → SO2
2H2S + 3O2 → 2SO2 + 2H2O
2CuS + 3O2 → 2SO2 + 2CuO
- Действие высокой температуры на сульфиты (термическое разложение):
CaSO3 = СаО + SO2↑
- Действие сильных кислот на сульфиты:
Na2SO3 + 2HCl = SO2 + Н2O + 2NaCI
- Взаимодействие концентрированной H2SO4 с восстановителями, например с неактивными металлами:
2H2SO4 + Сu = SO2↑ + CuSO4 + 2Н2O
Физические
свойства сернистого газа
При обычной температуре SO2 — газ с резким запахом без цвета. В воде растворим хорошо — при 20°С в 1 л воды растворяется 40 л SO2.
Химические свойства сернистого газа
SO2 – типичный кислотный оксид. За счет того, что сера находится в промежуточной степени окисления (+4) SO2 может проявлять свойства как окислителя так и восстановителя.
- При растворении в воде SO2 частично соединяется с молекулами воды с образованием слабой сернистой кислоты.
SO2 + H2O ↔ H2SO3
- Как
кислотный оксид, SO2 вступает
в реакции с щелочами и оксидами щелочных и щелочноземельных металлов:
SO2 + СаО = CaSO3
SO2 + Na2O → Na2SO3
SO2 + NaOH = NaHSO3
SO2 + 2NaOH = Н2O + Na2SO3
- При взаимодействии с окислителями SO2 проявляет восстановительные свойства. При этом степень окисления серы повышается:
2SO2 + O2 ↔ 2SO3
SO2 + Br2 + 2H2O → H2SO4 + 2HBr
SO2 + 2HNO3 → H2SO4 + 2NO2
SO2 + O3 → SO3 + O2
SO2 + PbO2 → PbSO4
5SO2 + 2H2O + 2KMnO4 → 2H2SO4 + 2MnSO4 + K2SO4
Обесцвечивание раствора перманганата калия KMnO4 является качественной реакцией для обнаружения сернистого газа и сульфит-иона
- SO2 проявляет окислительные свойства при взаимодействии с сильными восстановителями, восстанавливаясь чаще всего до свободной серы:
SO2 + 2Н2S → 3S↓ + 2H2O
SO2 + 2CO → S↓ +2СО2
SO2 + С → S↓ + СO2
Оксид серы (VI), триоксид серы, серный ангидрид (SO3)
Способы получения серного ангидрида
- SO3 можно получить из SO2 путем каталитического окисления последнего кислородом:
2SO2 + O2 ↔ 2SO3
- Окислением SO2 другими окислителями:
SO2 + O3 → SO3 + O2
SO2 + NO2 → SO3 + NO
- Разложением сульфата железа (III):
Fe2(SO4)3 → Fe2O3 + 3SO3
Физические
свойства серного ангидрида
При обычных условиях SO3 представляет собой бесцветную жидкость с характерным резким
запахом. На воздухе SO3 «дымит» и сильно
поглощает влагу.
SO3 – тяжелее
воздуха, хорошо растворим в воде.
SO3 ядовит!
Химические свойства серного
ангидрида
Оксид серы (VI) – это кислотный оксид.
- Хорошо поглощает влагу и реагирует с водой образуя серную кислоту:
SO3 + H2O → H2SO4
- Как
кислотный оксид, SO3 взаимодействует с щелочами и
основными оксидами, образуются средние или кислые соли:
SO3 + 2NaOH(избыток) → Na2SO4 + H2O
SO3 + NaOH(избыток) → NaHSO4
SO3 + MgO → MgSO4 (при сплавлении):
SO3 + ZnO = ZnSO4
-
SO3 проявляет
сильные окислительные свойства, так
как сера в находится в максимальной степени окисления (+6).
Вступает в реакции с восстановителями:
SO3 + 2KI → I2 + K2SO3
3SO3 + H2S → 4SO2 + H2O
5SO3 + 2P → P2O5 + 5SO2
- При растворении в концентрированной
серной кислоте образует олеум (раствор
SO3 в H2SO4).
Сернистая кислота (H2SO3)
Способы
получения сернистой кислоты
При растворении в воде SO2 образует слабую сернистую кислоту, которая сразу частично разлагается:
SO2 + H2O ↔ H2SO3
Физические
свойства сернистой кислоты
Сернистая кислота H2SO3 – двухосновная кислородсодержащая кислота. При обычных условиях неустойчива.
Валентность серы
в сернистой кислоте равна IV, а степень окисления
+4.

Химические свойства сернистой кислоты
Общие свойства
кислот
- Сернистая кислота – слабая кислота, диссоциирует в две стадии. Образует два типа солей:
- кислые – гидросульфиты
H2SO3 ↔ HSO3— + H+
- средние – сульфиты
HSO3—↔ SO32- + H+
- Сернистая кислота самопроизвольно распадается на SO2 и H2O:
H2SO3 ↔ SO2 + H2O
Соли сернистой кислоты, сульфиты и гидросульфиты
Способы
получения сульфитов
Соли сернистой кислоты получаются при взаимодействии SO2 с щелочами и оксидами щелочных и щелочноземельных металлов:
SO2 + СаО = CaSO3
SO2 + Na2O → Na2SO3
SO2 + NaOH = NaHSO3
SO2 + 2NaOH = Н2O + Na2SO3
Физические
свойства сульфитов
Сульфиты
щелочных металлов и аммония растворимы в воде, сульфиты остальных металлов — нерастворимы
или не существуют.
Гидросульфиты
металлов хорошо растворимы в Н2O, а некоторые из
них, такие как Ca(HSO3)2 существуют
только в растворе.
Химические свойства сульфитов
Cернистая кислота – двухосновная, образует нормальные (средние) соли — сульфиты Mex(SO3)y и кислые соли — гидросульфиты Me(HSO3)x.
- Водные растворы сульфитов подвергаются гидролизу. Реакция среды – щелочная (окрашивают лакмус в синий цвет):
SO3— + Н2O = HSO3— + ОН—
Na2SO3 + Н2O = NaHSO3 + NaOH
Реакции, протекающие без изменения степени окисления:
- Реакция с сильными кислотами:
Na2SO3 + 2HCl = 2NaCl +
SO2↑ + Н2O
NaHSO3 + HCl = NaCl + SO2↑ + Н2O
- Термическое разложение сульфитов:
CaSO3 = СаО + SO2↑
- Нормальные сульфиты в водных растворах, при избытке SO2, переходят в гидросульфиты:
CaSO3 + SO2 + Н2O = Ca(HSO3)2
- Ионно-обменные реакции с другими солями, протекающие с образованием нерастворимых сульфитов:
Na2SO3 + ZnCl2 = ZnSO3↓ + 2NaCl
Окислительно-восстановительные реакции
Сульфиты, также как и SO2, могут быть как восстановителями, так и окислителями, т.к. атомы серы в анионах находятся в промежуточной степени окисления +4
- Окисление водных растворов сульфитов, и гидросульфитов до сульфатов:
Na2SO3 + Вr2 + Н2O = Na2SO4 + 2НВr
5K2SO3 + 2КМnO4 + 3H2SO4 = 6K2SO4 + 2MnSO4 + 3Н2O
Na2SO3 + HNO3 = 2NaNO3 + SO2 + H2O
- Твердые сульфиты при хранении на воздухе также медленно окисляются до сульфатов:
2Na2SO3 + O2 = 2Na2SO4
- При нагревании сухих сульфитов с активными восстановителями (С, Mg, Al, Zn) сульфиты превращаются в сульфиды:
Na2SO3 + ЗС = Na2S + ЗСО
- При нагревании сухих сульфитов до высоких температур сульфиты диспропорционируют, превращаются в смесь сульфатов и сульфидов:
4K2SO3 = 3K2SO4 + K2S
Серная кислота (H2SO4)
Способы
получения серной кислоты
В промышленности серную кислоту производят из серы, сульфидов
металлов, сероводорода и др.
Наиболее часто серную кислоту получают из пирита FeS2.
Основные стадии получения серной кислоты включают:
1.Обжиг пирита в кислороде в печи для обжига с получением сернистого газа:
4FeS2 +
11O2 → 2Fe2O3 +
8SO2 + Q
2. Очистка полученного сернистого газа от примесей в циклоне, электрофильтре.
3. Осушка сернистого газа в сушильной башне
4. Нагрев очищенного газа в теплообменнике.
5. Окисление сернистого газа в серный ангидрид в контактном аппарате:
2SO2 + O2 ↔ 2SO3 + Q
6. Поглощение серного ангидрида серной кислотой в поглотительной башне – получение олеума.

Физические
свойства, строение серной кислоты
При обычных условиях серная кислота – тяжелая бесцветная маслянистая жидкость, хорошо растворимая в воде. Максимальная плотность равна 1,84 г/мл
При растворении серной кислоты в воде выделяется большое количество теплоты. Поэтому, по правилам безопасности в лаборатории при приготовлении разбавленного раствора серной кислоты во избежание разбрызгивания необходимо наливать серную кислоту в воду тонкой струйкой по стеклянной палочке при постоянном перемешивании. Но не наоборот!
Валентность серы в серной кислоте равна VI.

Качественные
реакции для обнаружения серной кислоты и сульфат ионов
Для обнаружения сульфат-ионов используют реакцию с растворимыми солями бария. В результате взаимодействия, образуется белый кристаллический осадок сульфата бария:
BaCl2 + Na2SO4 → BaSO4↓ + 2NaCl
Видео Взаимодействие хлорида бария и сульфата натрия в растворе (качественная реакция на сульфат-ион).
Химические свойства серной кислоты
Серная кислота — сильная двухосновная кислота, образует два типа солей: средние – сульфаты, кислые – гидросульфаты.
- Серная кислота практически полностью диссоциирует в разбавленном в растворе по первой ступени и достаточно по второй ступени:
H2SO4 ⇄ H+ + HSO4–
HSO4– ⇄ H+ + SO42–
Характерны все свойства кислот:
- Реагирует с основными оксидами, основаниями, амфотерными оксидами, амфотерными гидроксидами и аммиаком:
H2SO4 + MgO → MgSO4 + H2O
H2SO4 + КОН → KHSО4 + H2O
H2SO4 + 2КОН → К2SО4 + 2H2O
3H2SO4 + 2Al(OH)3 → Al2(SO4)3 + 6H2O
H2SO4 + NH3 → NH4HSO4
- Вытесняет более слабые кислоты из их солей в растворе (карбонаты, сульфиды и др.) и летучие кислоты из их солей (кроме солей HBr и HI):
Н2SO4 + 2NaHCO3 → Na2SO4 + CO2 + H2O
H2SO4 + Na2SiO3 → Na2SO4 + H2SiO3
- Концентрированная серная кислота реагирует с твердыми солями, например нитратом натрия, хлорида натрия.
NaNO3(тв.) + H2SO4 → NaHSO4 + HNO3
NaCl(тв.) + H2SO4 → NaHSO4 + HCl
- Вступает в обменные реакции с солями:
H2SO4 + BaCl2 → BaSO4 + 2HCl
- Взаимодействует с металлами:
Разбавленная серная кислота взаимодействует с металлами, расположенными в ряду напряжения металлов до водорода. В результате реакции образуются соль и водород:
H2SO4(разб.) + Fe → FeSO4 + H2
H2SO4 + Zn = ZnSO4
+ H2
Концентрированная серная кислота — сильный окислитель. Реакция с металлами протекает без вытеснения водорода из кислоты. В зависимости от активности металла образуются различные продукты реакции:
- Активные металлы и цинк при обычной температуре с концентрированной серной кислотой образуют соль, сероводород (или серу) и воду:
H2SO4 + Na = Na2SO4 + Н2S↑ + H2O
5H2SO4(конц.) + 4Zn → 4ZnSO4 + H2S↑ + 4H2O
- Металлы средней активности с концентрированной H2SO4 образуют соль, серу и воду:
4H2SO4 + 3Mg → 3MgSO4 + S + 4H2O
-
Такие металлы, как железо Fe,
алюминий Al, хром Cr пассивируются концентрированной
серной кислотой на холоде. При нагревании,
при удалении оксидной пленки реакция возможна.
6H2SO4(конц.) + 2Fe → Fe2(SO4)3 + 3SO2 + 6H2O
6H2SO4(конц.) + 2Al → Al2 (SO4)3 + Н2S↑ + 6H2O
- Неактивные металлы восстанавливают концентрированную серную кислоту до сернистого газа:
2H2SO4(конц.) + Cu → CuSO4 + SO2 ↑ + 2H2O
2H2SO4(конц.) + Hg → HgSO4 + SO2 ↑ + 2H2O
2H2SO4(конц.) + 2Ag → Ag2SO4 + SO2↑+ 2H2O

- В реакциях с неметаллами концентрированная серная кислота также проявляет окислительные свойства:
5H2SO4(конц.) + 2P → 2H3PO4 + 5SO2↑ + 2H2O
2H2SO4(конц.) + С → СО2↑ + 2SO2↑ + 2H2O
2H2SO4(конц.) + S → 3SO2 ↑ + 2H2O
3H2SO4(конц.) + 2KBr → Br2↓ + SO2↑ + 2KHSO4 + 2H2O
5H2SO4(конц.) + 8KI → 4I2↓ + H2S↑ + K2SO4 + 4H2O
H2SO4(конц.) + 3H2S → 4S↓ + 4H2O (комнатная температура)
H2SO4(конц.) + H2S = S↓ + SО2↑ + 2Н2О (при нагревании)
H2SO4(конц.) + 2HBr = Br2 + SO2 + 2H2O
- Концентрированная серная кислота широко используется в химических процессах как водоотнимающий агент, т.к. проявляет сильное водоотнимающее действие. В органической химии ее используют при получении спиртов, простых и сложных эфиров, альдегидов и т.д.
Соли серной кислоты, сульфаты, гидросульфаты
Способы
получения солей серной кислоты
Сульфаты можно получить при взаимодействии серной кислоты с металлами,
оксидами, гидроксидами (см. Химические свойства серной кислоты). А также при
взаимодействии с другими солями, если продуктом реакции является нерастворимое
соединение.
Физические
свойства солей серной кислоты
Кристаллы разного цвета. Многие средние и кислые сульфаты растворимы
в воде. Плохо растворяются или не растворяются в воде сульфаты многозарядных
щёлочноземельных металлов (BaSO4, RaSO4), сульфаты лёгких
щёлочноземельных металлов (CaSO4, SrSO4) и сульфат свинца.
Средние сульфаты щелочных металлов термически устойчивы. Кислые
сульфаты щелочных металлов при нагревании разлагаются.
Многие средние сульфаты образуют устойчивые кристаллогидраты:
Na2SO4 ∙ 10H2O − глауберова
соль
CaSO4 ∙ 2H2O − гипс
2CaSO4 xH2O –
алебастр
CuSO4 ∙ 5H2O − медный купорос
FeSO4 ∙ 7H2O − железный купорос
ZnSO4 ∙ 7H2O − цинковый купорос
Na2CO3 ∙ 10H2O −
кристаллическая сода
KАl(SO4)2 x 12H2O
– алюмокалиевые квасцы.
Химические свойства солей серной кислоты
Разложение сульфатов на различные классы соединений в зависимости от металла, входящего в состав соли.
- Сульфаты щелочных металлов плавятся без разложения.
- Кислые сульфаты щелочных металлов разлагаются с отщеплением воды:
2KHSO4 → K2S2O7
+ H2O↑.
- Сульфаты металлов средней активности разлагаются на соответствующие оксиды:
ZnSO4
= ZnO + SO3
FeSO4
= 2Fe2O3 + 4SO2 + O2
2CuSO4 → 2CuO + SO2 + O2 (SO3)
2Al2(SO4)3 → 2Al2O3 + 6SO2 + 3O2
2Cr2(SO4)3 → 2Cr2O3 + 6SO2 + 3O2
- Сульфаты тяжёлых или малоактивных металлов разлагаются с образованием металла и кислорода:
HgSO4 = Hg + SO2 + O2
- Некоторые сульфаты проявляют окислительные свойства и вступают в реакции с простыми веществами:
CaSO4 +
C = CaO + SO2 + CO
BaSO4 +
4C = BaS + 4CO
Оксид серы (IV) – это кислотный оксид. Бесцветный газ с резким запахом, хорошо растворимый в воде.
Cпособы получения оксида серы (IV)
1. Сжигание серы на воздухе:
S + O2 → SO2
2. Горение сульфидов и сероводорода:
2H2S + 3O2 → 2SO2 + 2H2O
2CuS + 3O2 → 2SO2 + 2CuO
3. Взаимодействие сульфитов с более сильными кислотами:
Например, сульфит натрия взаимодействует с серной кислотой:
Na2SO3 + H2SO4 → Na2SO4 + SO2 + H2O
4. Обработка концентрированной серной кислотой неактивных металлов.
Например, взаимодействие меди с концентрированной серной кислотой:
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
Химические свойства оксида серы (IV)
Оксид серы (IV) – это типичный кислотный оксид. За счет серы в степени окисления +4 проявляет свойства окислителя и восстановителя.
1. Как кислотный оксид, сернистый газ реагирует с щелочами и оксидами щелочных и щелочноземельных металлов.
Например, оксид серы (IV) реагирует с гидроксидом натрия. При этом образуется либо кислая соль (при избытке сернистого газа), либо средняя соль (при избытке щелочи):
SO2 + 2NaOH(изб) → Na2SO3 + H2O
SO2(изб) + NaOH → NaHSO3
Еще пример: оксид серы (IV) реагирует с основным оксидом натрия:
SO2 + Na2O → Na2SO3
2. При взаимодействии с водой SO2 образует сернистую кислоту. Реакция обратимая, т.к. сернистая кислота в водном растворе в значительной степени распадается на оксид и воду.
SO2 + H2O ↔ H2SO3
3. Наиболее ярко выражены восстановительные свойства SO2. При взаимодействии с окислителями степень окисления серы повышается.
Например, оксид серы окисляется кислородом на катализаторе в жестких условиях. Реакция также сильно обратимая:
2SO2 + O2 ↔ 2SO3
Сернистый ангидрид обесцвечивает бромную воду:
SO2 + Br2 + 2H2O → H2SO4 + 2HBr
Азотная кислота очень легко окисляет сернистый газ:
SO2 + 2HNO3 → H2SO4 + 2NO2
Озон также окисляет оксид серы (IV):
SO2 + O3 → SO3 + O2
Качественная реакция на сернистый газ и на сульфит-ион – обесцвечивание раствора перманганата калия:
5SO2 + 2H2O + 2KMnO4 → 2H2SO4 + 2MnSO4 + K2SO4
Оксид свинца (IV) также окисляет сернистый газ:
SO2 + PbO2 → PbSO4
4. В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства.
Например, при взаимодействии с сероводородом сернистый газ восстанавливается до молекулярной серы:
SO2 + 2Н2S → 3S + 2H2O
Оксид серы (IV) окисляет угарный газ и углерод:
SO2 + 2CO → 2СО2 + S
SO2 + С → S + СO2









![mathsf{2SO_2 + O_2 xrightarrow[V_2O_5]{450^oC} 2SO_3}](https://dic.academic.ru/dic.nsf/ruwiki/99ec4a075f53d8fe12df7b248c54cdde.png)



